2. 中国医学科学院生物医学工程研究所, 天津 300193
2. Institute of Biomedical Engineering, Chinese Academy of Medical Sciences, Tianjin 300193, China
香连化滞丸是由黄连、木香、黄芩、枳实(麸炒)、陈皮、青皮(醋炙)、厚朴(姜炙)、槟榔(炒)、滑石、白芍(炒)、当归、甘草12味中药组成,方中黄连、黄芩清热燥湿为主药;木香、陈皮、青皮、枳实、厚朴行气止痛,滑石清热利湿,槟榔行气导滞共为辅药;白术健脾燥湿,当归养血活血为佐药;甘草调和诸药为使药。该中成药具有清热利湿、行血化滞的功效,用于湿热凝滞引起的里急后重,腹痛下痢;分别收载于《吉林省药品标准1977》《卫生部药品标准中药成方制剂第七册》《国家中成药标准汇编内科脾胃分册》《中国药典》2010年版第二增补本[1, 2, 3, 4]。《国家中成药标准汇编内科脾胃分册》中采用TLC法测定了盐酸小檗碱;《中国药典》2010年版第二增补本中采用HPLC法测定了盐酸小檗碱;中药尤其是复方中药,其发挥作用的物质基础是活性物质群,经多途径的整合而发挥疗效[5],特别是近年来对于中药的质量控制多采用HPLC法多指标控制的方法[6, 7, 8]。
对于香连化滞丸仅测定盐酸小檗碱的量并不能完全反映香连化滞丸的质量。为了更好地控制香连化滞丸的质量,根据组方中的中药组成,本实验采用梯度洗脱建立了同时测定香连化滞丸中芍药苷(白芍)[9]、甘草苷(甘草)、厚朴酚(厚朴)、阿魏酸(当归)、橙皮苷(陈皮、青皮)、木香烃内酯(木香)、去氢木香烃内酯(木香)、辛弗林(枳实)、黄芩苷(黄芩)、盐酸小檗碱(黄连)10种成分的HPLC法,所测10种成分的色谱峰与相邻色谱峰均能得到良好的分离,对香连化滞丸的质量控制奠定了基础。
1 仪器与材料FINNIGAN液相色谱仪,美国Finnigan公司;DL-360D智能超声波清洗器,上海之信仪器有限公司;BP211D型电子分析天平,德国Sartorius公司。
对照品芍药苷(批号110736-201337,质量分数94.9%)、橙皮苷(批号110721-201316,质量分数95.3%)、甘草苷(批号111610-201106,质量分数93.7%)、厚朴酚(批号110729-200412,质量分数98%)、阿魏酸(批号110773-201313,质量分数99.6%)、木香烃内酯(批号111524-201208,质量分数99.5%)、去氢木香烃内酯(批号111514-201206,质量分数99.5%)、辛弗林(批号110727-201107,质量分数99.4%)、黄芩苷(批号110715-201318,质量分数93.3%)、盐酸小檗碱(批号110713-201212,质量分数86.7%)均购于中国食品药品检定研究院。甲醇与乙腈为色谱纯,均购自美国Fisher公司。流动相用水为双蒸水(自制),其余试剂均为分析纯。香连化滞丸(西安正大制药有限公司,水丸,每10丸质量0.3 g,批号20130528、20130529、20130530、20130611、20130612、20130613)。
2 方法与结果 2.1 色谱条件色谱柱为Waters Symmetry-C18(150 mm×4.6 mm,3.5 μm);流动相为甲醇-乙腈-水(50∶45∶5,A)和甲醇-0.1%磷酸水溶液(4∶96,B),梯度洗脱:0~12.0 min,85% B;12.0~20.0 min,85%~55% B;20.0~28.0 min,55%~35% B;28.0~38.0 min,5% B;体积流量1.0 mL/min;分段变波长测定:0~13.0 min为230 nm,13.0~16.0 min为316 nm,16.0~20.0 min为345 nm,20.0~38.0 min为280 nm;柱温45 ℃;进样量10 μL。
2.2 对照品溶液的制备分别称取芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱对照品适量,精密称定,置于25 mL量瓶中,加甲醇-乙腈-水(50∶45∶5)至刻度,摇匀,制成质量浓度分别为60、20、40、20、500、100、100、30、60、30 μg/mL混合对照品溶液。混合对照品溶液色谱图见图 1。
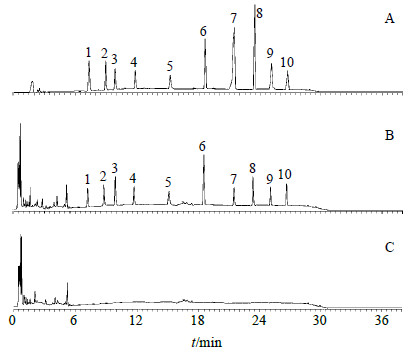 |
1-芍药苷 2-木香烃内酯 3-去氢木香烃内酯 4-甘草苷 5-阿魏酸 6-盐酸小檗碱 7-黄芩苷 8-橙皮苷 9-辛弗林 10-厚朴酚 1-paeoniflorin 2-costunolide 3-dehydrocostus lactone 4-liquiritin 5-ferulic acid 6-berberine 7-baicalin 8-hesperidin 9-synephrine 10-magnolol 图 1 混合对照品 (A) 、 样品 (B) 与阴性样品 (C) 溶液的 HPLC 图Fig.1 HPLC of mixed reference substances (A), sample (B), and negative sample (C) |
取质量差异项下的水丸,剪碎,取约l g,精密称定,置具塞锥形瓶中,加入甲醇-乙醇-水(50∶25∶25)溶液50 mL,称定质量,加热回流120 min,放冷,再称定质量,用上述混合溶液补足减失的质量,摇匀,滤过,取续滤液,即得。色谱图见图 1。
2.4 阴性样品溶液的制备制备缺相应药材的阴性样品,按“2.3”项方法操作,即得。阴性样品溶液色谱图见图 1。
2.5 线性关系考察精密吸取混合对照品溶液0.25、0.5、1.0、1.5、2.0、2.5 mL,分别置10 mL量瓶中,用甲醇-乙腈-水(50∶45∶5)定容至刻度,制成不同质量浓度的混合对照品溶液。分别精密吸取10 μL,进样测定,以峰面积为纵坐标(Y),质量浓度为横坐标(X)进行线性回归,得回归方程:芍药苷Y=11.451 X+265.13,r=0.999 2;甘草苷Y=23.111 X-21.729,r=0.999 1;厚朴酚Y=17.815 X-13.529 8,r=0.999 3;阿魏酸Y=76.211 X+87.361,r=0.999 5;橙皮苷Y=81.253 X-2.735 2,r=0.999 1;木香烃内酯Y=56.238 X-34.222 9,r=0.999 5;去氢木香烃内酯Y=11.343 X-6.246 6,r=0.999 2;辛弗林Y=34.765 X-12.235 5,r=0.999 2;黄芩苷Y=12.333 X+17.341,r=0.999 1;盐酸小檗碱Y=56.812 X-23.482 1,r=0.999 2;表明芍药苷在1.5~15.0 μg/mL、甘草苷在 0.5~5.0 μg/mL、厚朴酚在1.0~10.0 μg/mL、阿魏酸在0.5~5.0 μg/mL、橙皮苷在12.5~125.0 μg/mL、木香烃内酯在2.5~25.0 μg/mL、去氢木香烃内酯在2.5~25.0 μg/mL、辛弗林在0.75~7.5 μg/mL、黄芩苷在1.5~15.0 μg/mL、盐酸小檗碱在0.75~7.5 μg/mL线性关系良好。
2.6 方法学考察 2.6.1 精密度试验精密吸取“2.2”项制备的混合对照品溶液2 mL,置5 mL量瓶中,用甲醇-乙腈-水(50∶45∶5)定容至刻度,制成含芍药苷24.0 μg/mL、甘草苷8.0 μg/mL、厚朴酚16.0 μg/mL、阿魏酸8.0 μg/mL、橙皮苷200 μg/mL、木香烃内酯40.0 μg/mL、去氢木香烃内酯40.0 μg/mL、辛弗林12.0 μg/mL、黄芩苷24.0 μg/mL、盐酸小檗碱12.0 μg/mL的混合对照品溶液。精密吸取制备的混合对照品溶液10 μL,进样,连续进样6次,在上述色谱条件下测定,记录峰面积,计算得芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱峰面积的RSD分别为1.11%、1.24%、1.42%、1.73%、1.82%、1.28%、0.95%、1.02%、1.49%、0.65%。
2.6.2 稳定性试验取样品(批号20130521-1)按照“2.3”项下方法制备供试品溶液,分别在0、2、4、8、12、24 h进样,在上述色谱条件下测定,结果芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱峰面积的RSD分别为1.23%、1.62%、1.11%、0.86%、0.82%、0.91%、1.38%、0.72%、0.79%、1.24%,表明供试品溶液中10种有效成分在室温条件下12 h内稳定。
2.6.3 重复性试验取样品(批号20130521-1)6份,按照供试品溶液制备方法制备,在上述色谱条件下分别进样10 μL测定。结果供试品中芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱质量分数的RSD分别为0.64%、0.99%、1.22%、0.85%、1.10%、1.47%、1.49%、1.45%、1.03%、0.69%。
2.6.4 加样回收率试验称取批号20130521-1的供试品9份,精密称定,每份1.0 g,每3份加入相同量的芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱对照品,按“2.3”项下方法操作,制备供试品溶液,按“2.1”项条件测定,结果平均回收率分别为98.5%、101.1%、99.5%、101.4%、101.3%、99.7%、100.9%、100.1%、99.2%、100.4%,RSD分别为1.21%、1.23%、1.22%、1.62%、1.51%、1.49%、1.64%、1.28%、1.78%、1.25%。
2.7 样品测定取6批香连化滞丸,照“2.3”项下操作制备供试品溶液,每批平行3份,精密吸取供试品溶液10 μL,进样,每份进样3次,计算每批样品中各成分的量,结果见表 1。
| 表 1 香连化滞丸中指标性成分的质量分数(n=3) Table 1 Contents of target components in Xianglian Huazhi Pill(n=3) |
首次建立HPLC同时测定香连化滞丸中10种活性成分的方法,方法简便、结果可靠,可作为香连化滞丸多指标定量测定方法,可用于香连化滞丸的质量控制。
在选择指标成分时,根据组成药物的单味中药中的指标成分进行了梳理,根据《中国药典》对于每一种中药的检测指标,白芍的指标成分为芍药苷,木香的指标成分为木香烃内酯与去氢木香烃内酯,当归的指标成分为阿魏酸,甘草的指标成分为甘草苷,陈皮与青皮的指标成分为橙皮苷,黄芩的指标成分为黄芩苷,厚朴的指标成分为厚朴酚,枳实的指标成分为辛弗林,黄连的指标成分为小檗碱,确定了芍药苷、甘草苷、厚朴酚、阿魏酸、橙皮苷、木香烃内酯、去氢木香烃内酯、辛弗林、黄芩苷、盐酸小檗碱10个成分控制该中成药的质量。
在提取方式上,对提取溶剂与加热回流时间进行了较为详细的考察,分别考察了不同比例的甲醇-乙醇-水的提取效率,最后确定提取溶剂为甲醇-乙醇-水(50∶25∶25)。同时考察了20、40、60、120、180 min的加热回流时间,确定加热回流时间120 min较为合适。在波长选择上,根据每个指标成分的最大吸收波长,确定了检测波长,用分段变波长测定药物中各个指标的量。
| [1] | 吉林省药品标准 [S]. 1977. |
| [2] | 卫生部药品标准中药成方制剂第七册 [S]. 1993. |
| [3] | 国家中成药标准汇编内科脾胃分册 [S]. 2002. |
| [4] | 中国药典 [S]. 一部. 2010. |
| [5] | 安益强, 贾晓斌, 袁海建, 等. 板蓝根抗病毒物质基础研究思路 [J]. 中草药, 2008, 39(4): 616-619. |
| [6] | 郭 倩, 田成旺, 朱月信, 等. HPLC法同时测定疏风解毒胶囊中7种活性成分 [J]. 中草药, 2015, 46(8): 1174-1177. |
| [7] | 石 伟, 李家春, 刘汉清, 等. 基于多成分定量测定的六味地黄浓缩丸质量分析 [J]. 中草药, 2015, 46(7): 1002-1006. |
| [8] | 陈晓虎, 苏 晶, 王 慧, 等. UPLC法同时测定栀子金花丸中11种成分 [J]. 中草药, 2014, 45(7): 955-959. |
| [9] | 李玉仿. RP-HPLC法测定香连化滞丸中芍药苷的含量 [J]. 天津药学, 2007, 19(3): 8-10. |
 2015, Vol. 46
2015, Vol. 46


