2. 南京中医药大学 江苏省中药资源产业化过程协同创新中心, 江苏 南京 210023;
3. 江苏省儿童呼吸疾病(中医药)重点实验室, 南京中医药大学中医儿科学研究所, 江苏 南京 210023
2. Jiangsu Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. Jiangsu Key Laboratory of Pediatric Respiratory Disease, Institute of Pediatrics by Traditional Chinese Medicines, Nanjing University of Chinese Medicine, Nanjing 210023, China
香附四物汤出自清代梁廉夫《不知医必要》卷四,由当归、川芎、白芍、熟地、木香、香附、延胡索7味药组成,具有养血调血、行气止痛之功效,主治气滞血瘀所致痛经、月经不调等症[1, 2],为行气化瘀代表方之一。
曾有文献报道[3, 4, 5],对香附四物汤的物质基础进行研究,并对提取工艺进行了优化,制备了香附四物汤效应部位(BW)并提出阿魏酸、芍药苷、芍药苷内酯、普鲁托品、延胡索乙素、四氢非洲防己碱6个成分为BW的主要活性成分,其中阿魏酸主要来自当归和川芎,普鲁托品、延胡索乙素、四氢非洲防己碱主要来自延胡索。在此基础上将BW开发成外用制剂,研制了透皮贴剂,结果显示该制剂有较好的治疗效果[6]。但BW自身的透皮吸收性质还未见研究报道,本实验按照BW中6种活性成分的比例制备活性组分群,并考察了BW和活性组分群的体外透皮吸收性质。
1 仪器与材料TSQ Vantage型串联三重四级杆质谱仪,美国Thermo Fisher公司;Ultimate 3000型超高效液相色谱,美国Beckman Coulter公司;TK-12D透皮扩散试验仪,上海锴凯科技贸易有限公司;赛多利斯BSA-124S分析天平,赛多利斯科学仪器有限公司;TGL-20BR高速冷冻离心机,上海安亭科学仪器厂;S-210C酸度计,梅特勒公司;EP-ED超纯水机,南京易普易达科技发展有限公司;FD-1A-50冷冻干燥机,北京博医康实验仪器有限公司;KH5200E型超声波清洗机,昆山禾创超声仪器有限公司;DKZ-2电热恒温振荡水浴槽,上海精宏实验设备有限公司。
当归为伞形科当归属植物当归Angelica sinensis (Oliv.) Diels的干燥根、川芎为伞形科藁本属植物川芎Ligusticum chuanxiong Hort. 的干燥根茎、白芍为毛茛科芍药属植物芍药Paeonia lactiflora Pall. 的干燥根、熟地黄为玄参科地黄属植物地黄Rehmannia glutinosa Libosch. 的块根的炮制加工品、木香为菊科植物Aucklandia lappa Decne. 的干燥根、香附为莎草科莎草属植物莎草Cyperus rotundus L. 的干燥根茎、延胡索为罂粟科紫堇属植物延胡索Corydalis yanhusuo W. T. Wang的干燥块茎,药材饮片均购自安徽纪淞堂中药饮片有限公司,药材经南京中医药大学段金廒教授鉴定,药材质量均符合《中国药典》2010年版一部规定,标本收藏于南京中医药大学药学院药物制剂研究室。
对照品延胡索乙素(批号110726-201414,质量分数≥99.9%)、克拉霉素(质量分数≥98%,批号130558-201303)均购自中国食品药品检定研究院;对照品反式阿魏酸(批号20150112)、芍药内酯苷(批号20141128)、普鲁托品(批号20141209)、四氢非洲防己碱(批号20141124)、芍药苷(批号20141129),质量分数均≥98%,均购自南京春秋生物工程有限公司;D101大孔树脂,购自西安蓝晓科技有限公司;甲酸,色谱纯,Aladdin;乙腈、甲醇,色谱纯,Tedia;其余试剂均为分析纯。
雌性SD大鼠,200~220 g,购于上海杰思捷实验动物有限公司,合格证号SCXK(沪)2013-0006。
2 方法和结果 2.1 UPLC-MS/MS条件 2.1.1 液相条件色谱柱为Hibar HR C18柱(100 mm×2.1 mm,2 μm);流动相为乙腈-0.1%甲酸水溶液。梯度洗脱:0~1 min,10%乙腈;1~5 min,10%~30%乙腈;5~6 min,30%~75%乙腈;6~8 min,75%~10%乙腈;8~11 min,10%乙腈;体积流量0.4 mL/min;进样体积4 μL;柱温35 ℃。
2.1.2 质谱条件离子源:ESI源;扫描方式:多反应监测(MRM)方式;气化管温度:450 ℃;毛细管温度:350 ℃;喷雾电压:负离子(3 500 V),正离子(3 184 V)。各成分的质谱参数见表 1。
| 表 1 质谱参数 Table 1 Parameters of mass spectrometry |
分别取阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素对照品适量,精密称定,用甲醇溶解配制成对照品储备液;取适量的各成分储备液置于10 mL量瓶中,加甲醇稀释至刻度,配制成混合对照品溶液,其中阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的质量浓度分别为2 500.0、529.8、529.0、31.69、31.75、33.13 ng/mL。取上述混合对照品溶液用甲醇稀释成6份不同质量浓度的混标工作液。
精密称取克拉霉素对照品适量于量瓶中,用甲醇溶解配制成内标储备液,再取适量储备液用甲醇稀释至质量浓度为16.06 ng/mL的内标工作液。
精密量取混标工作液100 μL,加入100 μL内标工作液,混匀,19 000 r/min离心10 min。取上清液,按“2.1”项下UPLC-MS/MS方法进行分析。以被测化合物与内标的峰面积之比(Y)对质量浓度(X)进行线性回归,并按信噪比(S/N)>10计算被测组分的定量限(LOQ)。结果分别为阿魏酸Y=8.123×10−5 X-1.061×10−3,r=0.999 4,线性范围78.13~2 500.00 ng/mL,定量限78.13 ng/mL;芍药苷Y=1.804×10−4 X-1.505×10−3,r=0.999 7,线性范围16.56~529.75 ng/mL,定量限16.56 ng/mL;芍药内酯苷Y=1.888×10−4 X-3.602×10−4,r=0.999 8,线性范围16.53~529.00 ng/mL,定量限16.53 ng/mL;四氢非洲防己碱Y=0.337 7 X-0.156 3,r=0.999 0,线性范围0.99~31.69 ng/mL,定量限0.99 ng/mL;普鲁托品Y=0.210 3 X+0.561 9,r=0.997 7,线性范围0.99~31.75 ng/mL,定量限0.99 ng/mL;延胡索乙素Y=0.299 0 X+0.409 6,r=0.999 4,线性范围1.04~33.13 ng/mL,定量限1.04 ng/mL。各成分均有良好的线性关系,r值均>0.997。
2.3 方法学考察 2.3.1 精密度试验精密量取中质量浓度混标工作液(阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的质量浓度分别为312.5、132.5、132.3、7.9、7.9、8.3 ng/mL)100 μL,加内标工作液100 μL,连续进样6次,以各成分质量分数为指标,计算阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的RSD值分别为1.61%、0.94%、2.20%、2.53%、2.66%、1.83%,各成分精密度RSD≤2.66%,符合分析要求。
2.3.2 重复性试验按“2.4”项下方法制备BW供试液,平行6份,分别进样,以各成分质量分数为指标,计算阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的RSD分别为2.87%、2.56%、2.02%、2.98%、1.51%、1.00%,重复性RSD≤2.98%,符合分析要求。
2.3.3 稳定性试验用“2.5.2”项下空白接收液配制BW混悬液,置于37 ℃水浴,分别于0、2、4、8、12 h分别取样,进行UPLC-MS/MS分析,以被测化合物质量浓度为指标,计算RSD,考察方法的稳定性。结果阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的RSD分别为2.21%、1.68%、1.64%、3.51%、3.99%、2.27%,表明供试品溶液在12 h内稳定,各成分在空白皮肤接收液中12 h内稳定性RSD≤3.99%,均符合分析要求。
2.3.4 加样回收率试验取已测定的BW粉末适量,加入BW中各成分量的80%、100%、120%的对照品,各平行3份,用UPLC-MS/MS测定,计算加样回收率。结果各成分高、中、低回收率分别为阿魏酸(102.76±2.09)%、(97.11±6.52)%、(95.22±5.48)%,芍药苷(101.73±3.55)%、(97.06±2.08)%、(96.99±5.65)%,芍药内酯苷(103.65±1.13)%、(102.31±6.35)%、(96.32± 7.40)%、四氢非洲防己碱(99.18±1.40)%、(95.89± 2.14)%、(98.45±2.59)%,普鲁托品(102.89± 3.02)%、(102.02±3.26)%、(96.38±8.32)%,延胡索乙素(103.68±2.90)%、(98.97±2.67)%、(97.82±5.93)%,平均加样回收率95.22%~103.68%,符合分析要求。
2.3.5 方法专属性考察取空白皮肤接收液,按“2.5.3”项下方法处理(不加内标),作为空白样品;取已知质量浓度混标工作液100 μL,加入100 μL内标,获得混合对照样品;取已知浓度的BW溶液100 μL,加入100 μL内标,获得测试样品。按“2.1”项下UPLC-MS/MS方法进行测定,结果见图 1。皮肤接收液中的内源性物质不干扰各成分的测定,方法专属性良好。
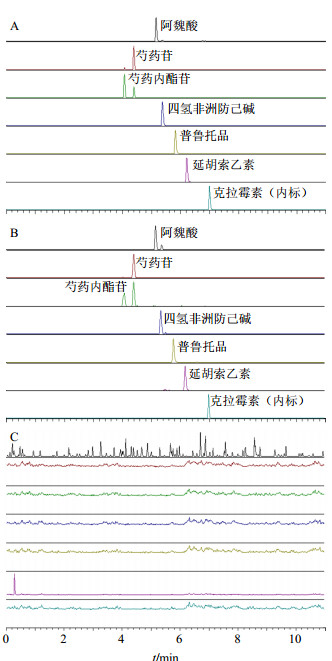 | 图 1 混合对照品+内标 (A)、样品溶液+内标 (B) 和空白皮肤接收液 (C) 中6个成分的MRM色谱图Fig.1 MRM chromatograms of six compounds in mixed reference substances + internal standard (A), sample solution + internal standard (B), and blank receptor solution (C) |
取当归、川芎、白芍、熟地、木香、香附、延胡索(6∶3∶3∶8∶2∶3∶3)药材饮片2.1 kg,加10倍量水浸泡12 h后连续煎煮2次,合并2次药液,加热浓缩至生药质量浓度为1 g/mL,加入95%乙醇至药液达到80%酒精度,静置24 h后取上清液浓缩至无醇味,浓缩液经大孔吸附树脂以水、20%乙醇、40%乙醇、60%乙醇梯度洗脱,收集60%乙醇洗脱部位(得率为0.366%),冷冻干燥后即得BW粉末。精密称取BW粉末适量,用50%甲醇超声溶解并定容,19 000 r/min离心10 min,精密量取上清液100 μL,加入100 μL内标,混匀,得BW供试液,用于UPLC-MS/MS分析。
经UPLC-MS/MS测定,BW中阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素的量分别为(4.65±0.11)%、(8.24±0.12)%、(3.00±0.09)%、(0.20±0.03)%、(0.24±0.01)%、(0.22±0.02)%(n=3)。
2.5 体外透皮吸收研究 2.5.1 离体皮肤的制备取大鼠,麻醉后用刀片将腹部毛剔除干净,24 h后脱颈处死,剥离腹部皮肤,除去皮下血管及组织,于−20 ℃保存。实验前将皮肤自然解冻,用20%乙醇水溶液清洗干净备用。
2.5.2 供给液与接收液的制备(1)BW混悬液的制备:精密称取BW粉末适量置于量瓶,用20%乙醇水溶液超声溶解,最终BW质量浓度为2.06 mg/mL(阿魏酸、芍药苷、芍药苷内酯、四氢非洲防己碱、普鲁托品、延胡索乙素的质量浓度分别为72.0、155.4、59.2、4.1、4.1、4.2 μg/mL)。用pH计测定其pH值为4.04。
(2)活性组分群溶液的制备:精密称取阿魏酸、芍药苷、芍药苷内酯、四氢非洲防己碱、普鲁托品、延胡索乙素适量(按照BW部位中6个成分的比例),用20%乙醇水溶液溶解,定容到10 mL。再用20%乙醇水溶液稀释一定倍数。最终得到活性组分群溶液(阿魏酸、芍药苷、芍药苷内酯、四氢非洲防己碱、普鲁托品、延胡索乙素的质量浓度分别为72.0、155.4、59.2、4.1、4.1、4.2 μg/mL)。用pH计测定其pH值为4.89,为活性组分群A。同法配制活性组分群B,质量浓度与活性组分群A相同,溶剂中加入适量醋酸调节其pH值与BW混悬液(pH值为4.04)相同。
(3)空白接收液的制备:20%乙醇水溶液,使用前37 ℃预热并超声除去气泡。
2.5.3 体外透皮吸收实验采用改良Franz扩散池(扩散面积为3.14 cm2,接收室体积为7.0 mL)进行透皮实验,将离体腹部皮肤固定于扩散池上,角质层向上,接收室加入接收液,将装好皮肤与接收液的扩散池放入透皮扩散仪,37 ℃,500 r/min,平衡1 h。精密量取供给液2.0 mL于供给室,BW和活性组分群A、B各平行3份;在0、1、2、4、6、8、10、12 h分别吸取0.2 mL接收液,及时补充等温空白接收液。接收液样品用甲醇稀释,19 000 r/min离心10 min,精密量取上清液100 μL,加入内标100 μL,进行UPLC-MS/MS分析。
按公式Q=(V总Cn+∑V取Cn-1)/A[8]求算不同时间单位面积的药物累积透过量;按公式Tn=AQn/Z总求算不同时间药物累积透过率,式中Q为单位面积累积透过量(μg/cm2),A为有效透皮吸收面积(cm2),V总为接收室体积(mL),V取为取样体积(mL),Cn为第n个取样点测得的接收液中药物质量浓度(μg/mL),Cn-1为第n-1个取样点测得的接收液中药物质量浓度(μg/mL),Tn为第n取样点的累积透过率,Qn为第n个取样点测得的单位面积累积透过量,Z总为供给室中加入的总药量。
6个成分的体外透皮吸收结果见图 2及表 2、3。图 2是各成分在不同时间点的累积透过率曲线。以各时间点单位面积累积透过量为纵坐标,时间(t)为横坐标作图,将曲线尾部直线部分数据进行线性回归,得到Q-t方程,直线的斜率为稳态流量[J,μg/(cm2·h)],渗透系数(K)=J/(3 600 C),C=Q/V总,结果见表 2。表 3是6个成分12 h的累积透过率的比较。
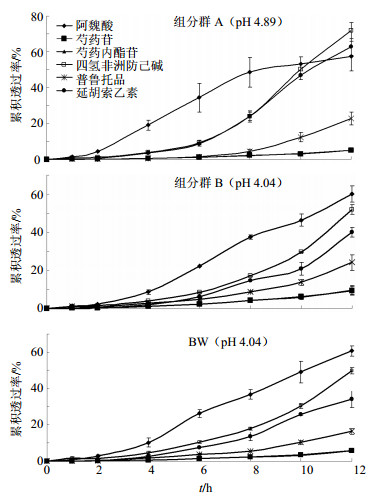 | 图 2 活性组分群A、B和BW中6个成分累积透过率曲线 (n = 3)Fig.2 Accumulate transmittance curves of six ingredients in active ingredient groups A, B, and BW (n = 3) |
| 表 2 体外透皮实验结果 Table 2 Results of in vitro transdermal experiment |
| 表 3 主要活性成分12 h累积透过率 (x±s, n = 3) Table 3 Cumulative transmittance rate of main active ingredients for 12 h (x±s, n = 3) |
从图 2可以看出,供给液pH值不同,6个成分在活性组分群中的累积透过率不同,活性组分群A(pH值为4.89)与活性组分群B(pH值为4.04)相比,延胡索乙素和四氢非洲防己碱的累积透过率变高,阿魏酸的累积透过率变低。从表 3中也可以看出pH值影响6个成分的累积透过率,特别是延胡索乙素、四氢非洲防己碱12 h的累积透过率在活性组分群A与BW中有统计学差异(P<0.05)。
将活性组分群与BW的pH值调节一致后,活性组分群B与BW中6个成分的累积透过率具有相同的顺序:阿魏酸>四氢非洲防己碱>延胡索乙素>普鲁托品>芍药苷≈芍药内酯苷,阿魏酸的累积透过率最高,T12为60%,而芍药苷和芍药内酯苷的T12在10%以下。表 2中,将活性组分群B和BW组6个活性成分的K值用单侧t检验,得到P值为0.499>0.1,无统计学差异,进一步说明这6个成分在活性组分群B(pH 4.04)和BW中有相似的透皮行为,BW中其他成分对这6个成分的体外透皮吸收无影响。
2.6 主要活性成分饱和溶解度的测定取阿魏酸、芍药苷、芍药内酯苷、四氢非洲防己碱、普鲁托品、延胡索乙素对照品适量,置于西林瓶中,加入0.5 mL 20%乙醇水溶液,各平行3份。37 ℃水浴振荡12 h,12 000 r/min离心5 min后立即取上清液,用甲醇稀释一定倍数,UPLC-MS/MS进行测定,按“2.2”项回归方程求得饱和溶解度。结果见表 4。从表 4中可知,在体外透皮实验中,6个成分均满足漏槽条件。
| 表 4 主要活性成分相关理化性质 (x±s, n = 3) Table 4 Physicochemical properties of main active ingredients (x±s, n = 3) |
张伯礼院士[9, 10]提出以组分配伍研究现代中药的观点,认为研究必须遵循“复杂-简单-复杂”的原则,借鉴现代药学的研究方法,发挥中医药理论优势,保持中药方剂的配伍特点,研制创新中药。在此基础上,苗明三等[11]对中药有效组分配伍研究进行探讨,认为中药有效组分配伍研究是开展中药现代研究的重要途径。本实验基于中药有效组分配伍的观点,首次以6个主要活性成分按照BW的比例制备活性组分群,将复杂的中药效应部位进行简化。体外透皮吸收实验结果显示,活性组分群B与BW中的6个成分透皮行为具有较高的一致性,BW中的其他成分对这6个成分的体外透皮吸收无影响。说明在透皮吸收研究中可以考虑用活性组分群B代替BW进行处方筛选优化。
本实验在体外透皮实验中发现pH值对BW的吸收行为具有显著影响,所以将活性组分群和BW的pH调至一致。因为6个成分pKa值从3.97~12.89,如阿魏酸pKa 3.97,3个生物碱的pKa在7.78~8.40,芍药苷和芍药内酯苷的pKa>12,溶液pH值从4.04变为4.89,会影响各成分的解离程度,从而会影响其透皮行为,且影响的程度不同。对阿魏酸和3个生物碱的影响较大,而对pKa>12的芍药苷和芍药内酯苷的影响不显著。
对在透皮制剂的处方优化和促渗剂筛选中,往往会忽视pH的影响,如油酸、丙二醇、氮酮等经常作为促渗剂[13, 14],很明显其中油酸(pKa 4.69)具有酸性,会影响基质的pH,从而影响药物的透皮吸收效果。在本实验中,由于6个成分的pKa和Mw差异很大,且pH对这6个成分的透皮行为的影响不同,所以,还要通过药效实验进一步来确定制剂的最佳pH值。
| [1] | 王 娟. 香附四物汤治疗原发性痛经气滞血瘀证疗效观察及其对凝血功能的影响 [D]. 南京: 南京中医药大学, 2012. |
| [2] | 董其虎, 王佩娟. 香附四物汤对原发性痛经 (气滞血瘀型) 凝血功能的影响 [J]. 中医药导报, 2012, 18(2): 34-35. |
| [3] | Liu P, Duan J A, Hua Y Q, et al. Effects of Xiang-Fu-Si-Wu Decoction and its main components for dysmenorrhea on uterus contraction [J]. J Ethnopharm, 2011, 133(2): 591-597. |
| [4] | 刘 培. 四物汤类方用于妇科血癖证原发性痛经的物质基础与配伍规律研究—香附四物汤的基础研究 [D]. 南京: 南京中医药大学, 2011. |
| [5] | 禹良艳, 华永庆, 刘 培, 等. 香附四物汤对大鼠卵巢颗粒细胞增殖的影响及活性部位成分分析 [J]. 南京中医药大学学报, 2011, 27(3): 238-242. |
| [6] | 李振皓. 香附四物汤用于原发性痛经外用制剂的研制 [D]. 南京: 南京中医药大学, 2013. |
| [7] | 李振皓, 刘 培, 钱大玮, 等. 香附四物汤全方及其效应部位中3个生物碱类成分在比格犬体内的药动学比较研究 [J]. 药物分析杂志, 2013, 33(3): 355-361. |
| [8] | 张传辉, 贾成友, 李 微, 等. 三七接骨凝胶膏剂的制备及体外透皮特性研究 [J]. 中草药, 2015, 46(5): 654-664. |
| [9] | 张伯礼, 王永炎. 方剂关键科学问题的基础研究—以组分配伍研制现代中药 [J]. 中国天然药物, 2012, 3(5): 174-178. |
| [10] | 张伯礼, 王永炎, 商洪才. 组分配伍研制现代中药的理论和方法 [J]. 继续医学教育, 2006, 20(19): 89-90. |
| [11] | 苗明三, 马 霄, 王 灿. 中药有效组分配伍研究的探讨 [J]. 中药新药与临床药理, 2009, 20(5): 487-490. |
| [12] | 钟江华, 周晓舟, 熊凤祥. 中药透皮吸收促进剂的研究进展 [J]. 氨基酸和生物资源, 2010, 32(4): 63-68. |
| [13] | 杨 柳, 王爱武, 苗 杰, 等. 6种透皮吸收促进剂对盐酸普萘洛尔乳膏透皮吸收性能的影响 [J]. 中国药房, 2013, 24(9): 2721-2723. |
| [14] | 邱 琳, 王乃婕, 杜 丰, 等. 促渗剂对青蒿琥酯贴剂体外经皮吸收的影响 [J]. 中药研究与开发, 2009, 16(10): 38-40. |
 2015, Vol. 46
2015, Vol. 46



