2. 大连美罗大药厂, 辽宁 大连 116034;
3. 咸阳职业技术学院 医学系, 陕西 咸阳 712000
2. Dalian Merro Pharmaceutical Factory, Dalian 116034, China;
3. Department of Medicine, Xianyang Vocational College, Xianyang 712000, China
穿心莲内酯(andrographolide,And)为爵床科穿心莲属植物穿心莲Andrographis paniculata (Burm. f.) Nees中提取得到的半日花烷型二萜内酯类化合物。据文献报道[1],And具有广谱的抗癌活性,可以抑制不同肿瘤细胞(乳腺癌、结肠癌、肝癌、子宫颈癌等)的增殖[2]。然而And在水中溶解度较低,口服生物利用度低,且口感极苦,口服时易致呕吐,患者依从性差,使其临床应用受到极大限制[3]。鉴于此,有学者对其新型制剂进行了尝试研究[4]。固体脂质纳米粒(solid lipid nanoparticles,SLNs)是近年正在发展的一种新型脂质载药系统,其采用固态的天然或合成的生理相容的高熔点脂质材料为载体,将药物包裹于类脂核中或吸附于纳米粒表面形成固体胶粒给药体系,是一种极有发展前景的新型给药系统的载体,可采用高压均质法进行工业化生产[5, 6, 7]。
近年来,随着药品质量管理研究的深入,质量控制模式也随之不断发生变化,药品质量源于设计(quality by design,QbD)的理念已逐渐被整个工业界所认可并实施。人用药物注册技术要求国际协调会(international conference on harmonization of technical requirements for registration of pharmaceuticals for human use,ICHQ8)中讨论了实施QbD需要以下5个要素:①建立目标产品质量特性(quality target product profile,QTPP);②利用风险分析工具,确定产品的关键质量属性(critical material attributes,CMA)和关键工艺参数(critical process parameter,CPP);③通过实验设计(design of experiment,DoE)建立产品生产工艺的设计空间(design space,DS);④开发出控制策略(control strategy,CS),形成控制空间;⑤大生产开始后,对生产过程进行实时检测和控制,持续改进(continuous improvement,CI),保证质量的稳定。
本研究以And为模型药物,采用QbD药物开发新理念制备And-SLNs,希望能够设计出理想的And载药系统,提高药物的口服生物利用度。
1 仪器与材料Agilent-1200高效液相色谱系统,安捷伦科技有限公司;BP211D电子天平,德国赛多利斯集团公司;DF2101S集热式恒温加热磁力搅拌器,河南巩义英峪予华仪器厂;IKA T18 ULTRA-TURRAX高速剪切机,德国IKA集团公司;Master-sizer 2000粒度分析仪、AH-100D高压均质机,加拿大ATS工业系统有限公司;Zetasizer Nano电位分析仪,英国马尔文公司;JM21200EX透射电镜、GC2120GX日立冷冻离心机,日本日立公司。
And,批号20120507-B,质量分数>98.5%,四川什邡华康药物原料厂;And对照品,批号110797-201108,质量分数>99.5%,中国食品药品检定研究院;注射用大豆磷脂,上海太伟药业有限公司;泊洛沙姆188(Fluronic F-68)、山嵛酸甘油酯(Compritol-888 ATO),德国巴斯夫公司;聚山梨酯80(Tween 80),上海申宇医药化工有限公司;甲醇,色谱纯,天津博迪化工有限公司;其他试剂均为分析纯。
2 方法与结果 2.1 建立And-SLNs的QTPP通过文献信息调研[8],考虑到临床给药特点,确定本制剂的剂型、给药途径、规格、容器密闭系统等信息,建立了And-SLNs的QTPP,见表 1。
| 表 1 And-SLNs的QTPP Table 1 QTPP of And-SLNs |
And-SLNs采用热熔乳化-高压均质法制备[7]。称取处方量的And和山嵛酸甘油酯,置于2 mL无水乙醇中,在恒温(75±1)℃水浴磁力搅拌下溶解,形成油相;称取处方量的大豆磷脂和助表面活性剂(F68或聚山梨酯80)置于20 mL纯化水中,在恒温(75±1)℃水浴条件下分散均匀,形成水相;在高速剪切机(10 000 r/min)分散条件下,将水相缓慢滴加到油相中,恒温(75±1)℃持续分散5 min,挥干乙醇,制得初乳。将初乳在保温条件下用高压均质机进一步减小粒径通过调节均质压力和均质次数可得到淡蓝色透明的胶体溶液。采用冰水浴迅速将SLNs充分冷却,即得And-SLNs。
同法制备不含And的SLNs,即得空白SLNs。
2.3 And-SLNs的风险分析本研究采用鱼骨图法评估可能影响And-SLNs性质的风险因素,并对各因素进行排列和比较,找出影响And-SLNs性质的各种因素,结果见图 1。
 | 图 1 And-SLNs鱼骨图Fig.1 Fishbone diagram of And-SLNs |
色谱柱为菲罗门C18柱(250 mm×4.6 mm,5 μm),流动相为甲醇-水(60∶40),检测波长225 nm,体积流量1 mL/min,柱温30 ℃,进样量20 μL。
2.4.2 对照品溶液的配制精密称取And对照品10 mg置50 mL量瓶中,甲醇溶解,定容至50 mL,稀释至刻度,即得200 μg/mL And对照品储备液。取上述储备液5 mL置100 mL量瓶中,以流动相稀释定容至刻度,过0.45 μm微孔滤膜,取续滤液,即得10 μg/mL And对照品溶液。
2.4.3 样品溶液的配制精密称取And-SLNs溶液5 mL,置50 mL量瓶中,加入30 mL甲醇超声溶解后,加入纯化水稀释至刻度,振荡摇匀。取上述溶液5 mL置100 mL量瓶中,以流动相稀释定容刻度,过0.45 μm微孔滤膜,取续滤液,即得样品溶液。
2.4.4 线性关系考察精密量取And对照品储备液,用流动相稀释成2.0、5.0、10.0、20.0、50.0 μg/mL的对照品溶液,摇匀,滤过,精密吸取20 μL,按“2.4.1”项色谱条件测定。以And质量浓度(X)对峰面积积分值(Y)进行线性回归,得回归方程Y=79.416 X-116.4,r=0.999 9;可见And在2.0~50.0 μg/mL与峰面积线性关系良好。
2.4.5 专属性考察取按“2.2”项下方法制备的And-SLNs溶液、空白SLNs溶液以及And对照品溶液,分别照“2.4.1”项下色谱条件测定,色谱图见图 2。结果表明,在本色谱条件下,辅料对And测定无干扰;主峰理论塔板数为4 000,拖尾因子在0.95~1.05,符合测定要求。
 | 图 2 空白辅料 (A)、And-SLNs (B)、And对照品 (C) 的HPLC图Fig.2 HPLC of blank excipients (A),And-SLNs (B),and And reference substance (C) |
按“2.4.2”项下制备1份对照品溶液,在“2.4.1”项下色谱条件重复进样6次,测定And的峰面积,并计算6份对照品溶液峰面积平均值及其RSD值。结果其RSD为0.79%,表明仪器精密度良好,符合定量测定要求。
2.4.7 重复性试验取And-SLNs溶液6份,按“2.4.3”项下配制样品溶液,以“2.4.1”项下色谱条件进样测定。结果And-SLNs溶液中药物质量浓度的RSD为1.25%,表明重复性较好。
2.4.8 加样回收率试验按制剂处方量的80%、100%、120%比例精密移取And对照品溶液至20 mL量瓶中,各3份,分别加入5 mL空白SLNs,加流动相稀释至刻度,振荡摇匀,制成高、中、低质量浓度的回收率试验溶液,进样测定,计算And的回收率,结果表明高、中、低3个质量浓度的平均回收率为99.4%,RSD为0.94%,回收率良好。
2.4.9 稳定性试验取And样品溶液,分别在0、4、8、12、24、36、48、72 h进样测定,记录峰面积。结果And峰面积的RSD为1.94%,表明样品溶液在72 h内稳定。
2.5 包封率的测定采用低温超速离心法测定And-SLNs中And的包封率。取2.0 mL And-SLNs加到超速离心管中,在50 000 r/min的条件下离心1 h,吸取上清液;同时精密移取And-SLNs 1.0 mL于10 mL量瓶中,用甲醇破坏And-SLNs并定容稀释至刻度,采用“2.4.1”项下色谱条件测定And-SLNs中And的总质量浓度。利用公式计算And在And-SLNs中的包封率。
包封率=(And在And-SLNs中的总质量浓度-游离And的质量浓度)/And在And-SLNs中的总质量浓度
2.6 实验设计 2.6.1 Plackett-Burman实验设计筛选变量通过对And-SLNs处方及制备工艺的分析,以药物质量浓度(X1,mg/mL)、山嵛酸甘油酯质量浓度(X2,mg/mL)、大豆磷脂质量浓度(X3,mg/mL)、表面活性剂种类(X4)、均质压力(X5,MPa)、均质温度(X6,℃)、均质次数(X7)为考察对象,以包封率(Y1,%)、粒径分布(Y2,nm)为评价指标,利用Plackett-Burman实验设计筛选出对And-SLNs性质影响较显著的因素。因素水平、筛选试验安排及结果见表 2。
| 表 2 Plackett-Burman实验设计与效应值 Table 2 Plackett-Burman experimental design and effect values |
由Pareto图(图 3)可知,山嵛酸甘油酯质量分数、大豆磷脂质量分数对And-SLNs包封率有显著影响(P<0.05);均质压力对And-SLNs的粒径分布有显著影响(P<0.05)。因此,固定药物质量分数、表面活性剂种类、均质次数和均质温度不变,采用山嵛酸甘油酯质量浓度为50~100 mg/mL,大豆磷脂质量浓度为40~80 mg/mL,均质压力为60~100 MPa,应用Box-Behnken效应面法进一步优化。
 | 图 3 Plackett-Burman实验设计变量筛选时标准化效应的Pareto图 (α = 0.05)Fig.3 Pareto charts of standardized effect values on variable screening by Plackett-Burman experimental design (α = 0.05) |
通过Plackett- Burman实验设计,筛选出对And-SLNs性质影响较显著的3个因素:山嵛酸甘油酯质量浓度(X1,mg/mL),大豆磷脂质量浓度(X2,mg/mL)、均质压力(X3,MPa)。以该3个因素为考察对象,以包封率(Y1,%)、平均粒径(Y2,nm)为评价指标,利用Box-Behnken效应面法对And-SLNs处方和工艺进行优化。因素水平、处方优化试验安排及结果见表 3。试验过程中固定的处方和工艺参数为药物质量浓度15 mg/mL,表面活性剂种类F68,均质次数8次,均质温度70 ℃。
| 表 3 Box-Behnken实验设计与效应值 Table 3 Box-Behnken experimental design and effect values |
由表 4中数据结果可知,方程中X1、X2、X1X2、X12、X32对包封率影响较显著,由相关系数可知,包封率与山嵛酸甘油酯质量浓度成正相关,与大豆磷脂质量浓度呈负相关(图 4)。
| 表 4 拟合方程中各项的系数及显著性检验结果 Table 4 Each coefficient in fitting equation and its significant test results |
 | 图 4 自变量X1、X2与因变量Y1的3D效应面图Fig.4 3D Response surface of independent variables X1and X2 and dependent variable Y1 |
由表 4中数据结果可知,方程中X1、X2、X3、X1X2、X1X3、X2X3、X12、X22、X32对平均粒径影响较显著,由相关系数可知,平均粒径与山嵛酸甘油酯质量浓度呈正相关,与大豆磷脂质量浓度、均质压力呈负相关(图 5)。
 | 图 5 各自变量 (X1、X2、X3) 与因变量Y2的3D效应面图Fig.5 3D Response surface of independent variables X1,X2,and X3 and dependent variable Y2 |
根据Design expert 7.0实验设计软件综合评价后给出的最佳制备条件:山嵛酸甘油酯质量浓度为80 mg/mL、大豆磷脂质量浓度为60 mg/mL、均质压力为85 MPa。以优化的最优处方按照“2.2”项下制备3批And-SLNs,按照“2.5”和“2.7”项下测定固体脂质纳米粒包封率和平均粒径,实测值与模型预测值见表 5,由表可知实验观察值和模型预测值比较接近,说明模型预测性良好。
| 表 5 各指标预测值和实测值 Table 5 Predicted and observed response values for each index |
取And-SLNs溶液适量,用蒸馏水稀释适量倍数,采用Malvern粒度测定仪测定固体脂质纳米粒的粒径分布和Zeta电位。由图 6可见,And-SLNs平均粒径为(258.4±42.1)nm,多分散指数(PDI)为0.215±0.025,Zeta电位为(-36.1±3.4)mV。
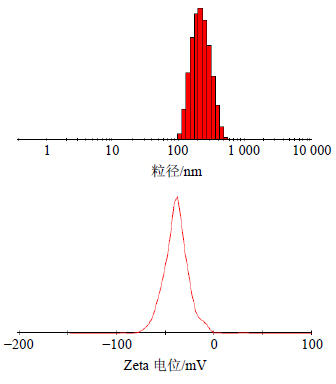 | 图 6 And-SLNs粒径分布和Zeta电位Fig.6 Particle size distribution and Zeta potential of And-SLNs |
采用磷钨酸负染法制备透射电镜样品。取And- SLNs适量,加入重蒸馏水稀释适当倍数,滴加在憎水基质的表面,将附Formvar膜的铜网放入固体脂质纳米粒中浸泡15 min,用滤纸吸除大部分水分,滴加2%的磷钨酸水溶液,染色5 min,用滤纸吸去水分,将铜网取出,待干后用透射电镜观察固体脂质纳米粒的形态结构。由图 7可见,And-SLNs大小均匀,成球形或椭球形,大部分粒子的粒径在200 nm左右,未见到过大的粒子,透射电镜观察进一步确证了粒度测定的结果。
 | 图 7 And-SLNs透射电镜照片Fig.7 TEM photo of And-SLNs |
采用透析法[9]考察And-SLNs在PBS(pH 7.4)中的释放行为。释放介质为0.5%聚山梨酯80的PBS可以保证药物释放在漏槽状态下进行。精密吸取固体脂质纳米粒2 mL置于处理好的透析袋内,平行3份,扎紧后置于溶出仪的桨叶底部,移取48 mL释放介质于溶出仪的小杯中,于(37.0±0.5)℃水浴中以50 r/min恒速旋转,分别于1、2、4、6、8、l2、16、20、24、30、36、42、48 h吸取1 mL释放介质(同时补加等量、同温的释放介质),采用“2.4”项下方法测定And的量,并计算游离药物的累积释放度。
体外释放研究结果(图 8)表明,固体脂质纳米粒中药物开始出现突释,主要是由于固体脂质纳米粒中游离药物以及吸附在纳米粒表面的药物首先释放,在6 h后药物释放较平缓,48 h累积释放度为52.4%,表明固体脂质纳米粒有延缓And释放的作用。
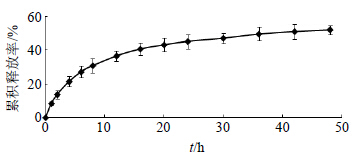 | 图 8 And-SLNs体外释放曲线 (n = 3)Fig.8 In vitro release profile of And-SLNs (n = 3) |
QbD的基本内容是以预先设定的目标产品质量特性作为研发的起点,在了解关键物质属性和关键工艺参数的基础上,通过实验设计,研究产品的关键质量属性。在多个影响因素下,建立能满足产品性能且工艺稳健的设计空间,并根据设计空间,建立质量风险管理,确立质量控制策略和药品质量体系。实施QbD是将过程分析技术与风险管理综合应用于药品工艺开发的过程,其目的不是消灭生产过程中的偏差,而是建立一种可以在一定范围内调节偏差来保证产品质量稳定性的生产工艺。
实验设计(DoE)是研究正确的实验计划和分析实验数据的理论和方法,通过改变过程的输入因素,观察其相应的输出响应变化,从而获取关于这个过程的知识,确定各个输入因素的重要性以及各输入因素如何影响输出响应,并如何达到最优化过程的目的。本研究首先通过Plackett-Burman实验设计筛选出对And固体脂质纳米性质影响较为显著的3个因素(山嵛酸甘油酯、大豆磷脂浓度和均质压力),然后通过Box-Behnken效应面法优化得到最优制备处方和工艺。
| [1] | 杨 静. 穿心莲内酯的研究进展[J]. 中草药, 2009, 40(7): 1168-1170. |
| [2] | Varma A, Padh H, Shrivastava N. Andrographolide: A new plant-derived antineoplastic entity on horizon[J]. Evid Based Complment Altermat Med, 2011, doi: 10. 1093/ecam/nep135, 2011-02-10. |
| [3] | Ye L, Wang T, Tang L, et al. Poor oral biolavailability of a promising anticancer agent andrographolide is due to extentive metabolism and efflux by P-glycoprotein[J]. J Pharm Sci, 2011, 100(11): 5007-5017. |
| [4] | 王 芳, 翟文婷, 李艳丽, 等. Box-Behnken效应面法优化穿心莲内酯-PLGA微球处方研究[J]. 中草药, 2013, 44(13): 1743-1747. |
| [5] | Mehnert W, Mäder K. Solid lipid nanoparticles Production, characterization and applications[J]. Adv Drug Deliv Rev, 2001, 47(2/3): 165-196. |
| [6] | 瞿 文, 陈庆华, 朱宝泉. 固体脂质纳米粒的研究进展[J]. 中国医药工业杂志, 2001, 32(9): 424-429. |
| [7] | Müller R H, Mäder K, Gohla S. Solid lipid nanoparticles (SLN) for controlled delivery-a review of the state of the art[J]. Eur J Pharm Biopharm, 2000, 50(1): 161-177. |
| [8] | 王 芳, 翟文婷, 李艳丽, 等. Box-Behnken效应面法优化穿心莲内酯-PLGA微球处方研究[J]. 中草药, 2013, 44(13): 1743-1747. |
| [9] | Hao J F, Fang X S, Zhou Y F. Development and optimization of solid lipid nanoparticle formulation for ophthalmic delivery of chloramphenicol using a Box-Behnken design[J]. Int J Nanomed, 2011, 47(6): 683-692. |
 2015, Vol. 46
2015, Vol. 46

