半枝莲Scutellaria barbata D. Don为唇形科(Labiatae)黄芩属Scutellaria L. 植物,收载于《中国药典》2015年版,又名并头草、牙刷草、花半菊、狭叶韩信草等,常生长在湿润草地及近水处,分布在河北、陕西、湖北、河南、广东等地,全草入药,具有清热解毒、化瘀利尿功效,主治咽喉肿痛、疔疮肿痛、毒蛇咬伤、肝炎、肿瘤等症[1]。半枝莲化学成分包含黄酮类、二萜及二萜酯类、生物碱类、挥发油类、多糖类等[2],半枝莲的抗肿瘤活性成分包括黄酮类、多糖等[3, 4],近年在半枝莲中的二萜类化合物中发现了新克罗烷型二萜具有显著抗肿瘤活性[5, 6]。本实验从95%乙醇半枝莲全草的醋酸乙酯部位分离出1个新的克罗烷型二萜化合物,命名为半枝莲二萜J(scutellone J,1)。结构见图 1。
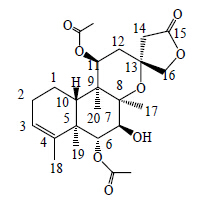 | 图 1 化合物1的结构Fig.1 Structure of compound 1 |
AV600MHz液体核磁共振质谱仪(Bruker公司);AL300核磁共振质谱仪(JEOL);6130 SQ质谱仪(Agilent公司);双压线性离子阱串联高分辨质谱Orbitrap Velos Pro(Thermo Fisher公司);Nicolet 6700傅里叶变换红外光谱仪(Thermo);AUTOPOL V plus高精度旋光仪(Rudolph);旋转蒸发器N-1100、油浴锅OSB-2100(上海爱朗仪器有限公司);DX-204冷水循环机(北京长流科学仪器公司);MPC 301Z真空泵(伊尔姆真空设备贸易有限公司);Sartorius BP 211 D型分析天平(德国赛多利斯公司);KQ3200DB型数控超声波清洗器(昆山市超声仪器有限公司);Sephadex LH-20葡聚糖凝胶(GE healthcare);MCI CHP20/P120(日本三菱公司);Sunchrom SP-120-40/75-ODS-A C18(北京金欧亚科技发展有限公司)。薄层色谱硅胶G、GF254、160~200目柱色谱硅胶(青岛海洋化工有限公司);色谱甲醇、乙腈(Fisher);超纯水和蒸馏水为本实验室自制;其他试剂均为分析纯试剂(北京化工厂)。
半枝莲干燥全草购自北京仟草中药饮片有限公司,产地为江苏。样品经北京中医药大学刘春生教授鉴定为唇形科黄芩属植物半枝莲Scutellaria barbata D. Don的干燥全草。
2 提取与分离干燥半枝莲全草40 kg粉碎,95%乙醇回流提取,减压回收溶剂浓缩为10 kg浸膏,继而蒸至无醇味,加水弥散,分别用等体积的石油醚、醋酸乙酯各萃取3次,回收溶剂得到石油醚、醋酸乙酯(793.6 g)及水部位。醋酸乙酯部位经硅胶柱色谱分离,依次用石油醚-醋酸乙酯(1∶0、9∶1、8∶2、7∶3、5∶5、3∶7、0∶1),甲醇进行系统分离,得8组馏份Fr. A1~A8。馏份Fr. A6(57.6 g)经硅胶柱色谱分离,以石油醚-醋酸乙酯(9∶1→0∶1)洗脱,得到馏分Fr. B1~B9。馏份Fr. B4 56~62(11.9 g)经MCI柱分离,80%甲醇洗脱,得到Fr. C5~C8(2.2 g);Fr. C5~C8再经ODS柱分离,80%甲醇洗脱,得到Fr. D1(0.5 g),Fr. D1再经Sephadex LH-20柱分离,甲醇洗脱,得到Fr. E,在Fr. E17中得到化合物1(15 mg)。
3 结构鉴定化合物1:白色结晶(甲醇-氯仿)。[α]25D −68.574° (c 0.102,MeOH)。HR-ESI-MS m/z: 473.218 1 [M+Na]+(计算值473.215 2),确定分子式为C24H34O8,不饱和度为8。IR吸收给出-OH(3 434 cm−1)、γ-内酯 (1 787 cm−1)、C=O (1 727 cm−1)、C=C (1 621 cm−1) 特征信号峰。1H-NMR和13C-NMR数据见表 1。
| 表 1 化合物1的1H-NMR (600 MHz,CDCl3)和13C-NMR (150 MHz,CDCl3)数据 Table 1 1H-NMR (600 MHz, CDCl3) and 13C-NMR (150 MHz, CDCl3)dataof compound 1 |
1H-NMR和13C-NMR给出4个甲基信号 [δH1.46 (3H, s, H-17), 1.59 (3H, s, H-18), 1.16 (3H, s, H-19), 0.98 (3H, s, H-20)],2个乙酰氧羰基信号 (δC 171.1, 169.3),1个C8-C13醚桥结构单元 [δH 1.46 (3H, s, H-17), δC 18.9 (C-17);δC 83.4 (C-8);δC 75.7 (C-13)] 及1个C13螺C15-C16 γ-内酯环结构片段 [δH 2.83 (1H, d, J = 17.4 Hz, H-14a), 2.72 (1H, d, J = 17.4 Hz, H-14b), 4.29 (1H, d, J = 9.0 Hz, H-16a), 4.18 (1H, d, J = 9.0 Hz, H-16b);δC 41.6 (CH2, C-14), 173.0 (C, C-15), 78.0 (CH2, C-16)]。1H-1H COSY图谱可观察到δH 2.35 (1H, m, H-1a), 1.53 (1H, m, H-1b) 与2.02 (2H, m, H-2), 2.25 (1H, d, J = 13.0 Hz, H-10) 相关,2.02 (2H, m, H-2) 与5.25 (1H, brs, H-3) 相关, 可确定双键位置在C3-C4位;δH4.98 (1H, d, J = 9.9 Hz, H-6) 与3.45 (1H, d, J = 9.9 Hz, H-7) 相关,由耦合常数确定C-6与C-7为反式构型。以上基团及结构单元波谱数据与scutelinquanine D文献数据[7]相似,由此推测化合物1具有新克罗烷型二萜母核结构。与化合物scutelinquanine D比较,显示化合物1无烟酸酰基片段,而有2个乙酰氧基基团,结合HMBC谱(图 1)显示H-11与δC 169.3相关、H-6与δC171.1相关,说明2个乙酰氧基分别连在C-11位和C-6位。该化合物的在NOESY谱(图 2)中,δH 1.46
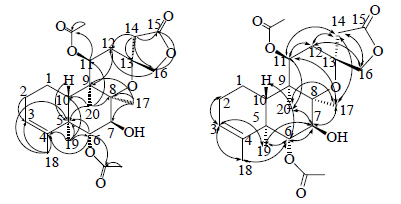 | 图 2 化合物1主要的HMBC图和NOESY相关图Fig.2 Key HMBC and NOESY correlations of compound 1 |
(H-17) 与3.45 (H-7)、5.37 (H-11)、2.82 (H-14a)、2.72 (H-14b)、0.98 (H-20) 相关,0.98 (H-20) 与3.45 (H-7)、5.37 (H-11)、1.46 (H-17)、1.16 (H-19) 相关,4.98 (H-6) 与2.25 (H-10) 相关,5.37 (H-11) 与1.89 (H-12a)、1.85 (H-12b)、2.82 (H-14a)、2.72 (H-14b)、1.46 (H-17)、0.98 (H-20) 相关。说明H-7、H-11、H-14、H-17、H-19、H-20同平面且为α构型,而H-6、H-10为β构型。基于上述数据最终确定新化合物为 (13R)-7β-羟基-8,13-螺-6α,11β-二乙酰氧基-3-烯- 15,16-新克罗烷内酯。此化合物为新结构并命名为半枝莲二萜J。
| [1] | 陈裕, 李世全, 罗小飞. 新编中草药实用图典[M]. 北京:农村读物出版社, 2012. |
| [2] | 林敬明, 刘煜, 罗荣城. 半枝莲的化学成分及其抗肿瘤作用的研究现状[J]. 中药材, 2006, 29(4):407-410. |
| [3] | 张秀娟, 杨姗姗. 半枝莲多糖体内抗肿瘤及其免疫调节作用的实验研究[J]. 亚太传统医药, 2008, 4(2):54-56. |
| [4] | 窦锦明, 荆汉卫. 半枝莲黄酮类有效部位体内抗肿瘤实验研究[J]. 药学与临床研究, 2015, 23(1):21-22. |
| [5] | Dai S J, Peng W B, Shen L, et al. Two new neo-clerodane diterpenoid alkaloids from Scutellaria barbata with cytotoxic activities[J]. J Asian Nat Prod Res, 2009, 11(5):451-456. |
| [6] | Nie X P, Qu G W, Yue X D, et al. Scutelinquanines A-C, three new cytotoxic neo-clerodane diterpenoid from Scutellaria barbata[J]. Phytochem Lett, 2010, 3(4):190-193. |
| [7] | Qu G W, Yue X D, Li G S, et al. Two new cytotoxic ent-clerodane diterpenoids from Scutellaria barbata[J]. J Asian Nat Prod Res, 2010, 12(10):859-864. |
 2015, Vol. 46
2015, Vol. 46


