2. 吉林农业大学中药材学院, 吉林 长春 130118;
3. 沈阳师范大学, 辽宁 沈阳 110034
2. College of Chinese Material Medicine, Jilin Agricultural University, Changchun 130118, China;
3. Shenyang Normal University, Shenyang 110034, China
五味子咀嚼片由五味子、丹参、野菊花、茯苓、香附组成,用于酒精性肝损伤的预防和治疗。目前已有五味子、丹参、野菊花、茯苓、香附单独的指纹图谱研究报道[1, 2, 3, 4, 5, 6, 7, 8, 9],但采用HPLC-DAD技术[10]对同时含有这5种药材的药物指纹图谱研究尚未见报道。本实验建立了10批五味子咀嚼片的HPLC-DAD指纹图谱,相似度均大于0.90,并确认了五味子中五味子醇甲、五味子醇乙、五味子酯甲、五味子乙素、五味子丙素;丹参中丹参素钠、原儿茶醛、丹酚酸B、隐丹参酮、丹参酮IIA;野菊花中木犀草苷和蒙花苷,为五味子咀嚼片的鉴定及质量控制提供了科学依据。
1 仪器与材料LC-20A高效液相色谱仪,SPD-M20A二极管阵列检测器,SIL-10AF自动进样器,LC-15C二元梯度泵,LC-solution色谱工作站,日本岛津公司;AK-400A粉碎机,温岭市奥力中药机械有限公司;BT-25S天平,德国赛多利斯公司;HH-4数显恒温水浴锅,常州中捷实验仪器制造有限公司。
对照品五味子醇甲、五味子酯甲、五味子乙素、丹参素钠、丹酚酸B、隐丹参酮、丹参酮IIA、原儿茶醛、木犀草苷和蒙花苷购于中国食品药品检定研究院,批号分别为110857-201309、111529-201306、110855-201412、110765-201005、111652-201311、110852-200806、110766-201012、110810-201007、111720-201408、11528-201308,质量分数均>98%;对照品五味子醇乙和五味子丙素购于成都瑞芬思生物科技有限公司,批号分别为W-008-140801、W-009-140801,质量分数均>98%。纯净水为超纯水,乙腈为色谱纯,其余均为分析纯。
五味子咀嚼片由吉林省公共医药平台有限公司生产,批号分别为20141001~20141010,编码为S1~S10。
2 方法与结果 2.1 色谱条件色谱柱为Luna C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.05%磷酸水溶液,二元梯度洗脱:0~10 min,15%~20%乙腈;10~20 min,20%~35%乙腈;20~25 min,35%~60%乙腈;25~40 min,60%~70%乙腈;40~50 min,70%~50%乙腈;50~60 min,50%~90%乙腈;60~70 min,90%乙腈;柱温35 ℃,检测波长220 nm,体积流量1 mL/min,进样量20 μL。
2.1.1 溶剂的选择取S3批五味子咀嚼片5片研磨成细粉(过80目筛),精密称取0.25 g,分别用10 mL 90%、70%、50%甲醇,水,90%、70%、50%乙醇7种不同溶剂溶解,滤过,滤液转移置10 mL棕色量瓶中,分别加入相应的溶剂定容至刻度,摇匀,即得供试品溶液。每种溶剂分别进样20 μL,对得到的色谱图进行比较,研究发现,50%甲醇提取效果优于其他溶剂,所得峰数量最多,峰形好,因此选择50%甲醇作为溶剂。
2.1.2 检测波长的选择取同一供试品溶液,按上述洗脱梯度进行检测,比较220、254、286、334 nm检测结果,结果表明,220 nm得到的色谱峰数目较多,色谱峰峰形对称,不拖尾,与其他4个波长相比此波长为最佳检测波长,故选择220 nm作为检测波长。
2.2 溶液的配制 2.2.1 混合对照品溶液的制备精密称取各对照品适量,用甲醇分别溶解并定容至量瓶中,配成单个对照品储备液,分别精密量取各储备液适量,置同一棕色量瓶中,甲醇溶解定容至刻度,配制成含五味子醇甲、五味子醇乙、五味子酯甲、五味子乙素、五味子丙素、丹参素钠、丹酚酸B、隐丹参酮、丹参酮IIA、原儿茶醛、木犀草苷、蒙花苷质量浓度分别为57.0、47.5、36.0、49.6、52.3、47.0、64.0、26.0、110.0、24.0、38.0、62.0 μg/mL的混合对照品溶液,避光低温保存。
2.2.2 供试品溶液的制备取S1~S10批五味子咀嚼片各5片研磨成细粉(过80目筛),精密称取0.25 g,加入50%甲醇约10 mL置锥形瓶中,超声,滤过,滤液转移至10 mL棕色量瓶中,加50%甲醇定容至刻度,摇匀,即得。
吸取“2.2.1”和“2.2.2”项溶液,经0.45 μm微孔滤膜滤过,续滤液即为上样溶液。
2.3 指纹图谱的方法学考察 2.3.1 精密度试验取S3批五味子咀嚼片,按“2.2.2”项方法制备得供试品溶液,连续进样6次,进样量为20 μL,统计并计算所得谱图的相似度均大于0.99,相似度RSD小于0.33%,表明仪器精密度良好。
2.3.2 稳定性试验取S3批五味子咀嚼片按“2.2.2”项制备得供试品溶液,室温放置,分别于0、3、6、9、12、24 h进样,进样量为20 μL,计算所得谱图的相似度均大于0.98,相似度RSD小于1.50%,表明样品稳定性良好。
2.3.3 重复性试验取S3批五味子咀嚼片6份,按“2.2.2”项制备得供试品溶液,按上述条件测定。6份样品所得谱图的相似度大于0.98,相似度RSD小于1.21%,证明此方法重复性良好。
2.4 指纹图谱的建立采用中药指纹图谱相似度软件(2004A版)对10批不同批次的五味子咀嚼片指纹图谱数据进行处理,以S8样品为参照谱图,时间窗宽度为0.50 s,采用多点校正的方法生成指纹图谱。为保证不同批次五味子咀嚼片指纹图谱匹配时校正时间的准确性,选择了主要色谱峰作为校正的Mark峰。10批药材的HPLC-DAD指纹图谱及采用中位数法生成10批不同批次五味子咀嚼片的对照谱图(R),建立HPLC-DAD指纹图谱的共有模式,见图 1-A。
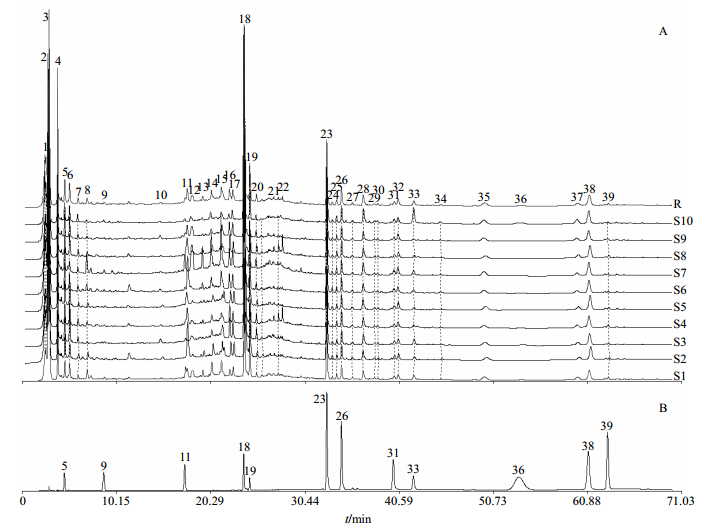 | 5-丹参素钠 9-原儿茶醛 11-木犀草苷 18-丹酚酸B 19-蒙花苷 23-五味子醇甲 26-五味子醇乙 31-五味子酯甲 33-隐丹参酮 36-丹参酮IIA 38-五味子乙素 39-五味子丙素 5-sodium danshensu 9-protocatechuic aldehyde 11-cynaroside 18-salvianolic acid B 19-buddleoside 23-schisandrin 26-schisandrol B 31-schisantherrin A 33-cryptotanshinone 36-tanshinone IIA 38-schisandrin B 39-schisandrin C图 1 10批五味子咀嚼片HPLC-DAD指纹图谱及R (A) 和混合对照品的HPLC-DAD图 (B)Fig. 1 HPLC-DAD fingerprint of 10 batches of SCCT(A) and HPLC of reference substance (B) |
10批五味子咀嚼片经HPLC-DAD分离得到90多个色谱峰,比较测定的色谱峰,获得39个共有峰。共有峰经与对照品比对(图 1-B),保留时间、紫外吸收光谱(DAD检测器给出)均与对照品一致,确定了5号峰为丹参素钠、9号峰为原儿茶醛、11号峰为木犀草苷、18峰为丹酚酸B、19号峰为蒙花苷、23号峰为五味子醇甲、26号峰为五味子醇乙、32号峰为五味子酯甲、33号峰为隐丹参酮、36号峰为丹参酮IIA、38号峰为五味子乙素、39号峰为五味子丙素。23号共有峰(五味子醇甲)峰面积超过总峰面积的7.0%,结构稳定,分离度好,因此选五味子醇甲作为参比峰,计算各共有峰的相对保留时间和相对峰面积,测得10批产品与共有模式间的相似度依次为0.970、0.976、0.973、0.991、0.975、0.976、0.962、0.991、0.986、0.968,相似度均大于0.90,表明10批不同样品具有良好的相似性。
3 讨论采用DAD检测器对同一供试品溶液在220、254、286、334 nm检测波长下色谱进行比较,220 nm(五味子酯甲、五味子乙素、五味子丙素最大吸收波长)波长下色谱峰数量多(59个,最小积分面积4万),分布均匀,峰形对称;254 nm波长下色谱峰数量较少(36个),10、24、25、29、30、34、39(五味子丙素)号色谱峰未积分(小于最小积分面积);286 nm(丹酚酸B最大吸收波长)波长下色谱峰数量较少(34个),24、25、27、28、29、30、31、32(五味子酯甲)、34、35、37、39(五味子丙素)号色谱峰未积分;334 nm(蒙花苷最大吸收波长)波长下,只有前27 min有吸收峰(22个),选择334 nm作为检测波长不具代表性。确定检测波长为220 nm可较好地体现五味子咀嚼片中各味药材的化学成分特征。
五味子、丹参、野菊花阴性样品在五味子醇甲、五味子丙素、丹参酮IIA及木犀草苷的相应位置无色谱峰,其保留时间及紫外光谱与对照品的保留时间及紫外光谱一致。五味子中五味子醇乙、五味子酯甲和五味子乙素,丹参中丹参素钠、原儿茶醛、丹酚酸B和隐丹参酮,野菊花中蒙花苷在阴性样品中相应位置有干扰峰,其保留时间与相应的对照品的保留时间接近,但其紫外光谱与相应的对照品的紫外光谱不一致,故上述物质也能得到确认。丹参和野菊花中均检测出原儿茶醛,故指纹图谱中9号色谱峰来自于丹参和野菊花。茯苓的主要成分为多糖及三萜类化合物,香附的主要成分为挥发油α-香附酮,分别对茯苓和香附水提浸膏进行液相色谱分析,结果表明茯苓和香附中所含色谱峰很少,并且吸光度低,故未能在指纹图谱中识别,已采用薄层色谱对2味药材进行鉴别。
| [1] | 付绍平, 杨 博, 陈 彤, 等. 北五味子的液相色谱指纹图谱的建立 [J]. 色谱, 2008, 26(1): 64-67. |
| [2] | 黎琼红, 张国刚, 徐世义, 等. 丹参药材脂溶性成分的HPLC指纹图谱 [J]. 沈阳药科大学学报, 2006, 23(1): 22-25. |
| [3] | 宋 敏, 杭太俊, 张正行. 丹参水溶性成分HPLC指纹图谱指纹对照品对照法的研究 [J]. 中草药, 2005, 36(3): 360-364. |
| [4] | 林丽美, 李 春, 刘塔斯, 等. 野菊花药材HPLC指纹图谱 [J]. 中国实验方剂学杂志, 2012, 18(22): 120-123. |
| [5] | 刘婷娜, 朱恩圆, 侴桂新, 等. 野菊花高效液相色谱指纹图谱及质量评价方法的建立 [J]. 时珍国医国药, 2009, 20(4): 823-825. |
| [6] | 宋桂萍, 陈国宝, 郑礼娟, 等. 不同产地茯苓饮片的HPLC指纹图谱研究 [J]. 世界中西医结合杂志, 2013, 8(1): 36-38. |
| [7] | 许腊英, 万 芳, 付文强, 等. 不同产地茯苓中萜类成分的HPLC指纹图谱研究 [J]. 湖北中医学院学报, 2007, 9(3): 41-42. |
| [8] | 王 艳, 赵 勇, 郑金凤, 等. 香附挥发油指纹图谱的研究 [J]. 中南药学, 2013, 11(2): 126-128. |
| [9] | 徐 媛, 张文娟, 王庆伟, 等. 香附不同炮制品HPLC指纹图谱研究 [J]. 中国医药导报, 2011, 8(31): 29-32. |
| [10] | 胡建兰, 邵 萌, 余林中. 凉膈散汤剂HPLC-DAD指纹图谱研究 [J]. 中草药, 2014, 45(1): 50-54. |
 2015, Vol. 46
2015, Vol. 46


