醇沉是中药复方制剂最常用的除杂方法之一,从20世纪50年代后期沿用至今,已成为中药生产的“经典”工艺。但是,中药大生产中醇沉工艺还存在一些实际问题。其中,醇沉上清液的实际含醇量是否达到目标含醇量的要求就是一个未引起充分重视的问题。客观上,由于国家药品标准的“制法”项下仅规定加乙醇使含醇量达到多少,但未在《中国药典》“凡例”或其他规范性文件中对该表述的实际内涵进行明确解释。在中成药的研究及大生产中,不同研究者或生产企业按各自对“制法”的理解确定加醇量。为了解中药大生产中醇沉上清液的实际含醇量情况,笔者对22个已上市中成药进行了调研,并以醇沉实际含醇量与目标含醇量之差等为指标进行了分析。
1 调研方法以国内11家中药生产企业规模化生产的22个品种200批次中成药的实际生产数据为研究对象,采用《中国药典》2010年版一部附录IXM乙醇量测定法(包括蒸馏法及气相法),对大生产过程中醇沉静置结束后的上清液的实际含醇量进行了测定。
本次调研收集的信息主要有目标含醇量、表观含醇量、实际含醇量、含醇量差值(ΔC)、确定醇沉加乙醇量的方法等。其中,目标含醇量是指相应中成药质量标准“制法”项下规定的醇沉应达到的含醇量。如“制法”中“醇沉使含醇量达60%”,即目标含醇量为60%;加入等量95%乙醇,即1/(1+1)×95%=47.5%;加入2倍量乙醇,即2/(1+2)×95%=63%。此外,有一个品种的质量标准中规定“醇沉使含醇量达65%~70%”,故以企业《生产操作规程》中规定的66%为目标含醇量。表观含醇量是指酒精计插入醇沉上清液中读取的刻度值。实际含醇量是以《中国药典》2010年版附录的“乙醇含量测定法”对醇沉静置结束后的上清液进行测定所得的含醇量,为醇沉上清液中的实际含醇量。ΔC是指醇沉实际含醇量与目标含醇量之差,ΔC=实际含醇量(Cs)-目标含醇量(Cm)。为了便于对不同目标含醇量的中药进行横向对比,以ΔC为指标进行数据分析。
调研中发现,实际大生产中,醇沉加醇量的确定多采用酒精计法、计算法或倍数法。其中,酒精计法是指在醇沉操作过程中以酒精计插入醇沉上清液时液面达到目标含醇量的刻度作为醇沉加乙醇结束的终点。计算法是在醇沉时根据公式的计算结果来确定醇沉加乙醇量 [目标含醇量×待醇沉药液体积/(0.95-目标含醇量)]。倍数法是根据“制法”的规定,向待醇沉药液中加入一定倍数的乙醇(一般按体积比计)。
2 调研结果 2.1 中药大生产醇沉数据调研的基本情况本次调研共收集了22个品种200批次中成药大生产的醇沉相关信息。22个品种的目标含醇量分别为45%、63%、65%、70%、75%、80%、85%。以酒精计法确定醇沉加醇量的品种,其表观含醇量大多与目标含醇量一致。倍数法的表观含醇量大多低于目标含醇量。从收集的数据看,不同企业大生产的醇沉数据之间存在明显差异,同品种不同批次间的醇沉实际含醇量存在一定差异,不同企业间相同目标含醇量品种的实际醇沉含醇量也存在差异。
2.2 醇沉实际ΔC的总体分布情况从调研的数据可见,200批中药醇沉的ΔC大致呈正态分布,见图 1。中药醇沉的实际含醇量大多高于目标含醇量。低于目标含醇量的品种数量较少,约占品种总数的7.5%。实际含醇量偏离目标含醇量向下最低值为-5.2%,向上最高值为11.6%。实际含醇量高于目标含醇量0~9%的品种数较多。
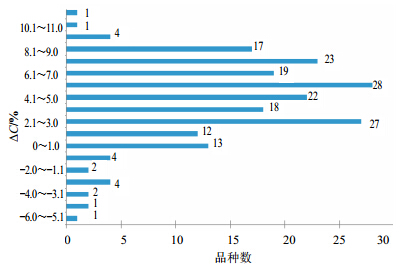 | 图 1 200批中药醇沉的ΔC的分布情况Fig.1 Distribution of ΔC for 200 batches of CMM in alcohol precipitation process |
从表 1可见,(1)中药大生产中的实际醇沉含醇量与质量标准“制法”规定的目标含醇量之间有一定的偏差。ΔC的平均值与品种有关,不同中药品种的ΔC大小不同。ΔC平均值最大达7.9,最小达1.3,总体平均值为4.6。如质量标准中规定目标含醇量为60%,则实际平均含醇量约为64.6%。(2)同品种不同批次之间的醇沉实际ΔC有一定的波动。有的品种实际生产中控制较好,不同批次间ΔC的标准差较小,最小达0.212 13。而有的品种不同批次间的ΔC标准差较大,最大达6.376 38。此外,不同企业之间也表现出一定的差异,如企业E、H、D、K的品种,不同批次ΔC的标准差均相对较小,且极差也较小。推测可能与企业的生产管理与规范操作有关。
| 表 1 不同品种的醇沉ΔC Table 1 ΔC for different batches of products in alcohol precipitation process |
从表 2可见,采用倍数法来确定醇沉加乙醇量的品种,不同批次间ΔC的标准差相对较小。而采用计算法及酒精计法确定醇沉加醇量的品种,不同批次间ΔC的波动相对较大。
| 表 2 不同醇沉加醇量确定方法的ΔC Table 2 ΔC by different ways of real alcohol concentrations in alcohol precipitation process |
一般情况下,按酒精计法或计算法确定醇沉加醇量,其实际醇沉含醇量应高于目标含醇量。但少数样品的实际醇沉含醇量低于目标含醇量。此种情况与理论推测的结果不符。此类品种相对集中,主要在企业B、J、F。根据进一步调查,J企业醇沉时浸膏的温度及室温均较高,加入乙醇后用酒精计测量表观含醇量时的温度约为30 ℃,与20 ℃相比,整体醇沉上清液的相对密度降低,使得酒精计下沉,显示的表观含醇量偏高,加入乙醇量减少。B企业在醇沉时采用计算法,但醇沉前浸膏的体积采用不锈钢桶粗略计量,加入乙醇量按贮槽的液位计估算,且未根据温度对乙醇的体积进行校正。F企业的生产记录资料较少,醇沉实际含醇量出现偏差的原因不明。
2.6 表观含醇量与实际含醇量的关系根据调研的数据,计算了表观含醇量与实际含醇量的相关系数为0.900 19。说明醇沉时的表观含醇量与实际含醇量有一定相关性。
3 讨论 3.1 ΔC对药品质量的影响水提醇沉淀法是以水为溶媒进行提取,浓缩后再加入一定量乙醇以去除提取液中杂质的方法。由于中药所含不同结构类型的成分在水和乙醇中的溶解性不同,通过水和不同浓度的乙醇交替处理,可保留生物碱、苷类、氨基酸、有机酸等成分,去除蛋白质、糊化淀粉、黏液质、油脂、脂溶性色素、树脂、树胶、部分糖类等杂质[1]。醇沉上清液的含醇量对醇沉处理后提取液中能够保留的成分种类及量具有重要影响,是醇沉工艺的关键参数。对于同一种中药而言,当不同批次的醇沉含醇量发生较大差异时,其所含有效成分的损失情况不同,质量也会产生较大差异。
以葛根素为指标,对某中药复方醇沉含醇量对药品质量的影响进行了研究,结果表明,醇沉前浸膏中葛根素转移率为82.51%,醇沉使含醇量分别达到60%、65%、70%、75%、80%时,其葛根素的转移率分别为70.55%、75.09%、72.41%、64.90%、65.82%[2]。补气生血方水提液醇沉的浓度为40%、50%、60%、70%、80%、90%时,在醇沉上清液回收乙醇并定容后的溶液中黄芪甲苷的量分别为0.136 3、0.155 2、0.160 1、0.181 2、0.247 2、0.143 6 mg/mL;多糖的量分别为1.011 1、0.566 7、0.248 1、0.081 1、0.004 07、0.002 963 mg/mL,干浸膏的量分别为0.186 9、0.153 9、0.121 9、0.112 0、0.101 3、0.095 2 g/mL[3]。多糖、干浸膏的量随着醇沉含醇量的提高而逐步下降,而黄芪甲苷的量在80%时最高。常通口服液(含大黄、丹参等)的醇沉含醇量为50%、65%、75%时,丹参素的量分别为1.45、1.54、1.50 mg/mL;大黄素的量分别为19.52、10.55、6.21 mg/mL[4]。健脾止泻颗粒醇沉浓度为40%、50%、60%时,白头翁皂苷B4的转移率分别为78.34%、76.98%、70.42%[5]。华蟾素提取液醇沉含醇量分别为60%、70%、80%、85%时,华蟾素保留率分别为35%、50%、52%、50%[6]。在一定范围内随着终点乙醇量的提高,华蟾素保留率逐渐升高;当终点乙醇量大于80%时,随着终点乙醇量的升高,华蟾素保留率降低。当终点乙醇量过高时,形成的沉淀颗粒粒度增大,容易产生包裹团聚现象,使华蟾素更容易被夹带于形成的块状沉淀中,造成损失。丹参注射剂醇沉实验中丹参素保留率在21%~49%,显示醇沉中丹参素损失明显,加入乙醇的体积分数越高,丹参素损失越多[7]。红花提取液醇沉含醇量为50%、60%、70%、80%、85%时,羟基红花黄色素A转移率分别为98%、100%、92%、83%、79%。终点含醇量在50%~60%,羟基红花黄色素A转移率增加,60%时达到最大值,之后随着乙醇的加入,析出的杂质颗粒粒径增大,包裹药液而造成有效成分的损失,羟基红花黄色素A转移率显著降低[8]。板蓝根水提液的醇沉含醇量为30%、40%、50%、60%、70%时,干浸膏得率分别为93.4%、88.6%、80.1%、72.9%、50.2%。随着醇沉浓度的提高,板蓝根浓缩液喷雾干燥的得粉率明显降低,且黏壁、干法制粒黏轮现象越来越明显[9]。因此,在水提醇沉法进行醇沉含醇量研究时,不但要考虑对成分的影响,必要时还需考察对后续制剂成型的影响。
3.2 ΔC与对目标含醇量的认识差异从本次调研的情况看,调研初期,接受调研的企业均认为其产品的生产严格按质量标准规定的“制法”进行,虽然平时生产中并未对醇沉上清液的实际含醇量进行测定,但认为醇沉的含醇量应符合要求。但从醇沉操作的具体细节和SOP中却反映出不同企业对“制法”中醇沉含醇量的理解存在较大差异,即对于目标含醇量的理解存有分歧。对于“制法”中相同表述的醇沉目标含醇量,不同企业按各自理解的不同“目标含醇量”进行操作。醇沉实际含醇量的测定结果显示,大部分企业生产品种的醇沉实际含醇量与目标含醇量之间确有一定差距,且同品种不同批次之间也存在一定偏差。如2个企业生产的某品种执行相同的国家标准(制法同为浸膏浓缩至相对密度为1.2,加乙醇使含醇量达到60%),但其中一家企业用计算法醇沉,样品平均实际含醇量为69%,而另一家企业用酒精计法醇沉,样品平均实际含醇量为57.7%。由此推测,对于质量标准“制法”项下的醇沉目标含醇量的理解不同是导致醇沉含醇量差异的重要原因。
3.3 ΔC与醇沉加醇量的确定方法在中药实际生产中,醇沉加醇量的确定方法主要有酒精计法、计算法、倍数法等。酒精计法是根据水与乙醇不同比例混合物的相对密度不同的原理制成的,而中药醇沉上清液中由于溶解了一定量的药物,其相对密度比相应的水醇混合物高,酒精计显示的刻度值会因此而偏低,需多加乙醇才能使酒精计的表观含醇量与目标含醇量一致,这样最终上清液的含醇量就会高于目标含醇量。计算法目前较普遍使用的公式仅适用于水与乙醇的混合溶液,并不适用于中药醇沉时的非均相体系,由于醇沉时有较多沉淀物产生,醇沉上清液的体积明显小于浸膏与加入乙醇的体积之和,故计算法所得的加乙醇量理论值高于达到目标含醇量所需的乙醇量,最终使得上清液的实际含醇量高于目标含醇量。倍数法为计算法的一种特例,同样因醇沉沉淀物的产生而使实际上清液的含醇量高于目标含醇量(质量标准中未规定倍数法的目标含醇量,此处的目标含醇量为计算的理论值)。
3.4 缩小ΔC的方法建议研究明确醇沉加醇量的方法,采用适当的在线控制指标来预测醇沉含醇量,尽可能缩小实际含醇量与目标含醇量之间的差距。如用酒精计测量醇沉药液离心后上清液的表观含醇量,或测量其折光率、电导率等指标,或以浸膏含水量代替浸膏体积对醇沉加醇量的计算公式进行校正,并分析这些数据与醇沉静置后的实际含醇量之间的关联,选择其中关联较好且稳定的指标作为醇沉在线控制的指标,以此确定醇沉加醇量。当然,上述方法或指标需结合品种的具体情况,经反复研究验证后,才能缩小实际醇沉含醇量与目标含醇量之间的差距。此外,林冬杰等[10]以近红外的方法测定藿香正气水中的含醇量,用时约10 min,可尝试用该方法测定醇沉时的含醇量,以此作为在线控制的指标,保证实际含醇量的稳定。
4 结语与建议本次调研结果显示,中药复方醇沉的实际含醇量普遍高于质量标准规定的目标含醇量。同品种不同批次的醇沉含醇量也存在一定差异。ΔC可能与具体品种、企业的实际操作情况、醇沉加醇量的确定方法等有关。
建议在《中国药典》“凡例”中,明确解释中药质量标准“制法”项下目标含醇量的内涵。统一生产企业对于醇沉目标含醇量的认识[11]。
在中药新药的醇沉工艺研究中,应对醇沉工艺进行系统研究。建议以有效成分或指标成分的量、指纹图谱峰面积及醇沉上清液中固含物量等为指标,确定合适的目标含醇量及其允许波动的范围。应研究明确醇沉操作的详细方法和参数,明确醇沉加醇量的确定方法;明确醇沉工序在线控制的方法、指标及要求,并提供醇沉加醇量的确定方法及在线控制指标与醇沉上清液实际含醇量之间关系的研究资料。在工艺验证研究中,应以醇沉上清液的实际含醇量(以《中国药典》2010年版附录IXM乙醇量测定法测定)为指标验证醇沉加醇量的确定方法能否使醇沉实际含醇量达到预期目标。
建议将中药新药质量标准“制法”中醇沉含醇量的表述由“醇沉使含醇量为60%”改为“醇沉使上清液的含醇量为60%”。此处“含醇量为60%”的含义可解释为醇沉静置达到规定时间后上清液的实际乙醇量为(60±2)%(以《中国药典》2010年版附录IXM乙醇量测定法测定)。含醇量允许波动的范围可根据醇沉含醇量对具体品种质量的影响程度而定。
建议在中药新药的“生产现场检查用生产工艺”中,详细描述醇沉方法、参数及质控要求等。明确醇沉加醇量的确定方法,明确醇沉工序进行在线控制的方法、指标及要求;明确待醇沉浸膏的相对密度(测定温度)、体积的测量方法及要求;乙醇的浓度、体积、相对密度的测定方法及要求;对醇沉所用乙醇的含醇量、体积进行校正的方法;醇沉时加入乙醇的方法及速度;搅拌的类型、方法、参数、静置时间、温度等。以保证不同批次中药质量的稳定均一。
已上市中药醇沉加醇量的方法应与相应品种研发时采用的方法保持一致,以保证上市中药的药用物质基础与临床试验用样品一致。
由于种种原因,本次调研收集的信息不够全面,且收集的数据偏少,尚难以对中药醇沉实际含醇量的偏差进行全面、准确的分析。调研结果仅供参考。
| [1] | 张兆旺. 中药药剂学[M]. 第2版. 北京: 中国中医药出版社,2007. |
| [2] | 阎雪梅,李凤丽,宋洁瑾. 暑热宁合剂水提醇沉工艺研究[J]. 中国现代应用药学,2012,29(8): 702-704. |
| [3] | 张华. 醇沉浓度对补气生血口服液所含成分的影响[J]. 中成药,2006,28(8): 1204-1207. |
| [4] | 曾煦欣,杨西晓,王春霞,等. 常通口服液制备工艺研究[J]. 中国药房,2007,36 (18): 2822-2825. |
| [5] | 陈凌云,方波,陈兆蕊,等. 健脾止泻颗粒水提醇沉工艺研究[J]. 云南中医学院学报,2010,33(1): 38-40. |
| [6] | 胡晓雁,李页瑞,袁佳. 多指标综合评分法优选华蟾素提取液醇沉工艺的研究[J]. 时珍国医国药,2012,23(4): 1016-1019. |
| [7] | 龚行楚,严斌俊,瞿海斌. 丹参1次醇沉中3个重要工艺参数的相关性研究[J]. 中国中药杂志,2010,35(24): 3274-3277. |
| [8] | 袁佳,李页瑞,陈勇,等. 多指标综合评分法优选红花提取液醇沉工艺[J]. 浙江大学学报: 医学版,2011,40(1): 27-32. |
| [9] | 何雁,辛洪亮,黄恺,等. 水提醇沉法中醇沉浓度对板蓝根泡腾片制备过程的影响[J]. 中国中药杂志,2010,35(3): 288-292. |
| [10] | 林冬杰,陈学松,刘慧妍,等. 近红外光谱法测定藿香正气水中乙醇含量[J]. 中国药师,2012,15(3): 330-332. |
| [11] | 杜松,罗爱勤,刘美凤. 中药浸膏醇沉工艺中醇浓度概念与计算方法辨析[J]. 中草药,2012,43(8): 1652-1655. |
 2015, Vol. 46
2015, Vol. 46

