2. 太原天中益耀科技有限公司, 山西 太原 030006
2. Taiyuan Tian-Zhong-Yi-Yao Science and Technology Co., Ltd., Taiyuan 030006, China
抑郁症是一种常见的心境障碍,其核心症状为情绪低落、思维迟缓、意志活动减退,更有甚者出现睡眠障碍、自杀倾向等现象[1, 2, 3, 4]。心理学者认为,胃肠道症状是抑郁症的一种躯体化表现,即抑郁可能通过中枢神经系统与肠神经系统之间相互作用等多途径影响肠道运动、分泌、内脏感受等功能[5]。大量研究证实,应激、焦虑和抑郁与肠易激综合征(irritable bowel syndrome,IBS)密切相关,抗抑郁药物在治疗IBS中的作用已引起广泛关注[6]。本实验室前期对逍遥散干预慢性温和不可预知应激(CUMS)抑郁模型大鼠的盲肠菌群进行了大量研究,表明盲肠是抑郁症发生过程中的重要防御器官,具有扶植正常菌群生长和调整菌群失调的作用[7],为此本实验进一步研究盲肠组织化学成分的变化,探究抑郁症与盲肠组织的关系。
逍遥散出自《太平惠民和剂局方》,由柴胡、当归、白芍、白术、茯苓、生姜、薄荷和甘草共8味药组成,是疏肝解郁、调和肝脾的代表方剂,临床及实验研究均显示该方有确切的抗抑郁作用[8, 9, 10]。代谢组学是近年来生命科学领域研究的一大热点,它通过研究生物体对环境等因素产生的代谢物的质和量的动态变化,从整体角度评价生物体代谢状态的波动,从而更深刻地理解生命过程[11]。
GC-MS具有灵敏度高、分离效率高、分析时间短和同时提供样品的相对分子质量与结构信息等优点[12]。本研究采用GC-MS方法和代谢组学技术从代谢物组的角度分析逍遥散干预CUMS抑郁大鼠盲肠组织化学成分的变化,为抑郁症发病机制及逍遥散抗抑郁的作用机制研究提供依据。
1 材料 1.1 动物成年雄性SD大鼠,体质量(180±20)g,24只,购自中国食品药品检定研究院实验动物中心,许可证编号SCXK(京)2011-0008。置于昼夜节律光照下,自由禁食禁水3 d,采用旷场实验对大鼠行为学评分,并称体质量。
1.2 药品与试剂中药材饮片:北柴胡、当归、白芍、白术、茯苓、甘草、生姜和薄荷,购自山西华阳药业有限公司,经山西大学中医药现代研究中心秦雪梅教授鉴定均为正品。盐酸氟西汀(氟西汀,Eli Lilly & Company Limited,英国,批号A342299,购自山西黄河大药房);N-甲基-N-(三甲基硅烷) 三氟乙酰胺(MSTFA)、1%三甲基氯硅烷(TMCS)(Sigma- Aldrich公司,美国);二十四烷(上海索莱宝生物有限公司);吡啶、甲氧胺盐酸盐、正庚烷、甲醇、氯仿、甲苯(分析纯,北京化工试剂公司);丙氨酸、甘氨酸、谷氨酸、天冬氨酸、丝氨酸、酪氨酸、葡萄糖(中国食品药品检定研究院)。
1.3 仪器代谢笼(苏州实验动物笼具厂);YSD-4药理生理实验多用仪(蚌埠医学院无线电二厂);LD500-1电子天平(沈阳龙腾电子有限公司);101系列恒温干燥箱(北京和同创业科技有限责任公司);KQ2200DB型数控超声仪(昆山超声仪器有限公司);Trace GC-PolarisQ MS气相色谱-质谱联用仪(Thermo Finnigan公司,美国);TGL-16高速台式冷冻离心机(湘仪离心机有限公司)。
2 方法 2.1 溶液的配制逍遥散按照处方量配比(北柴胡、当归、白芍、白术、茯苓、甘草、薄荷、生姜质量比6∶6∶6∶6∶6∶3∶2∶2)称取药材适量,加入10倍量蒸馏水浸泡2 h,水煎提取2 h,收集水煎液,再用8倍体积水提取2次,每次1 h。合并3次水煎液,减压浓缩至稠浸膏[含藁本内酯(40.25±0.94)mg/g、白术内酯I(1.96±0.85)mg/g,白术内酯II(6.22±2.11)mg/g],干燥,磨成干粉,4 ℃保存,用时新配。
二十四烷-正庚烷溶液:精密称取二十四烷100 mg置于100 mL量瓶中,正庚烷稀释至刻度;精密移取上述溶液10 mL置于100 mL量瓶中,正庚烷稀释至刻度,即得质量浓度为0.1 mg/mL的内标溶液。
盐酸甲氧胺-吡啶溶液:精密称取盐酸甲氧胺适量,用吡啶稀释至质量浓度为15 mg/mL,即得。
2.2 分组与给药依据行为学评分和体质量,将大鼠随机分为4组:对照组、模型组、氟西汀(6 mg/kg)组和逍遥散(生药46.2 g/kg [13])组。给药组均ig给药,给药体积均为10 mL/kg,对照组和模型组大鼠ig给予等量生理盐水,每天1次,连续给药28 d,造模同时给药。
2.3 CUMS抑郁模型复制按照Li等[14]的方法复制CUMS抑郁模型。10种刺激因子随机安排:(1)潮湿垫料、45°倾斜;(2)禁食24 h;(3)禁水24 h;(4)50 ℃环境5 min;(5)夹尾1 min;(6)4 ℃冰水游泳5 min;(7)电击,电压50 mV,每隔30 s刺激1次,每次10 s,共15次;(8)束缚4 h;(9)接触陌生物体(如塑料杯、木勺等);(10)噪音(60 Hz)1 h。每天给予1种刺激,同种刺激不连续出现,造模21 d,恢复7 d。对照组大鼠群养,不给予刺激;其他各组大鼠单笼饲养,并给予刺激。饲养条件:温度(24±1)℃,湿度30%~60%,昼夜节律12 h/12 h,标准实验室饲料喂养,自由饮水。
2.4 样品的采集与处理实验第29天,称大鼠体质量,ip 20%乌拉坦(1.5 g/kg)麻醉,解剖盲肠,低温生理盐水洗涤,称质量,再用无RNase水冲洗至肉眼看不见残留物,液氮速冻,-80 ℃保存。
2.5 GC-MS代谢组学数据采集 2.5.1 样品制备精密称取盲肠组织样品20 mg,加入280 μL氯仿-甲醇-水溶液(8∶5∶15),冰浴超声10 min;1.0×104 r/min离心3 min,移取上清液120 μL,30 ℃真空干燥12 h;加入12 μL盐酸甲氧胺-吡啶溶液,70 ℃反应1 h,再加入20 μL MSTFA(含1% TMCS),40 ℃孵育90 min,最后加入200 μL二十四烷-正庚烷内标溶液,涡旋。
2.5.2 GC-MS条件色谱条件:DB-5MS毛细管柱(5%苯基-95%聚二甲基硅氧烷交联,30 m×250 μm,0.25 μm;Agilent J&W Scientific,Folsom,美国);进样口温度260 ℃,无分流模式进样,进样量1 μL,起始温度60 ℃,保持3 min,以7 ℃/min升至140 ℃,保持4 min,以5 ℃/min升至180 ℃,保持6 min,再以5 ℃/min升至280 ℃,保持2 min。质谱条件:EI离子源,离子源温度200 ℃,电子能量70 eV,扫描范围m/z 50~650。
2.6 多元统计分析使用XCMS软件(http://metlin.scripps.edu/ download)对GC-MS图谱预处理后,将数据导入Excel中进行归一化,导入SIMCA-P 13.0进行主成分分析,采用NIST 05质谱库检索、对照品比对、文献参考、HMDB数据库(http://www.hmdb.ca/)比对等方法对生物标志物进行结构指认。
3 结果 3.1 各组大鼠盲肠总离子流色谱图对照组、模型组与给药组大鼠盲肠组织GC-MS总离子流色谱图见图 1。由图 1可知,总离子流色谱图基本相似,色谱峰保留时间(tR)主要集中在5~45 min,但也有一定区别,如tR为5~7 min的2个主要峰在模型组中的峰高明显低于对照组;tR为37~38 min的峰在模型组中峰高也比较低;tR为6.35 min的峰在氟西汀组中的峰高明显高于逍遥散组;tR为37和41 min左右的2个峰在逍遥散组中也比较低。各色谱峰具体指认结果见表 1。
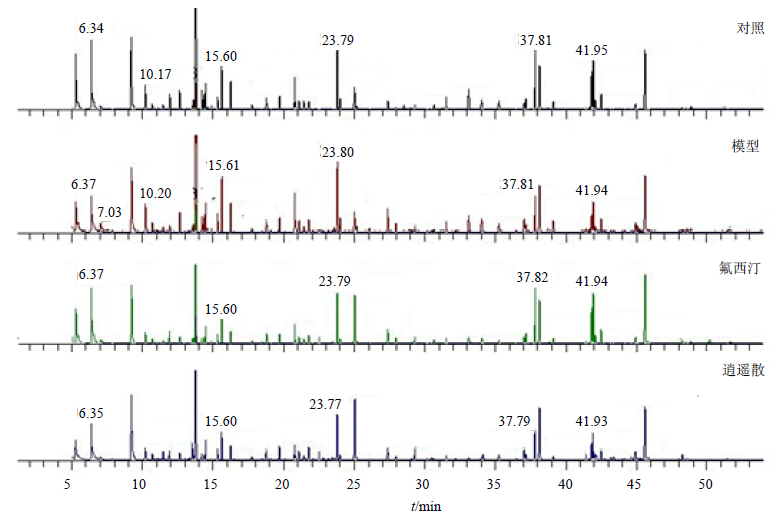 | 图 1 对照组、模型组、逍遥散组、氟西汀组大鼠盲肠组织GC-MS总离子流色谱图Fig.1 GC-MS total ion chromatograms of cecal tissue of rats in control,model,fluoxetine,andXiaoyaoSan groups |
| 表 1 指认的大鼠盲肠组织化学成分 Table 1Endogenous metabolites of cecal tissue in rats |
采用PCA方法对所有样本的GC-MS数据进行分析,结果见图 2。可知,对照组和模型组沿t[1]轴分开,表明CUMS模型复制成功。给药组与对照组、模型组距离均较远,说明药物在代谢过程中对盲肠组织化学成分的影响比较显著。
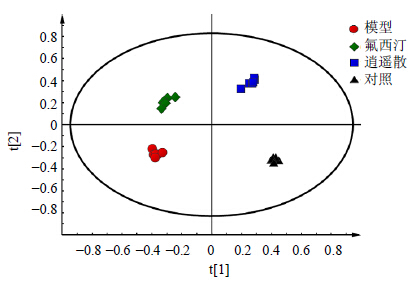 | 图 2 大鼠盲肠组织GC-MS谱PCA分析散点图Fig.2 GC-MS spectrum PCA scores plots of cecal tissue of rats |
为了找出发生显著变化(P<0.05)的生物标志物,对模型组与对照组及模型组与各给药组进行OPLS-DA分析,并得到代谢物载荷图,结果见图 3~图 5。由图 3可知,对照组和模型组能够很好地分开,说明两组之间盲肠组织的化学成分发生明显改变。由图 4可知,逍遥散组与模型组明显分开;由图 5可知,氟西汀组和模型组明显分开,说明盲肠组织的代谢物发生改变。
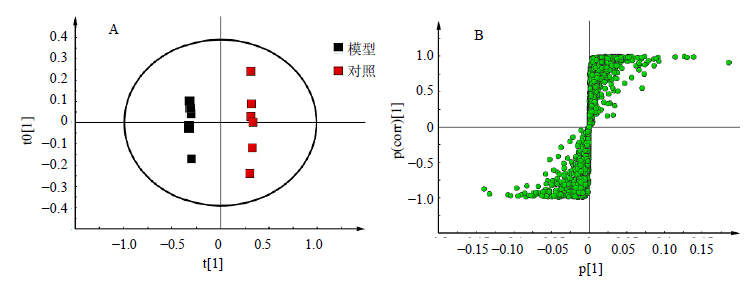 | 图 3 对照组和模型组大鼠盲肠组织的OPLS-DA图 (A) 和S-plot图 (B)Fig.3 OPLS-DA scores plot (A) and loading S-plot (B) of cecal tissue of rats in control and model groups |
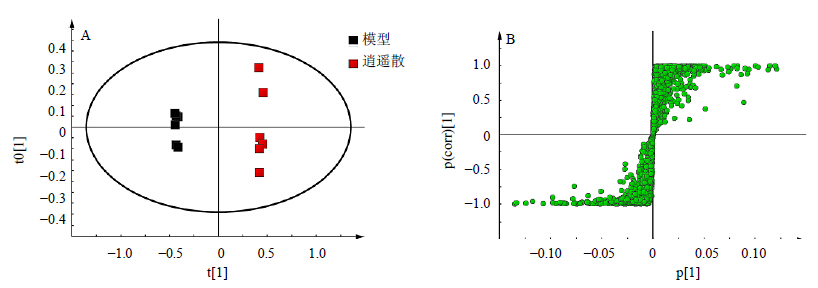 | 图 4 逍遥散组和模型组大鼠盲肠组织的OPLS-DA图 (A) 和S-plot图 (B)Fig.4 OPLS-DAscoresplot(A) and loading S-plot (B) of cecal tissue of rats in Xiaoyao San and model groups |
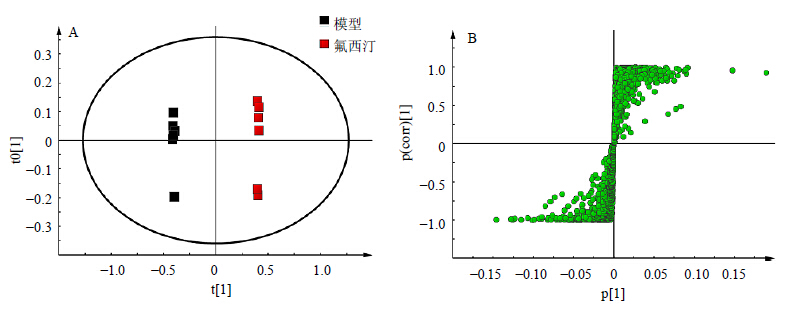 | 图 5 氟西汀组和模型组的OPLS-DA图 (A) 和S-plot图 (B)Fig.5 OPLS-DA scores plot (A) and loading S-plot (B) of cecal tissue of rats in fluoxetine hydrochloride and model groups |
依据载荷图中,离原点最远的点对分组贡献最大的原则,同时采用SPSS 18.0软件对位于载荷图中边缘位置代谢物的峰面积进行独立样本t检验,峰面积具有显著性差异的潜在生物标志物结果见表 2。在造模过程中,大鼠被给予各种刺激,使其处于抑郁状态,对盲肠组织造成影响。通过寻找有明显差异的化学成分,即生物标志物,能够说明逍遥散对盲肠组织化学成分的影响主要表现在丙氨酸、丝氨酸、棕榈酸、谷氨酸、硬脂酸的变化。
| 表 2 特征代谢物组相对峰面积比较 Table 2Comparison on typical compounds based on mean peak areas after internal standard normalization |
现代药理学研究表明,抑郁症的诱发可能与单胺类神经递质去甲肾上腺素(NE)、5-羟色胺(5-HT)等不足有关[15]。李熠萌等[16]研究表明,逍遥散对心理社会因素所致的应激性机体功能失调具有较好的调节作用,能改善慢性应激大鼠的行为学变化,对代谢终产物有明显的调节效应。石君杰等[17]研究发现逍遥散能降低结肠黏膜5-HT的表达,推测逍遥散的作用机制可能是通过调节模型大鼠5-HT信号系统,减弱脊髓背角神经元兴奋性,从而提高内脏痛阈,消除肠道的过敏反应。
代谢组学的研究方法与中医治疗疾病的整体观念是相一致的,对认识中药的药效作用,在治病中的正确用药都有重要意义,也为疾病的研究开拓了全新的方法[18, 19]。因此,应用代谢组学技术评价传统中药复方的药理活性具有先进性和合理性。研究表明代谢组学技术的多元统计分析(PCA、PLS-DA、OPLS-DA)指标灵敏性较传统方法明显提高[20],许多动物行为学、形态学,甚至有限的生化指标不能显示差异时,通过代谢组学方法不仅可以有效分类,而且可寻找到与分类有关的一组特征性标志物。
本研究从组织化学成分的角度采用GC-MS方法比较了CUMS抑郁模型及药物干预后大鼠盲肠组织化学成分的变化,发现CUMS能够引起大鼠盲肠组织化学成分的显著改变。采用盲肠组织样本作为研究对象,能够直接反映细胞的代谢轮廓。CUMS抑郁模型大鼠的盲肠组织中含有各类小分子代谢物,包括氨基酸、脂肪酸、有机酸、糖类等,且部分在量上与对照组有明显差异,这些物质参与了多种生理生化过程,特别是细胞的能量代谢和脂质代谢[21]。其中,与对照组相比,模型组大鼠盲肠组织中的棕榈酸、硬脂酸的量显著降低,而棕榈酸、硬脂酸是机体提供能量的主要来源,提示CUMS抑郁模型大鼠盲肠组织的能量代谢加强。
药物干预对CUMS大鼠盲肠组织的化学成分存在较大影响。其中,棕榈酸、硬脂酸的变化趋势与CUMS所引起的变化趋势并不相同,是否由于药物在体内代谢过程中与盲肠组织有直接接触,造成其所产生的影响比CUMS产生的间接影响更为显著,均需要进一步深入探索。
| [1] | 郭雨欣, 邢国刚. 抑郁症的生物学机制研究进展 [J]. 中国神经精神疾病杂志, 2012, 38(1): 57-60. |
| [2] | 李金兵, 李翼鹏, 田俊生, 等. 基于慢性温和不可预知应激模型内源性代谢物变化探讨抑郁症病理机制 [J]. 中草药, 2013, 44(1): 108-115. |
| [3] | 薛水玉, 郑兴宇, 窦春艳, 等. 文拉法辛和氟西汀抗抑郁作用机制和药效特点的代谢组学研究 [J]. 中国药学杂志, 2012, 47(1): 29-33. |
| [4] | 郑兴宇, 高晓霞, 刘晓节, 等. 基于代谢组学技术应激抑郁动物模型的评价 [J]. 药物评价研究, 2010, 33(3): 175-179. |
| [5] | O'Malley D, Julio-Pieper M, Gibney S M, et al. Distinct alterations in colonic morphology and physiology in two rat models of enhanced stress-induced anxiety and depression-like bahaviour [J]. Stress, 2010, 13(2): 114-122. |
| [6] | 杨金选, 曹德勇. 抗抑郁药物对肠易激综合征患者治疗效果与肠道敏感性的影响 [J]. 成都医学院学报, 2012, 7(2): 243-244. |
| [7] | 刘伟. 逍遥散干预慢性温和性不可预知应激大鼠盲肠菌群及组织研究 [D]. 太原: 山西大学, 2011. |
| [8] | 阎兆君, 彭伟. 难病奇方系列丛书——逍遥散 [M]. 北京: 中国中医药出版社, 2005. |
| [9] | 杨杰, 黄丹雪, 鹿秀梅, 等. 小柴胡汤化学成分及其在抑郁模型大鼠体内代谢成分的分析 [J]. 中草药, 2012, 43(9): 1691-1698. |
| [10] | 吴红彦, 王虎平. 逍遥散及其拆方对老年性痴呆模型小鼠学习记忆能力及抗氧化能力的影响 [J]. 中国实验方剂学杂志, 2009, 15(10): 102-104. |
| [11] | Hatzinger M. Neuropeptides and the hypothalamic- pituitary-adrenocortical (HPA) system: review of recent research strategies in depression [J]. World J Biol Psychiatry, 2000(1): 105-110. |
| [12] | 孙皓, 刘薇, 曾建国, 等. GC-MS分析不同产地香荚兰商品荚乙醇提取物化学成分差异及其香草醛的测定 [J]. 中草药, 2013, 44(8): 955-959. |
| [13] | 崔杰, 郑兴宇, 高晓霞, 等. 逍遥散抗抑郁作用最佳剂量筛选 [J]. 中国实验方剂学杂志, 2010, 16(13): 194-198. |
| [14] | Li Z Y, Zheng X Y, Gao X X, et al. Study of plasma metabolic profiling and biomarkers of chronic unpredictable mild stress rats based on gas chromatography/mass spectrometry [J]. Rapid Commun Mass Spectrom, 2010, 24: 3539-3546. |
| [15] | 黄佩珊. 柴胡疏肝散联合抗抑郁药物治疗抑郁障碍的研究进展 [J]. 中医学报, 2012, 27(168): 627-629. |
| [16] | 李熠萌, 蔡淦. 腹泻型肠易激综合征的中医实验研究进展 [J]. 世界科学技术—中医药现代化, 2009, 11(4): 541- 544. |
| [17] | 石君杰, 王海云, 宋李亚, 等. 逍遥散对肠易激综合征大鼠5-羟色胺及5-羟色胺转运体作用研究 [J]. 浙江中医杂志, 2012, 47(7): 490-491. |
| [18] | Rochfort S. Metabolomics reviewed: a new "omics" platform technology for systems biology and implications for natural products research [J]. J Nat Prod, 2005, 68(12): 1813-1820. |
| [19] | 谷金宁, 牛俊, 皮子风, 等. 尿液代谢组学方法研究人参总皂苷治疗糖尿病心肌病大鼠作用机制 [J]. 分析化学研究报告, 2013, 3(41): 371-376. |
| [20] | Par J, Hans S, Thomas M, et al. A strategy for modeling dynamic responses in metabolic samples characterized by GC/MS [J]. Metabolomics, 2006, 2(3): 135-143. |
| [21] | Liu P, Liu S L, Tian D Z, et al. The applications and obstacles of metabonomics in traditional Chinese medicine [J]. Evid-Based Compl Alt, 2012, 1155(10): 1-4. |
 2015, Vol. 46
2015, Vol. 46


