栀子Gardeniae Fructus为茜草科(Rubiaceae)植物栀子Gardenia jasminoides Eills的干燥成熟果实,《中国药典》2010年版收载的有生栀子、炒栀子和焦栀子[1]。栀子是临床常用中药,有泻火除烦、清热利尿、凉血解毒之功效,现代药理研究表明栀子具有抗炎、镇静、镇痛、保肝利胆、抗凝血等作用。已知的主要有效成分为有机酸、环烯醚萜苷和色素。其中有机酸以绿原酸等为代表,环稀醚萜苷 以栀子苷、京尼平龙胆二糖苷、去乙酰车叶草酸甲酯、京尼平苷酸等为代表,色素以西红花苷I和西红花苷II等为代表。但其味苦,性大寒,易损伤脾胃,自古以来即很重视对其的炮制处理[2]。栀子常见炮制法为药典法[1]、章帮法[3]和建昌帮法[4],各种炮制法仅从栀子果实选用部位就存在差异,药典法是对全果炮制、章帮法是弃皮留仁炮制,建昌帮法中还有对栀子果皮单独炮制。虽已有报道关于栀子果皮、果仁成分差异和栀子炮制研究[5],但选用的指标成分较少,也缺乏系统性。
通过对22批栀子类药材中10种主要有效成分研究,发现虽然不同产地批次栀子有效成分的量存在差异,但栀子中栀子苷、京尼平龙胆二糖苷、去乙酰车叶草酸甲酯、西红花苷I、西红花苷II等的量稳定[6];京尼平苷酸是栀子中环烯醚萜类代表成分之一,绿原酸是栀子有机酸中最具有代表性成分之一,具有显著的抗炎活性。为了更好地阐明栀子果仁、果皮分开药用的物质基础和栀子炮制的机制,也为制定栀子炮制规范提供依据,本实验利用HPLC-DAD对栀子全果、果仁、果皮及各自炮制品中绿原酸、栀子苷、京尼平龙胆二糖苷、去乙酰车叶草酸甲酯、京尼平苷酸、西红花苷I、西红花苷II 7种成分的量进行测定比较分析。
1 仪器与材料Agilent1260,美国Agilent公司,包括G1311C四元梯度泵、G1329B自动进样器、G1316A柱温箱、G4212B二极管阵列检测器;BP224S型万分之一电子天平,Sartorius公司;KQ-300E超声波清洗器,昆山超声仪器有限公司;永历111B中药粉碎机;CCFG-160型电炒锅,广东湛江家用电器工业公司。
京尼平苷酸(批号111828-201102,质量分数96.0%)、栀子苷(批号110749-201316,质量分数97.5%)、去乙酰车叶草酸甲酯(批号111786-200801,质量分数99.9%)、绿原酸(批号110753-201314,质量分数96.6%)、西红花苷I(批号111588-201202,质量分数91.1%)、西红花苷II(批号111589-201304,质量分数92.4%),以上对照品均购自中国食品药品检定研究院;京尼平龙胆双糖苷(HPLC测定质量分数>98%,批号ZM0501BA14),购自上海源叶生物科技有限公司;进口色谱纯乙腈(ACS);甲醇、磷酸为分析纯;水为娃哈哈纯净水。
栀子生品由汇仁集团提供,批号为20140601,经江西中医药大学药学院葛菲教授鉴定为栀子Gardenia jasminoides Ellis的干燥成熟果实。栀子各种炮制品(栀子全果炒黄、炒焦,栀子果仁炒黄、炒焦,栀子果皮炒黄、炒焦)由同一批生栀子炮制8批,在江西中医药大学药学院钟凌云教授指导下完成炮制。
2 方法与结果 2.1 供试品溶液的制备取栀子各种生品及其炮制品粉末约0.20 g(过4号筛),精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,称定质量,超声处理40 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,即得。
2.2 对照品溶液的制备分别精密称取京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆双糖苷、栀子苷、绿原酸、西红花苷I、西红花苷II对照品适量,加50%甲醇溶解制成质量浓度分别43.00、25.63、154.56、1 249.00、27.60、145.50、51.90 μg/mL的混合对照品溶液,取适量混合对照品溶液分别稀释2、4、8、16、32倍,待用。
2.3 色谱条件[7]色谱柱为Venusil MPC18柱(250 mm×4.6 mm,5 μm);流动相为0.1%磷酸水溶液-乙腈,梯度洗脱:0~18 min,8%~15%乙腈;18~25 min,15%~23%乙腈;25~40 min,23%~35%乙腈;40~55 min,35%~65%乙腈;柱温20 ℃;体积流量0.8 mL/min;检测波长为240、330、440 nm;进样量为10 μL。色谱见图 1。
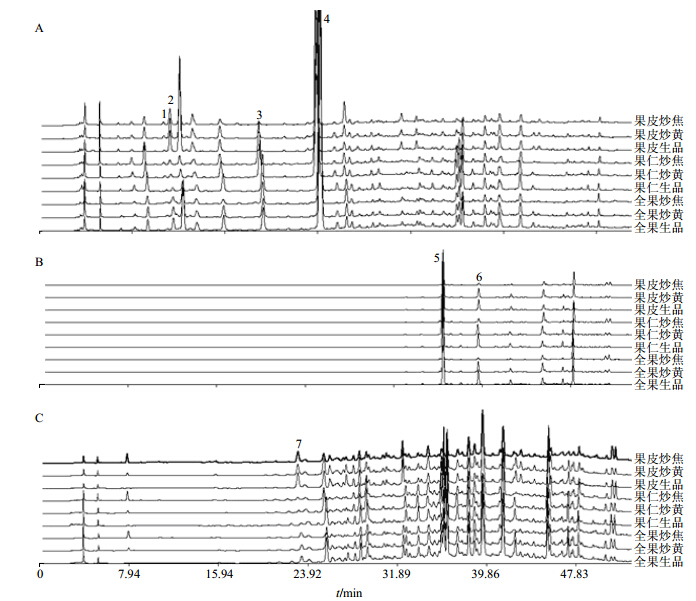 | 1-京尼平苷酸 2-去乙酰车叶草酸甲酯 3-京尼平龙胆二糖苷 4-栀子苷 5-西红花苷I 6-西红花苷II 7-绿原酸 1-geniposidic acid 2-deacetyl asperulosidic acid methyl ester 3-genipin-1-β-D-gentiobioside 4-gardenoside 5-crocin-I 6-crocin-II 7-chlorogenic acid 图 1 栀子生品及其不同炮制品在检测波长240 nm (A)、440nm (B) 和330 nm (C) 下的HPLC-DAD色谱图Fig.1 HPLC-DAD chromatograms of Gardeniae Fructus by different processing methods at detection wavelength of 240 (A),440 (B),and 330 (C)nm |
将“2.2”项中稀释不同倍数的混合对照品溶液,按“2.3”项下的色谱条件进行测定,进样量10 μL。以峰面积积分值为纵坐标(Y),进样质量浓度为横坐标(X),绘制标准曲线,进行线性回归,得回归方程分别为京尼平苷酸:Y=16 936.4 X+0.55,r=0.999 91,线性范围1.34~43.00 μg/mL;去乙酰车叶草酸甲酯:Y=15 464.7 X-1.18,r=0.999 99,线性范围0.80~25.63 μg/mL;京尼平龙胆二糖苷:Y=87 772.2 X+15.1,r=0.999 90,线性范围4.83~154.56 μg/mL;栀子苷:Y=13 032.6 X+57.0,r=0.999 92,线性范围39.03~1 249.00 μg/mL;绿原酸:Y=24 543.2 X+17.8,r=0.999 14,线性范围0.86~27.60 μg/mL;西红花苷I:Y=53 426.4 X+71.0,r=0.999 51,线性范围 4.55~145.50 μg/mL;西红花苷II:Y=31 275.0 X-1.4,r=0.999 93,线性范围1.62~51.90 μg/mL;结果表明各成分在相应的范围内,进样质量浓度与峰面积线性关系良好。
2.4.2 精密度试验取“2.2”项中混合对照品2倍稀释液,按“2.3”项下的色谱条件,连续进样6次,每次10 μL,测定得各峰面积的RSD分别为0.47%、0.83%、0.15%、0.12%、0.54%、0.26%、0.32%,符合规定,说明仪器精密度良好。
2.4.3 重复性试验取栀子生品(汇仁集团,批号20140601)粉末约0.2 g,精密称定6份,按“2.1”项中制备供试品溶液,以“2.3”项下的色谱条件分别进行测定,测得样品中京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆二糖苷、栀子苷、绿原酸、西红花苷I、西红花苷II的平均质量分数的RSD分别为1.73%、1.39%、1.40%、0.81%、1.10%、1.18%、1.38%,表明该方法重复性良好。
2.4.4 稳定性试验精密吸取同一供试品溶液,按“2.3”项下的色谱条件分别在0、2、4、6、8、12、24 h进样测定,测得样品中京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆二糖苷、栀子苷、绿原酸、西红花苷I、西红花苷II平均质量分数的RSD分别为0.55%、0.22%、0.42%、0.15%、0.99%、0.20%、0.64%,结果表明供试品溶液在24 h内稳定。
2.4.5 加样回收率试验取栀子生品粉末约0.2 g,精密称定,共6份,分别加入一定量的京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆二糖苷、栀子苷、绿原酸、西红花苷I、西红花苷II对照品,按“2.1”项中方法制备供试品溶液,以“2.3”项下的色谱条件分别进行测定,计算加样回收率,结果京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆二糖苷、栀子苷、绿原酸、西红花苷I、西红花苷II的平均回收率分别为98.38%、99.05%、97.95%、98.78%、97.16%、98.20%、98.35%,RSD分别为1.82%、0.31%、0.20%、0.82%、0.99%、1.01%、0.74%。
2.5 样品测定取栀子全果、果皮、果仁及其炒黄和炒焦品9种样品粉末各0.20 g,每种饮片8批次,按“2.1”项方法制备供试品溶液,以“2.3”项色谱条件测定各种供试品溶液峰面积,按回归方程计算各成分质量分数,结果见表 1。
表 1 样品测定结果 (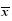 ±s, n = 8)
Table 1 Determination of content in sample ( ±s, n = 8)
Table 1 Determination of content in sample (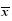 ±s,n = 8) ±s,n = 8) |
对栀子果仁、果皮、全果生品中的7种成分测定结果比较分析,发现各组分质量分数相差较大。其中去乙酰车叶草酸甲酯、绿原酸的量在栀子果皮中远高于栀子果仁(P<0.01),而栀子苷、京尼平龙胆二糖苷的量在栀子果仁中远高于栀子果皮(P<0.01),西红花苷I、西红花苷II的量在栀子果仁中明显高于栀子果皮(P<0.05)。分别对栀子全果及其炮制品,栀子果仁及其炮制品,栀子果皮及其炮制品7种成分质量分数进行比较分析,发现栀子各生品经炮制后,7种成分质量分数变化趋势基本一致,表现在京尼平苷酸质量分数升高,去乙酰车叶草酸甲酯、绿原酸、栀子苷、西红花苷I、西红花苷II质量分数下降,而京尼平龙胆二糖苷质量分数变化没有显著性差异。其中栀子苷在果仁、果皮生品炒黄后质量分数稍有下降,炒焦后质量分数下降明显(P<0.05);西红花苷I和西红花苷II在栀子各生品炮制后质量分数急剧下降。
3 讨论栀子中京尼平苷酸、去乙酰车叶草酸甲酯、京尼平龙胆二糖苷、栀子苷为环稀醚萜类化合物,结构相似,最大吸收波长均为240 nm,梯度洗脱有较好分离度;绿原酸最大吸收波长为330 nm;西红花苷I、西红花苷II的最大吸收波长均为440 nm,分离效果良好。通过方法学考察,本色谱条件可以准确检测栀子中7种成分的量。
实验结果表明,栀子炮制过程中不同化合物对热稳定性存在差异,强弱的顺序依次为京尼平龙胆二糖苷、栀子苷、去乙酰车叶草酸甲酯、绿原酸、西红花苷I、西红花苷II。京尼平苷酸质量分数升高,说明炮制可能促使栀子中其他化合物生成京尼平苷酸。
樟帮法炮制栀子需去皮留仁,从本实验中可以找到其内在的依据。鉴于果仁、果皮中栀子苷、西红花苷I、京尼平龙胆二糖苷质量分数的差异,可以认为栀子果仁在很多药效方面要比等量的栀子果皮的效果好。建昌帮法炮制栀子以果皮、果仁分用为特点,虽然栀子中很多有效成分的分布果仁中远高于果皮,但果皮中绿原酸、去乙酰车叶草酸甲酯质量分数远高于果仁,分别为果仁中的4.2、4.3倍。同时说明栀子果皮、果仁内在成分各有其特点,也可以认为在某些药效方面栀子果皮比果仁效果好。《本草备要》中也有“内热用仁,表热用皮”的论述[8],表明栀子果皮、果仁的使用具有针对性,与栀子建昌帮法炮制相一致。药典法炮制栀子是以栀子全果入药或炮制。由实验结果可知,尽管栀子果皮、果仁中的各种成虽然质量分数存在差异,但其有效成分种类极具相似性,说明了栀子药典法炮制的合理性。不同的炮制方法有其各自的特点,这也与一味药常有数种功效有关。为了更好地开发利用栀子,从资源保护角度,建议提倡药典法炮制栀子,且栀子樟帮法炮制与建昌帮法炮制并行发展。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 张学兰, 程合丽, 李慧芬. 栀子炮制的历史沿革研究 [J]. 中成药, 2005(11): 1281-1283. |
| [3] | 龚千锋. 樟树中药炮制全书 [M]. 南昌: 江西科学技术出版社, 1990. |
| [4] | 彭红, 付建武, 黄丽芸. 建昌帮法焦栀子炮制工艺研究 [J]. 中华中医药学刊, 2010, 28(5): 940-941. |
| [5] | 杜伟锋, 梁小娟, 吴晶宇, 等. 栀子炮制前后绿原酸、栀子苷和西红花苷I的比较 [J]. 中草药, 2011, 42(10): 2008-2010. |
| [6] | 付小梅, 彭水梅, 刘婧, 等. HPLC法同时测定栀子类药材中10个主要有效成分的含量 [J]. 药物分析杂志, 2014, 34(4): 615-621. |
| [7] | 苗琦, 罗光明, 罗扬婧, 等. 栀子多波长HPLC指纹图谱及化学模式识别研究 [J]. 中草药, 2014, 45(21): 3159-3164. |
| [8] | 汪昂. 本草备要 [M]. 天津: 天津科学技术出版社, 1993. |
 2015, Vol. 46
2015, Vol. 46


