葛根总黄酮(Puerariae Radix Flavones,PRF)是从中药葛根Pueraria lobata (Willd.) Ohwi中提取出的黄酮类物质,主要成分有葛根素、大豆苷元、大豆苷等,其具有改善微循环、扩张血管、增加冠脉流量、降低血压、减慢心律和降低心肌耗氧量的作用,同时还具有抗血栓、抗血管痉挛和抑制血小板聚集等功效,临床可用于高血压、高血脂、偏头痛、冠心病、心肌梗死、心绞痛等疾病的治疗[1, 2]。但是PRF在水中溶解性差,普通的口服片剂中溶出慢、吸收差、生物利用度低[3]。滴丸剂中药物以分子、微晶或胶体状态分散于基质中,分散度大,有利于难溶性药物在体内的溶解和吸收,具有速效、高效的特点[4]。本实验制备了PRF滴丸,采用HPLC法对其内的葛根素进行了测定,同时以葛根素为指标对制得滴丸与市售愈风宁心片的体外溶出度进行了比较,为PRF滴丸的进一步开发提供研究基础。
1 仪器与试药DWJ—2000S型多功能滴丸试验机(烟台百药泰中药科技发展有限公司);依利特230系列高效液相色谱仪(大连依利特有限公司);ZBS—6G型智能崩解仪、ZRS—8G溶出试验仪(天津天大天发科技有限公司);HWS24型电热恒温水浴锅(上海一恒科学仪器有限公司)。
PRF经UV法测定以芦丁计含黄酮80%,绵阳劲柏生物科技有限公司;二甲基硅油DY-201-100,山东大易化工有限公司;聚乙二醇(PEG)4000,广东光华化学有限公司;PEG 6000,天津市白世化工有限公司);葛根素对照品(中国食品药品检定研究院,批号110752-200912,质量分数以96.0%计);愈风宁心片(北京同仁堂健康药业有限公司,批号20120207);甲醇(色谱纯,天津科密欧化学试剂有限公司);纯净水(实验室自制)。
2 方法与结果 2.1 滴丸制备工艺研究 2.1.1 基质和冷凝液选择根据药物的性质和滴丸基质的理化特点,本实验选用了水溶性聚乙二醇作为基质。PEG 4000和PEG 6000因具有良好分散力和内聚力,是目前使用最广泛的2种滴丸基质。本实验以滴制的难易程度、滴丸的成型率、外观质量为考察指标,在药物与基质的比例为1∶3的条件下,分别以PEG 4000、PEG 6000、PEG 4000-PEG 6000(1∶1)为基质制备滴丸。结果显示以PEG 6000作为基质时滴制较困难,滴丸成型率较低;以PEG 4000-PEG 6000(1∶1)为基质滴制成的滴丸,易粘连,圆整度差,丸质量差异大;而以PEG 4000为基质时滴制较容易,滴丸成型率高,外观质量良好。故本实验选用PEG 4000作为滴丸基质。
冷凝液的选择,预试验分别测试了液体石蜡、二甲基硅油、蓖麻油作为冷凝液的冷凝效果,发现以二甲基硅油为冷凝剂时,滴丸的沉降速度适中,制得的滴丸不粘连,圆整度较好,故本实验选择二甲基硅油作为冷凝剂。
2.1.2 药物与基质比例对滴丸制备的影响将PRF与PEG 4000按不同的比例混合制成滴丸,其他条件固定(药液温度为80 ℃,管口温度为40 ℃,冷凝液温度为10 ℃,滴距为6 cm,滴速为30滴/min),以制得滴丸的外观质量评分[5, 6](包括圆整度、硬度、拖尾,外形由不圆至圆分为1~5级,硬度由软至硬分为1~5级(硬度仪测定),拖尾情况由差至好分为1~5级)、丸质量差异、溶散时限为评价指标,结果见表 1。
|
|
表 1 药物与基质比例对滴丸制备的影响 Table 1 Effects of proportion between drug and matrix on preparation of dropping pills |
实验结果表明,药物与基质比例为1∶2时,药液流动性差,较难滴制,制得滴丸的外观质量较差。药物与基质比例为1∶3~1∶6时,滴丸成型率高,外观质量良好,丸质量差异和溶散时限均较小,但考虑到滴丸的载药量问题,药物与基质比例应选择1∶3~1∶5较为合适。
2.1.3 药液温度对滴丸制备的影响滴丸基质PEG 4000的熔点为55 ℃左右,故药液温度不可低于60 ℃,预试验发现,药液温度在70 ℃以下时,滴制较慢,拖尾较严重,所以选择药液温度在70、80、90、100 ℃,其他条件固定,考察不同药液温度时滴丸的质量,结果见表 2。药液温度在70~90 ℃时,制得滴丸的外观质量较好,丸质量差异小,但当药液温度达到100 ℃,滴丸易粘连,制得滴丸圆整度不佳,丸质量差异大。
|
|
表 2 药液温度对滴丸的影响 Table 2 Effects of drug fluid temperatures on dropping pills |
滴距主要影响滴丸的圆整度。滴距过小,液滴来不及收缩,即落入冷凝液中,制得滴丸不圆整易拖尾;滴距过大,液滴易受重力作用跌散而产生小粒,丸质量差异大。预试验结果发现,滴距在4~8 cm,对滴丸质量影响不大,本实验选择滴距为6 cm。
滴速也是影响滴丸成型的重要因素。滴制速度过快,滴丸受重力影响较大,滴丸较扁,易粘连;滴制速度过慢,液滴变大,滴丸变重,丸质量差异大,同时生产效率降低。经预试验结果发现,滴速在20~40滴/min时,制得滴丸质量较好。
2.1.5 冷凝温度对滴丸制备的影响本实验使用的滴丸机冷凝液采用的是梯度冷却技术,在1.2 m长的冷凝管中,管口部分可以加热,管底部分可以降温,可把管口温度和冷凝液下部制冷温度分别进行考察,以研究2因素对滴丸质量的影响。
管口温度主要影响滴丸的圆整度和丸质量差异。管口温度过低,液滴提前收缩,丸型不圆整;管口温度过高,液滴易粘连,丸质量差异较大。参考有关文献并结合预试验结果[7],管口温度选择在30~50 ℃较为合适。其他条件固定,对冷凝液下部制冷温度进行考察,研究发现,制冷温度在12 ℃以下时制得滴丸的质量无显著性差异。从节约能源角度,选择冷凝液下部制冷温度为10 ℃。
2.1.6 正交试验设计在PRF滴丸制备工艺单因素考察的基础上,选取对滴丸质量影响较大的4个因素:药物与基质比例(A)、滴速(B)、药液温度(C)、管口温度(D),采用L9(34) 正交试验设计对滴丸的成型工艺作进一步优化,以其获得PRF滴丸的最佳制备工艺。滴丸的质量评价目前并无统一的指标,本实验参考有关文献[8],以制得滴丸的外观质量评分(y1)、丸质量变异系数(y2)、溶散时限(y3)为评价指标,采用综合评分(加权评分)法来评价滴丸质量,综合评分=100×y1i/y1max×0.3+100×y2min/y2i×0.4+100×y3min/y3i×0.3。试验设计与结果见表 3,方差分析见表 4。
|
|
表 3 L9(34) 正交试验设计与结果 Table 3 Design and results of L9(34) orthogonal test |
|
|
表 4 方差分析 Table 4 Analysis of variance |
正交试验结果表明药物与基质比例是影响PRF滴丸质量的主要因素,对滴丸的质量有显著性意义。影响PRF滴丸制备的因素主次顺序为药物与基质比例>滴速>药液温度>管口温度,最佳工艺为A2B1C2D3,但考虑到滴丸的载药量问题,最终将PRF滴丸的工艺条件定为药物与基质比为1∶3,滴速20滴/min,药液温度为80 ℃,管口温度为50 ℃,滴距为6 cm,制冷温度为10 ℃。
2.1.7 验证试验按上述工艺条件重复制备滴丸3批(批号分别为121011、121128、130116),并对其外观质量、丸质量差异系数、溶散时限进行考察,结果显示制得滴丸的外观质量良好,丸质量变异系数在2.34%~2.42%,溶散时限在5.81~5.85 min,表明该制备工艺重现性良好,结果见表 5。
|
|
表 5 验证实验结果 Table 5 Results of verification |
色谱柱依利特C18柱(200 mm×4.6 mm,5 μm),流动相为甲醇-水(25∶75),体积流量为1.0 mL/min,进样量为20 μL,检测波长为250 nm,柱温为30 ℃。
2.2.2 对照品溶液的制备取葛根素对照品适量,精密称定质量,加甲醇溶解并稀释制成含葛根素1 mg/mL的溶液,作为对照品储备液,吸取对照品储备液定量稀释至适宜质量浓度。
2.2.3 供试品溶液制备取滴丸20粒研碎,精密称定0.1 g,置50 mL三角瓶中,加30%乙醇25 mL,称定质量,超声30 min,放冷,用30%乙醇补足减少的质量,滤过,取滤液2 mL于10 mL量瓶中,加30%乙醇稀释至刻度,微孔滤膜滤过,即得。
2.2.4 阴性对照溶液制备参照PRF滴丸的制备工艺制得不含药物的空白滴丸,按“2.2.3”项方法,制得阴性对照溶液。
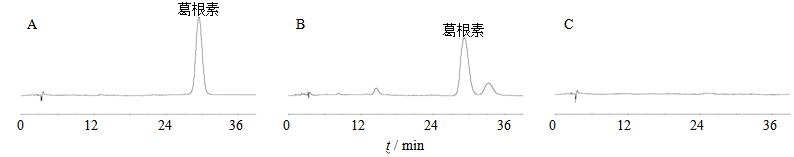
2.2.5 方法专属性考察分别取葛根素对照品溶液,供试品溶液以及阴性对照溶液,按照上述色谱条件进行测定,结果见图 1。由图可见,葛根素的保留时间约为29 min,阴性对照对葛根素的测定无干扰。
|
图 1 葛根素对照品 (A)、供试品 (B) 和阴性对照 (C) 的HPLC色谱图 Fig.1 HPLCof puerarin reference substance (A), sample (B),and negative reference substance (C) |
取对照品储备液分别配成质量浓度为348、174、87、43.5、21.75 μg/mL的对照品溶液,进样,以对照品质量浓度为横坐标(X),相应的峰面积为纵坐标(Y),绘制标准曲线,回归方程为Y=70 928 X-240 569,r=0.999 8,结果表明,葛根素浓度在21.75~348 μg/mL与峰面积具有良好的线性关系。
2.2.7 精密度试验取同一质量浓度的对照品溶液(87 μg/mL),在上述色谱条件下重复进样6次,计算得出葛根素峰面积的RSD值为1.0%,进样精密度较好。
2.2.8 重复性试验取同一批滴丸(批号121011),按照供试品溶液制备方法平行制备6份供试品溶液,在上述色谱条件下,进样,计算葛根素峰面积的RSD值为1.4%,实验重复性良好。
2.2.9 稳定性试验取同一供试品溶液(“2.2.8”中的1份),分别于0、2、4、6、8、24 h时进样,然后计算葛根素峰面积的RSD为1.1%,说明在24 h内供试品溶液稳定性良好。
2.2.10 加样回收率试验取已测定葛根素的滴丸(批号121011)研碎,精密称定9份粉末,每份约0.05 g,分别加入522、348、174 μg的对照品,配成高、中、低3个质量浓度,每个质量浓度3份,按供试品溶液制备方法处理,计算葛根素平均回收率为102.9%,RSD为1.5%。
2.2.11 样品测定取所制备的不同批号的滴丸样品3批(批号121011、121128、130116),每批分别按“2.2.3”项方法制备供试液,分别测定,结果葛根素分别为5.496、5.561、5.568 mg/g,平均为5.542 mg/g,RSD为0.7%。
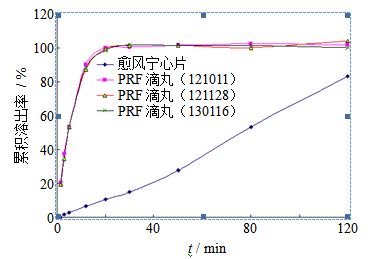
2.3 体外溶出度考察 2.3.1 滴丸与片剂的溶出度比较药物体外溶出度参照《中国药典》2010年版,采用转篮法测定,取滴丸或片剂适量,以水为溶出介质,转速为100 r/min,温度为(37±0.5)℃,依法测定,分别于1.5、3、5、12、20、30、50、80、120 min取样5 mL,经0.45 μm微孔滤膜滤过,得供试品溶液。取样后补充等量等温的溶出介质[9]。供试品溶液按上述葛根素定量测定方法,测定葛根素质量浓度,计算累积溶出率,绘制时间-累积溶出率曲线,见图 2。结果显示,滴丸在20 min内累积溶出率就可达到98.81%,但普通片剂20 min内的累积溶出仅有10.70%,120 min累积溶出也只有82.98%。将滴丸与普通片剂的溶出时间数据分别进行威布尔函数拟合[10],滴丸的溶出参数T50为4.38 min,而片剂的溶出参数T50为71.24 min,表明葛根素在滴丸剂中溶出速度远远大于片剂,两者有明显差异,滴丸可以达到速效作用。
|
图 2 滴丸与片剂的体外溶出比较 Fig. 2 Comparison on dissolution between dropping pills and tablets |
取同一批PRF滴丸(批号121011)6粒,按溶出度测定方法,测得滴丸在20 min内的溶出度,结果见表 6。6粒滴丸每个时间点的累积释放率的RSD均<10%,显示滴丸批内溶出均一性良好。取PRF滴丸3批(批号121011、121128、130116),按溶出度测定方法测定,结果见表 7。结果显示3批滴丸在每个时间点累积溶出率的RSD均<5%,该滴丸溶出度检查重复性较好、工艺稳定。
|
|
表 6 滴丸溶出均一性考察 Table 6 Equality of dissolution of dropping pills |
|
|
表 7 滴丸溶出重复性考察 Table 7 Reproducibility of dissolution of dropping pills |
本实验通过单因素考察和正交试验设计探讨了PRF滴丸的最佳成型工艺,研究发现基质用量越多,滴丸的成型性越好,滴制越容易,正交试验筛选出PRF与PEG 4000的比例最佳为1∶4,但考虑到滴丸的载药量小,服用剂量大,且药物与PEG 4000比例为1∶3时,制得滴丸的评分亦较高,最终的成型工艺为药物与基质比例选择了1∶3,滴速为20滴/min,药液温度为80 ℃,管口温度为50 ℃,滴距为6 cm,制冷温度为10 ℃,二甲基硅油为冷凝剂。以此工艺制备滴丸3批,并对制得滴丸进行质量评价,滴丸的外观质量好,丸质量差异系数和溶散时限均较小,符合《中国药典》2010年版滴丸剂项下规定,质量无显著性差异,此制备工艺简单合理,稳定可行。
葛根素是PRF中的主要有效成分,其与PRF的临床疗效密切相关,检测PRF滴丸中葛根素的量对于其质量控制有重要意义。本实验采用HPLC测定了滴丸中葛根素的量,经验证该方法简便、准确、可靠。在滴丸的体外溶出考察中亦选择了葛根素作为检测指标,能客观真实地反应制剂的溶出性能,为其临床应用提供科学数据。体外溶出实验表明,滴丸剂可实现难溶性成分的快速溶出、释放。
| [1] | 李 喆, 周莹君, 李素霞, 等. 中药葛根的研究进展[J]. 中国中医药现代远程教育, 2012, 10(19): 164-165. |
| [2] | 潘洪平. 葛根总黄酮和葛根素的药理作用和临床应用进展[J]. 广西药学, 2003, 25(10): 1941-1942. |
| [3] | 张嘉家, 易荆丽, 周毅生, 等. 葛根总黄酮分散片的处方工艺研究及溶出度测定[J]. 广东药学院学报, 2012, 28(6): 1-5. |
| [4] | 诸葛周, 戴德雄, 朱 莹. 肿节风滴丸的制备工艺研究[J]. 中草药, 2011, 42(9): 1759-1760. |
| [5] | 李扬秋, 崔升淼, 邢占磊. 穿心莲内酯滴丸的制备工艺研究[J]. 时珍国医国药, 2010, 21(9): 2381-2383. |
| [6] | 王治平, 孟祥平, 樊 化, 等. 鼻渊滴丸的制备研究[J]. 中成药, 2006, 28(1): 126-128. |
| [7] | 宋凤兰, 李碧云, 龚政奇, 等. 葛根芩连滴丸的成型工艺研究[J]. 海峡药学, 2012, 24(10): 20-23. |
| [8] | 俞 金, 崔佰吉, 张秀荣. 五味子滴丸成型工艺的研究[J]. 中国现代应用药学, 2010, 27(4): 326-329. |
| [9] | 周郁斌, 袁中文, 李海刚, 等. 用Origin软件计算药物溶出度Weibull分布参数[J]. 医药导报, 2011, 30(6): 721-723. |
| [10] | 华 洁, 马素珍, 阎立萍. 葫芦素滴丸与片剂的溶出对比研究[J]. 中草药, 2004, 35(10): 1131-1132. |
 2014, Vol. 45
2014, Vol. 45

