2. 南京中医药大学, 江苏 南京 210046
2. Nanjing University of Chinese Medicine, Nanjing 210046, China
微晶纤维素(microcrystalline cellulose,MCC)是以木材或棉花为原料制备的白色或类白色无臭、无味的多孔性微晶状颗粒或粉末,具有高度可变形性,对主药具有较大的容纳性,可作为片剂的填充剂、干燥粘合剂、微丸的成球剂,同时具有崩解作用,在制剂中应用十分广泛[1, 2]。然而MCC的结构中有很多羟基,故其自身具有一定的吸湿性,与吸湿性强的中药浸膏联用时,制剂成型过程中物料吸湿较快[3]。单硬脂酸甘油酯(glycerol monostearate,GMS)是含有C16-C18长链脂肪酸与丙三醇进行酯化反应而制得,是一种非离子型的表面活性剂,它既有亲水又有亲油基因,具乳化等多种功能,是食品和药品常用的添加剂,安全性好[4],且不溶于水,但与热水经强烈振荡混合后可分散于水中。
复合辅料,是将多种单一辅料按一定比例,经一定的工艺共同处理,均匀混合在一起,成为一种具有特定功能且表观均一的新辅料[5, 6]。复合辅料保持或改善了单一辅料的优点,同时也弥补了其不足之处[7, 8, 9, 10]。喷雾干燥法是目前复合辅料常用制备方法之一,通过喷雾干燥制备的复合辅料颗粒细小,粒径分布范围窄,流动性较好[11]。考虑到GMS的亲水基团可以和MCC的羟基缔合,而其疏水基团则可能伸向外部,从而降低MCC的吸湿性。故本实验采用喷雾干燥法制备MCC-GMS的复合辅料,尝试改善MCC在中药应用中的抗吸湿性。
实验选择吸湿性较强的馨月舒、淫羊藿总黄酮以及枸杞提取物的喷雾干燥粉体为模型药物[12],考察复合辅料对其吸湿性的影响,并研究以该复合辅料压制的馨月舒片剂中有效成分金丝桃苷和阿魏酸的溶出行为。
1 仪器与材料Labplant喷雾干燥仪(英国LabPlant公司);Agilent1100高效液相色谱仪;TDP型单冲压片机(上海天祺制药机械有限公司);ZB—2E智能崩解仪(天大天发仪器公司);Rcz—6B3型药物溶出度仪(上海黄海药检仪器有限公司);EyeTech激光粒度粒形分析仪(荷兰安米德Ankersmid有限公司);DSC204差示扫描量热仪(德国Netzsch公司);6390LV扫描电镜(日本电子公司);D8型X射线衍射仪(德国Bruker公司);470傅里叶红外光谱仪(美国Nicolet公司)。
对照品金丝桃苷(批号1512-200202)、阿魏酸(批号110773-201012),中国食品药品检定研究院;MCC(批号6610113219),上海昌为医药辅料科技有限公司;GMS(批号20100816),成都市科龙化工试剂厂);硬脂酸镁(批号20120723),国药集团化学试剂有限公司;乳糖(批号101012),上海博微生物科技有限公司;微粉硅胶(批号110624),安徽山河药用辅料股份有限公司;馨月舒喷雾干燥粉体(自制);淫羊藿总黄酮喷雾干燥粉体(自制);枸杞提取物喷雾干燥粉体(自制);乙腈为色谱纯,水为高纯水,其余试剂均为分析纯。
2 方法与结果 2.1 复合辅料MCC-GMS的制备 2.1.1 制备方法将MCC和GMS按比例加入热水中,在磁力搅拌器上乳化混合一定时间,喷雾干燥,过筛,备用。
2.1.2 制备工艺优化以GMS的乳化温度、水与GMS的比例、MCC与GMS的比例以及搅拌时间为可变因素,以复合辅料的吸湿性、流动性、可压性和崩解度为综合考察指标(各指标换算指数计算方法:将该组实验结果中数值最大的数据设为1,其余数据按相应比例换算,综合评分=吸湿性换算指数×3+休止角换算指数+崩解度换算指数-卡氏指数换算指数),采用均匀设计法优选复合辅料的制备工艺。
本实验采用均匀设计法优化复合辅料的制备工艺,预试验结果显示,搅拌时间达到1 h后,即见不到GMS的乳滴,故选择影响实验结果的3个主要因素,并确定其变化范围:乳化温度(A)为62~66 ℃;水与GMS的比例(B)为120∶1~200∶1;MCC与GMS的比例(C)为8∶1~12∶1。将各因素均分为5个水平,其因素与水平见表 1。
|
|
表 1 U10(1010) 均匀试验设计与结果 Table 1 Uniform experimental design and results of U10(1010) |
由于本实验的因素B水平范围较宽,为提高实验的精度和结论的可靠性,采用拟水平法,选用U10(1010) 的使用表安排实验方案,试验方案以及试验结果见表 1,其中实验结果栏对应的括号内的数值为各指标的换算指数。列方差分析表进行F比检验,见表 2。
|
|
表 2 方差分析 Table 2 Analysis of variance |
样本容量N=10,显著性水平α=0.05,检验值Ft=77.96,临界值F0.05(5,4)=6.256,Ft>F0.05(5,4),回归方程显著。最后,经过线性变换,得回归方程为Y=-115+3.66 X1+0.041 2 X2-0.125 X3-0.028 6 X12-0.000 137 X22。利用此方程可寻找实验范围内最优工艺条件为水-GMS 200∶1、MCC-GMS 12∶1、乳化温度66 ℃,搅拌时间达到1 h,此时的综合考察指标最优。
2.2 混合辅料MCC-GMS的制备MCC和GMS按一定比例,过筛后混合均匀,备用。
2.3 复合辅料粉体学性质考察 2.3.1 粒径及粒径分布抽真空状态下将适量样品均匀分散于载玻片上,再将载玻片置于激光粒度分析仪内,测定其粒径及粒径分布,结果见表 3[D代表粉体颗粒的直径,D50表示累积50%点的直径(或称50%通过粒径),又称平均粒径或中位径,D10、D90分别表示10%、90%通过粒径],结果表明复合辅料的粒径较混合辅料更小。
|
|
表 3 粒径与粒径分布(x±s,n=3) Table 3 Partical size and distribution of powder(x±s,n=3) |
采用固定圆锥底法,即取一定量的待测粉末,在一定振动频率下使粉末通过漏斗均匀流出,直到获得最高的圆锥体为止,测量圆锥体斜面与平面的夹角即得;重复3次,取其平均值,即得休止角。给予一定强度的振动,使粉末均匀流入一个10 mL杯子中,用刮片刮掉杯子上面多余的粉末,称定质量,质量除以10即得松密度。在粉末均匀流入10 mL杯子的同时,对杯子给予一定强度的撞击(3 min,180次),刮掉杯子上面多余的粉末,称定质量,质量除以10即得轻敲密度。卡氏指数通过公式:卡氏指数=(1-松密度/轻敲密度),计算而得。测定结果见表 4。
|
|
表 4 休止角和卡氏指数(x±s,n=3) Table 4 Repose angle and Carr index of excipient(x±s,n=3) |
结果表明,复合辅料的休止角在37°左右,显示出良好的流动性,而简单混合物的休止角达42°,流动性较差。卡氏指数反映粉末的压缩性和流动性。卡氏指数大的粉末通常可压性好,但流动性差;卡氏指数小的粉末流动性好,但可压性差。一般情况下,当卡氏指数介于15%~25%时,粉末的流动性和可压性均能达到直接压片的要求[6]。复合辅料的卡氏指数为23%,在此区间,故显示了较好的可压性,但混合辅料的卡氏指数超过了25%,这可能与MCC的海绵状多孔结构有关。结果说明了喷雾干燥法制备的复合辅料流动性和可压性都较好。
2.4 复合辅料微观结构研究 2.4.1 电子扫描显微镜(SEM)观察采用喷金法观察表面结构。将样品置于玻璃皿内,离子溅射后用SEM观察样品表面结构,加速电压为25.0 kV,结果见图 1。SEM结果显示,A、B分别为MCC和GMS的电镜扫描图,C为混合辅料,其中可以明显观察到2种辅料的单独特征,D为复合辅料,可以看出2种辅料在喷雾干燥后形成一整体颗粒,呈棒状,表面较光滑,粒度分散均匀。

|
图 1 MCC (A)、GMS (B)、混合辅料 (C) 和复合辅料 (D) 的SEM图 Fig.1 SEM imagines of MCC (A),GMS (B),mixedexcipient (C), and co-processd excipient (D) |
测试条件为铝坩埚;气氛为氮气;升温速率为10.00 ℃/min;升温范围为0~500 ℃,各样品的测试结果见图 2。DSC曲线图显示:MCC在335 ℃左右处分别出现1个明显吸热峰;GMS在75 ℃左右处出现1个明显的吸热峰;混合辅料可见MCC的吸热峰和GMS的吸热峰存在,而复合辅料中只见MCC的吸热峰,GMS的吸热峰显著缩小,考虑可能是由于GMS乳化之后与MCC进行复合时,产生相互作用导致。对比混合辅料和复合辅料DSC谱线,可知MCC与GMS未产生新的吸热峰,提示二者没有化学组分上的改变。

|
图 2 (A)、GMS (B)、混合辅料 (C) 和复合辅料 (D)的DSC图 Fig.2 DSC curves of MCC (A), GMS (B), mixed excipient (C), and co-processd excipient (D) |
测试条件为Cu靶(40 kV,40 mV);步进扫描为0.01°/步;扫描范围为5°~70°;扫描速度为4°/min。各测试样品的X射线衍射分析结果如图 3所示,MCC在20°~25°有一强的结晶特征衍射峰;GMS在18°~26°有多个结晶特征峰;混合辅料的谱线中GMS仍有结晶衍射峰存在,与MCC的结晶特征衍射峰相

|
图 3 MCC (A)、GMS (B)、混合辅料 (C) 和复合辅料 (D)的X衍射图谱 Fig.3 XRD patterns of MCC (A), GMS (B), mixed excipient (C), and co-processd excipient (D) |
重叠,说明GMS晶型未发生改变,化学组分也未发生变化;而在复合辅料的谱线中GMS结晶衍射峰显著减少。X衍射结果进一步证实部分GMS以无定形状态或分子状态分散在复合辅料中。
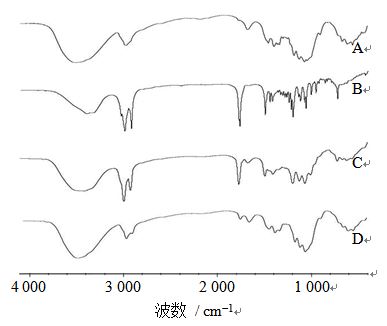
2.4.4 傅里叶变换红外光谱(FTIR)考察采用KBr压片法测定FTIR,将样品与KBr在干燥环境下混合制片后,分辨率为4 cm-1,在4 000~500 cm-1全谱扫。各测试样品的红外光谱分析结果如图 4所示,A为MCC的FTIR,其中3 500 cm-1的吸收峰为羟基峰[13];C为混合辅料的FTIR,可见MCC和GMS的几处特征峰,部分峰因为重叠而发生细微的变化;D为复合辅料的FTIR,其中3 500 cm-1左右的羟基峰变宽且峰强变弱,提示MCC的部分羟基与GMS产生缔合作用。
|
图 4 MCC (A)、GMS (B)、混合辅料 (C) 和复合辅料 (D)的FTIR图 Fig.4 FTIRspectraof MCC (A), GMS (B), mixed excipient (C), and co-processd excipient (D) |
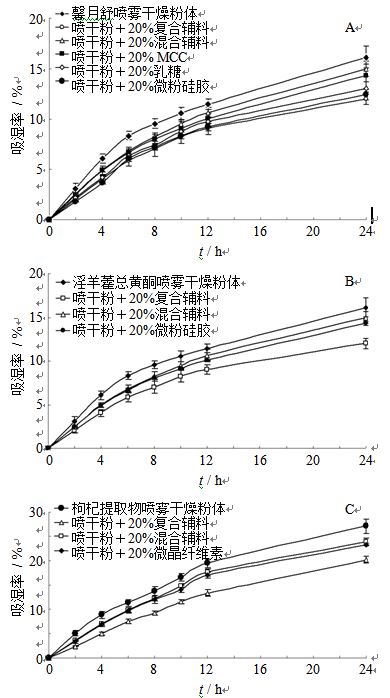
在馨月舒的喷雾干燥粉体中分别添加0、20%复合辅料、20%混合辅料、20% MCC、20%乳糖和20%微粉硅胶,混合均匀后进行吸湿性考察,在淫羊藿总黄酮、枸杞提取物的喷雾干燥粉体中分别添加0、20%复合辅料、20%混合辅料和20% MCC,混合均匀后进行吸湿性考察。将底部盛有氯化钠过饱和溶液的玻璃干燥器放入恒温培养箱中(25 ℃)恒温24 h,此时干燥器内的相对湿度为75%。根据《中国药典》2010年版附录XIXJ药物引湿性试验指导原则,在已恒定质量的称量瓶中分别放入干燥至恒定质量的各粉体适量,准确称定质量后置于干燥器中,25 ℃恒温保存,分别于2、4、6、8、10、12、24 h定时称量,计算吸湿率[吸湿率=(吸湿后质量-吸湿前质量) / 吸湿前质量],结果见图 5。
|
图 5 馨月舒片 (A)、淫羊藿总黄酮 (B) 和枸杞提取物 (C)喷雾干燥粉的吸湿平衡曲线 Fig. 5 Hydroscopic equilibrium curves of spray-drying powder in Xinyueshu Tablet (A), epimedium total flavonoids (B), and wolfberry extracts (C) |
由实验结果可知,馨月舒、淫羊藿总黄酮或枸杞提取物的喷雾干燥粉中加入辅料均能明显降低其吸湿性,且各种辅料抗吸湿效果的大小顺序为20%混合辅料<20%MCC<20%复合辅料。复合辅料的抗吸湿性效果大于相同用量的混合辅料以及MCC,说明将MCC与GMS制备成复合辅料,能增强MCC的抗吸湿效果并明显改善喷雾干燥粉的吸湿性。且对比与其他已上市的常用辅料,例如乳糖和微粉硅胶,该复合辅料对馨月舒喷雾干燥粉体的吸湿性改善更具优势。
2.6 复合辅料压制空白片剂的崩解时限测定 2.6.1 空白片剂的制备分别在MCC、混合辅料和复合辅料中加入0.5%的硬脂酸镁[14],混合均匀,放于单冲压片机,在相同压力下压成直径10 mm、片质量约0.30 g的平面片剂,得到不同辅料压制的空白片剂。
2.6.2崩解时限的测定崩解时限的测定 将吊篮固定在一能升降的金属杆上,浸入500 mL烧杯中(烧杯中盛有温度为37 ℃的水),上下运动。从把片剂加入吊篮中开始计时,直至完全崩解通过吊篮筛网,即为片剂的崩解时限。不同辅料(MCC、混合辅料、复合辅料)的崩解时限分别为(18±1)、(27±2)、(20±1)s(n=6)。
结果表明,MCC在片剂中除做填充剂外还兼有崩解剂的作用,复合辅料的崩解时限为20 s,与MCC本身的崩解时限相差不大,说明GMS与MCC通过喷雾干燥法复合之后,并未对MCC的崩解作用产生明显的影响,并且复合辅料比混合辅料崩解时限短。
2.7 辅料容纳量考察辅料容纳量或称稀释容纳量(稀释潜能),指辅料最大比例与药物结合而制成符合要求的片剂时,药物在片剂中的质量分数[15]。分别取馨月舒、淫羊藿总黄酮作为活性药物成分,与MCC或复合辅料以不同比例混合均匀,采用单冲压片机直接压片制备片剂,当各项指标(如外观、硬度等)符合片剂要求时可以容纳药物的最大量,即为该辅料对药物的稀释潜能。实验测得MCC和复合辅料对馨月舒、淫羊藿总黄酮的喷雾干燥粉体的辅料容纳量分别为MCC 50%和55%、复合辅料40%和50%。结果表明复合辅料MCC-GMS对不同中药提取物的辅料容纳量略低于单一辅料MCC,且辅料对淫羊藿总黄酮的承载能力略大于馨月舒喷雾干燥粉体。
2.8 复合辅料对馨月舒中金丝桃苷和阿魏酸溶出度的影响 2.8.1 色谱条件金丝桃苷:色谱柱为Agilent HC- C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈- 0.1%磷酸水溶液(17∶83);检测波长360 nm;体积流量为1 mL/min;柱温为30 ℃;进样量20 μL。理论塔板数以金丝桃苷计不低于3 000。阿魏酸:色谱柱为Agilent HC-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.085%磷酸水溶液(17∶83);检测波长316 nm;体积流量为1 mL/min;柱温为35 ℃;进样量20 μL。理论塔板数以阿魏酸计不低于3 000。
2.8.2 线性关系考察金丝桃苷:精密称取金丝桃苷对照品1.96 mg,置于2 mL量瓶中,甲醇溶解并稀释至刻度,摇匀,精密吸取对照品储备液1.0 mL,置于50 mL量瓶中,甲醇稀释至刻度,摇匀,得19.6 μg/mL对照品储备液。分别精密吸取混合对照品储备液0.5、1.0、2.0、4.0、6.0、8.0 mL各置10 mL量瓶中,加甲醇稀释至刻度,摇匀。按上述色谱条件取样,进行HPLC测定其对应的峰面积,以对照品溶液的进样质量浓度为横坐标(X),对应的峰面积为纵坐标(Y),进行线性回归,得回归方程Y=28.762 X-2.284 8,r=0.999 8,结果显示金丝桃苷在0.98~19.60 μg/mL线性关系良好。
阿魏酸:精密称取阿魏酸对照品3.34 mg,置于2 mL量瓶中,甲醇溶解并稀释至刻度,摇匀,精密吸取对照品储备液1.0 mL,置于50 mL量瓶中,甲醇稀释至刻度,摇匀,得33.40 μg/mL对照品储备液。分别精密吸取混合对照品储备液0.5、1.0、2.0、4.0、6.0、8.0 mL各置10 mL量瓶中,加甲醇稀释至刻度,摇匀。按上述色谱条件取样,进行HPLC测定其对应的峰面积,以质量浓度为横坐标(X),对应的峰面积为纵坐标(Y),进行线性回归,得回归方程Y=32.584 X-4.153 6,r=0.999 9,结果显示阿魏酸在1.67~33.40 μg/mL线性关系良好。
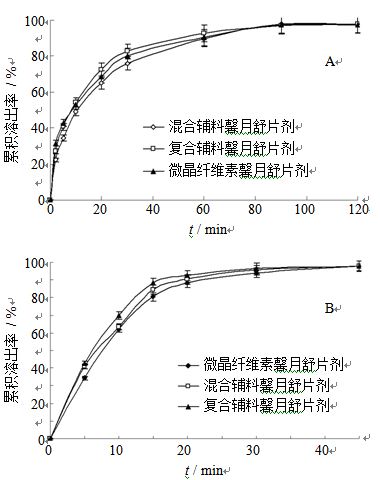
2.8.3 药物的溶出度测定取馨月舒喷雾干燥粉体3份各适量,分别添加二倍量的MCC、混合辅料和复合辅料,混合均匀。再分别加入0.5%硬脂酸镁[14],混合均匀,放于单冲压片机,在相同压力下压成直径10 mm、片质量约0.30 g的平面片剂。按溶出度测定方法测定(《中国药典》2010年版二部附录XC桨法),以经脱气处理的纯化水(900 mL)为溶出介质,转速50 r/min,温度(37.0±0.5)℃,分别于5、10、15、20、30、60、90、120 min&l t;/ span>定时定点取样2 mL(同时补加同温度等量溶出介质),以0.45 μm微孔滤膜滤过,弃去初滤液,取续滤液20 μL进行HPLC测定,测定结果代入标准曲线计算质量浓度,并换算成累积溶出率,以时间为横坐标,累积溶出率为纵坐标作图,金丝桃苷和阿魏酸从片剂中溶出的曲线分别见图 6。
|
图 6 不同辅料对馨月舒片剂中金丝桃苷 (A) 和阿魏酸(B) 溶出度的影响 Fig.6 Effects of different excipients on accumulative dissolution rate of hyperside (A) and ferulic acid (B) from Xinyueshu Tables |
实验分别选择测定馨月舒复方中水溶性较差的有效成分金丝桃苷和水溶性较好的阿魏酸的溶出速率,结果表明,分别添加不同辅料的片剂在60 min左右,溶出达到平衡。在前5 min,MCC压制的馨月舒片剂累积溶出度较快,可能是由于其崩解时限短,药物能较快地从片剂中释放;在溶出的中间过程,分别以MCC、混合辅料和复合辅料压制的馨月舒片剂中金丝桃苷和阿魏酸的累积溶出度无显著性差别。
3 讨论MCC与GMS经喷雾干燥形成的复合辅料可以改善馨月舒、淫羊藿总黄酮和枸杞提取物喷雾干燥粉体的吸湿性,分析原因可能是GMS的亲水基团可以和MCC的羟基缔合,而其疏水基团则可能伸向外部,从而降低MCC的吸湿性。分析表征图谱发现辅料复合前后化学成分没有发生改变,并表现出更好的流动性,而且从崩解时限的实验结果可以看出GMS的加入并未影响MCC的崩解作用。
本课题组前期研究制备了水溶性的复合辅料硬脂酰富马酸钠-共聚维酮,其能显著改善当归喷雾干燥粉体吸湿性[7]。但这种水溶性复合辅料成本较高,适于在颗粒剂等水溶性制剂中应用。相比之下MCC-GMS复合辅料虽然不溶于水,但是制备成本较低,更适宜于在片剂和胶囊等制剂中应用。
| [1] | 崔福德. 药剂学[M]. 第6版. 北京: 人民卫生出版社, 2010. |
| [2] | 杨明世, 何继东, 崔福德, 等. 一些常用片剂填充剂与崩解剂的性能比较[J]. 沈阳药科大学学报, 2001, 18(5): 316-319. |
| [3] | 朱 蕾, 冯 怡, 徐德生, 等. 中药提取物与微晶纤维素混合物的物理性质与其片剂成型性的相关性研究[J]. 中国医药工业杂志, 2008, 39(5): 349-351. |
| [4] | 陈小云, 张振海, 郁丹红, 等. 丹参酮组分缓释固体分散体的研究[J]. 中草药, 2013, 44(17): 2391-2396. |
| [5] | Gohe M C, Jogani P D. Exploration of melt granulation technique for the development of co-processed directly compressible adjuvant containing lactose and microcrystalline cellulose[J]. Pharm Dev Technol, 2003, 8(2):175-85. |
| [6] | Nachaegari S K, Bansal A K. Coprocessed excipients for solid dosage forms[J]. Pharm Technol, 2004, 28(1): 52-64. |
| [7] | 蒋艳荣, 张振海, 贾晓斌. 复合辅料富马酸钠-共聚维酮的制备及其应用[J]. 药学学报, 2013, 48(1): 125-130. |
| [8] | Ogunjimi A T, Alebiowu G. Aquantitative study of the influence of coprocessing of binders on the mechanical properties ofparacetamol tablets[J]. Braz J Pharm Sci, 2010, 46: 205-212. |
| [9] | Block L H, Moreton R C, Apte S P, et al. Co-processed excipients[J]. Pharm Forum, 2009, 35: 1026-1028. |
| [10] | 何 群, 赵碧清, 滕久祥, 等. 九香止泻方喷雾和减压干燥品中有效成分比较[J]. 中草药, 2011, 42(8): 1550-1553. |
| [11] | 曾文雪, 王金钱, 张爱玲, 等. 共处理辅料的开发应用及其存在问题分析[J]. 中成药, 2009, 31(7): 1096-1099. |
 2014, Vol. 45
2014, Vol. 45


