2. 中国食品药品检定研究院 中药民族药检定所, 北京 100050;
3. 福建中医药大学药学院, 福建 福州 350008
2. Research and Inspection Center of Traditional Medicine and Ethnomedicine, National Institutes for Food and Drug Control, Beijing 100050, China;
3. School of Pharmacy, Fujian University of Traditional Chinese Medicine, Fuzhou 350008, China
淫羊藿又名仙灵脾、刚前,是小檗科淫羊藿属Epimedium Linn. 植物,始载于《神农本草经》,列为中品,具有补肾阳、强筋骨、祛风湿的功效,在我国具有悠久的药用历史。中国是淫羊藿的地理分布中心,有40个淫羊藿品种,目前形成药材商品的主要种类有15种,这其中又以7种淫羊藿应用最广,为箭叶淫羊藿E. sagittatum (Sieb. et Zucc.) Maxim.、淫羊藿E. brevicornum Maxim.、粗毛淫羊藿E. acuminatum Franch.、朝鲜淫羊藿E. koreanum Nakai、柔毛淫羊藿E. pubescens Maxim.、黔岭淫羊藿E. leptorrhizum Stearn、巫山淫羊藿E. wushanense T. S. Ying。在《中国药典》2010年版中收录了箭叶淫羊藿、朝鲜淫羊藿、柔毛淫羊藿、淫羊藿共4个品种。贵州省是我国淫羊藿品种最多、产藏量最大的地区之一,其分布的淫羊藿属植物有17种2变种,其中,粗毛淫羊藿、黔岭淫羊藿、巫山淫羊藿等分布广且产藏量丰富[1],在《贵州中药材、民族药材质量标准》2003年版中收录了粗毛淫羊藿、黔岭淫羊藿、天平山淫羊藿E. myrianthum Stearn等5个品种药用。淫羊藿亦是苗族习用药材之一,在《苗族医药学》、《中国苗族药物彩色图集》等苗药著作中均有收载,苗药名有“锐鸡都”(贵州松桃)、“加俄西”(贵州黔东南)、“弯欧”(黔南)、“毛公堵”(贵州毕节)。自1935年至今,国内外学者已对淫羊藿展开了较为全面的化学成分研究,分离得到以黄酮为主,包括木脂素类、酚苷类、生物碱类、色酮类等上百种化学成分,临床上常用来治疗骨质疏松、股骨头坏死、性功能障碍等疾病[3]。
为了进一步对淫羊藿药用价值进行研究、开发和利用,本文以7种药用淫羊藿为主要对象,对淫羊藿的化学成分、分子鉴定技术和指纹图谱技术在其质量控制中的应用进展进行综述。
1 化学成分 1.1 黄酮类淫羊藿总黄酮有促进免疫调节、抗骨质疏松、抗心肌缺氧、改善心脏血液流变性、促进雄性生殖系统和生殖内分泌功能、抗炎、抗肿瘤、抗衰老等作用[4],是淫羊藿中的主要成分,根据是否具有异戊烯基取代可将其分为2类,最具特征性的异戊烯基取代成分为8-异戊烯基取代黄酮醇及其糖苷,淫羊藿苷为其代表性成分,具有降低动脉粥样硬化患者血栓形成几率及调血脂[5]、促进雌性激素体内生物合成[6]、保护受损神经元及恢复记忆力[7]等药理活性。淫羊藿素能够抑制肿瘤细胞分化[8];淫羊藿苷、淫羊藿素、朝藿定A~C都可显示出一定的雌激素活性[9, 10]。此外,孙朋悦等[11]从朝鲜淫羊藿中分离得到银杏双黄酮、异银杏双黄酮、白果素3个双黄酮类化合物;王明权等[12]从心叶淫羊藿中分离得到2种酮类化合物:1, 3, 5, 8-四羟基酮和1-羟基-3, 4, 5-三甲氧基酮;Li等[13]从巫山淫羊藿中分离得到甘草查耳酮A和甘草查耳酮B 2种查耳酮类化合物。淫羊藿中所含黄酮成分及其结构见图 1、2和表 1。
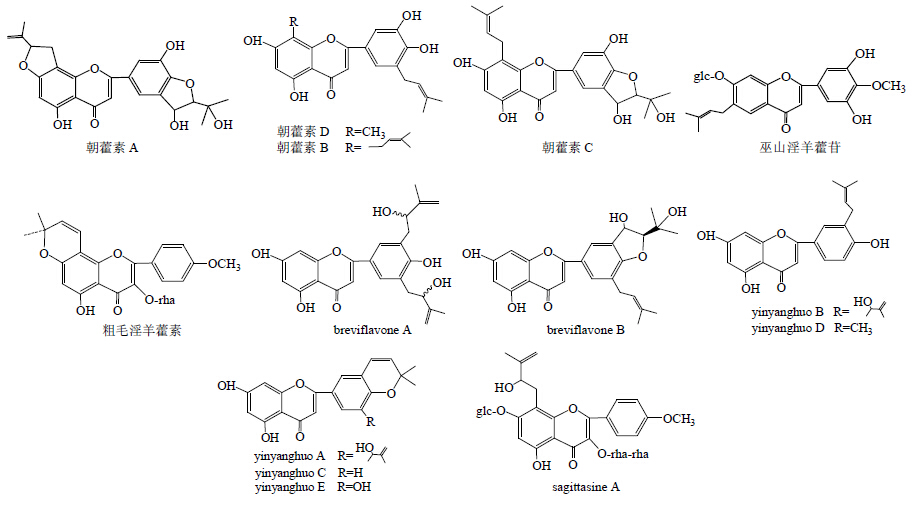 | 图 1 淫羊藿属植物中部分黄酮类化合物的结构Fig.1 Structures of some flavonoids in plants of Epimedium Linn. |
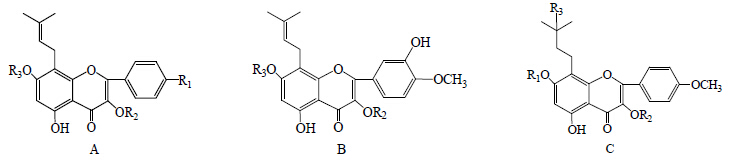 | 图 2 淫羊藿属植物黄酮类化合物母核结构Fig.2 Parent nucleus structures of flavonoids in plants of Epimedium Linn. |
| 表 1 淫羊藿属植物中的黄酮类化合物 Table 1 Flavonoids isolated from plants of Epimedium Linn. |
研究显示,淫羊藿中的木脂素类成分对大鼠骨肉瘤细胞UMR106的增殖及碱性磷酸酶具有一定的促进作用[67]。近年来,不断有木脂素类成分从淫羊藿属植物中被发现,Hiroyuri等[68]从箭叶淫羊藿中分离得到4种木脂素icariside E6、icariside E7、icariol A1、icariol A2。Wang等[25]首次从箭叶淫羊藿中分离鉴定得到6种黄酮木脂素类化合物hydnocarpin、5″-methoxyhydnocarpin、hydnocarpin- D、5′-methoxyhydnocarpin-D、5′,5″-dimethoxyhydno- carpin-D及lignan(+)-dihydro-dehydrodiconiferyl alcohol-4-O-β-D-glucopyranoside。杨云等[69]从心叶淫羊藿中分离得到 (7R, 8S, 8′R)-4, 4′, 8′, 9-四羟基- 3, 3′-二甲氧基-7, 9′-单环氧木脂素和 (7R, 8S)-4, 9-二羟基-3, 3′-二甲氧基-7, 8-二氢苯并呋喃-1′-丙醇基新木脂素-9′-O-α-L-鼠李糖苷。江芳等[67]从朝鲜淫羊藿中分离出柏木苷C、柏木苷A、(+)-南烛木树脂酚、(+)-异落叶松树脂醇。心叶淫羊藿[69]和朝鲜淫羊藿[49]中均含有 (+)-环橄榄树脂素。Li等[70]从朝鲜淫羊藿中分离得到 (+)-cycloolivil formaldehyde condensate、(−)-olivil monoacetate、(−)-(7R, 8S)- dihydrodehydro-diconiferyl alcohol。
1.3 多糖淫羊藿多糖安全可靠,现代研究表明其具有刺激细胞免疫应答、激活胸腺免疫功能的作用,是重要的免疫刺激剂,并通过增强机体免疫功能延缓机体衰老。此外,淫羊藿多糖还具有一定的抗病毒、促进个体激素分泌、促进核酸和蛋白质代谢及血小板凝聚作用[71]。李德耀[72]从淫羊藿多糖部位分离纯化得到10个组分,相对分子质量为122~656 679,质量分数最高的组分达到97.97%,相对分子质量70 374,由α-半乳糖醛酸组成。饶金华等[73]通过柱前衍生化高效液相色谱法分析1个淫羊藿多糖的组成为甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖(摩尔比0.60∶0.74∶1.00∶0.29∶2.29∶1.43)。安晓娟等[74]从淫羊藿中分离得到2个杂多糖成分,1个由鼠李糖、葡萄糖构成,1个由果糖、葡萄糖,以及1个不确定糖。
1.4 生物碱目前在淫羊藿中共分离得到3种生物碱。1957年,日本学者首次从淫羊藿属植物中分离得到木兰花碱,后续研究表明国内淫羊藿中也含有木兰花碱,在淫羊藿主要药用品种中,以朝鲜淫羊藿中木兰花碱的量最高,粗毛淫羊藿和天平山淫羊藿次之,量一般高于0.07%。刘春明等[75]从朝鲜淫羊藿中分离得到淫羊藿碱A;Zhang等[76]从朝鲜淫羊藿中分离得到生物碱epimediphine,并证实该生物碱具有较强的乙酰胆碱酯酶抑制作用。
1.5 苯酚苷淫羊藿中含有icariphenol[48]、毛柳苷[35, 45]、4- hydroxy-2-prenylpheno-1-O-β-D-glucopyranoside[48]。程岩等[77]从朝鲜淫羊藿中分离得到icariside A5;从黔岭淫羊藿中分离得到thalictoside[34]。
1.6 挥发油王丹红等[78]采用传统的水蒸气蒸馏法从巫山淫羊藿中提取到36种挥发油成分,主要为羧酸类、酮类、醇类、炔类。施启红等[79]从柔毛淫羊藿和朝鲜淫羊藿中分别得到66和38个挥发油成分,其中,二者共有成分为28个,以长链脂肪酸、不饱和醇及烃类居多。回瑞华等[80]用超临界流体萃取法从箭叶淫羊藿中提取得到43个挥发油成分。陆钊等[81]采用加速溶剂萃取法从朝鲜淫羊藿中提取鉴定出挥发油成分共91种。
1.7 微量元素淫羊藿中无机元素的量丰富,罗莉等[82]从四川产8种淫羊藿中均可测得16种无机元素,以Ca、K、Mg等6种元素的平均量最高;炮制会引起淫羊藿中无机元素量的变化,如羊脂炙法炮制朝鲜淫羊藿后可增强微量元素的溶出量,其中与肾功能有密切关系的Ca、Mn、Fe、Mg、Zn等微量元素的量明显增加[83]。也有研究显示,多种炮制手段均会使巫山淫羊藿中Fe的量有所降低[84],因此,炮制对淫羊藿中无机元素的量到底有何影响还有待进一步的研究。
1.8 其他淫羊藿中还含有色原酮、菲、蒽醌、鞣质、倍半萜、甾醇等成分。从箭叶淫羊藿中分离得到6-去氧甲基茵陈色原酮[25]、6-去氧甲基-7-甲基茵陈色原酮、6-去氧甲基-4′-甲基-8-异戊烯基茵陈色原酮、6-去氧甲基-7-异戊烯基茵陈色原酮[85]、绿原酸、香豆酸[25]、大黄素、1, 5-二羟基-3-甲氧基-7-甲基蒽醌[17]。从朝鲜淫羊藿中分离得到菲类成分epimedoicarisoside A[30](icariside A1)、淫羊藿苷A7[86],倍半萜类化合物淫羊藿次苷F[77]、淫羊藿次苷C1[46],麦芽酚[49];淫羊藿中还含有胡萝卜苷、β-谷甾醇、肌醇、6, 22-二羟基何柏烷等化学成分。
2 质量控制 2.1 显微鉴定淫羊藿的显微鉴定专属性较强,一般集中在对叶表面特征、花粉、腺毛、非腺毛等方面鉴别特点的研究,尤其是非腺毛更具有种的专属性[87];舒抒等[88]对巫山淫羊藿、粗毛淫羊藿、柔毛淫羊藿等药材粉末的显微特征进行了研究,指出非腺毛长度、直径、毛壁厚度及叶表皮细胞形态等特征可用于种间鉴别。
2.2 分子生物学鉴定DNA条形码概念由加拿大动物学家Hebert提出,是使用通用且相对较短的DNA片段对物种进行快速鉴定的技术,并被逐渐应用到中药鉴定中。郭宝林等[89]采用来源于3个基因组的9个DNA片段序列,通过对比种间序列变异率、构建系统发育树、考察特异性基因位点的方法对市场上常见的8种淫羊藿进行鉴别,仅能实现朝鲜淫羊藿与其他7种淫羊藿的区分。在此基础上,王川易等[90]利用ITS上的特异性位点设计并筛选出2对引物组合,使其对朝鲜淫羊藿进行特异性扩增,实现朝鲜淫羊藿的快速鉴别。Jiang等[91]对psbA-trnH、ITS、rbcL、matK 4个序列在10种淫羊藿37个样品中的扩增效率、种间差异性及barcoding gap等性质进行评价,认为psbA-trnH序列或可作为潜在的鉴别序列。综上所述,朝鲜淫羊藿与其他种淫羊藿亲缘关系较远,通过DNA条形码可实现与其他几种淫羊藿的鉴别,而其他淫羊藿间的亲缘关系较近,迄今关于淫羊藿分子方面的研究中所给出的序列在淫羊藿属植物中均显示出较小的遗传变异率,即种间序列变异与种内序列变异间无明显差异,不能用于鉴定,因此,找到能够将1种或几种淫羊藿(除朝鲜淫羊藿外)从其他的淫羊藿属植物中区分鉴别开的DNA条形码序列是今后淫羊藿DNA条形码技术的研究重点。
2.3 指纹图谱技术《中国药典》2010年版中以淫羊藿苷和总黄酮(巫山淫羊藿以朝藿定C为指标成分,无总黄酮定量测定)为指标性成分对淫羊藿的质量进行控制,然而,不同来源的淫羊藿所含化学成分类别及其量在种内和种间均存在着显著的差异,仅针对单一指标成分或总黄酮不能有效地评价其化学品质。中药指纹图谱能全面、综合地反映中药的化学成分及其量的分布状况,特征性明显,专属性强,信息量丰富,在对几种成分进行定量分析的同时,还能够通过其图谱的特征峰群对药材进行来源鉴定,是一种实现对中药多组分、多指标分析的理想方法。
目前,淫羊藿的指纹图谱多采用反相高效液相色谱法(RP-HPLC),黄酮苷类成分为淫羊藿中的主要成分,其紫外最大吸收在269~274 nm,因此多采用270 nm作为检测波长;流动相采用乙腈-水系统梯度洗脱,得到色谱峰数目多、分离度好,在水中加入一定比例(0.1%~0.5%)的甲酸或冰醋酸可抑制解离,改善峰拖尾。黄朝瑜等[92]首先建立了淫羊藿黄酮类成分的指纹图谱,得到7个共有峰,精密度、稳定性及重复性良好;王丽霞等[93]建立了秦岭山区产3种淫羊藿的指纹图谱,标出9种共有成分。
易中宏等[94]和张萍等[95]分别比较了巫山、朝鲜、箭叶淫羊藿不同生长部位的指纹图谱,证实不同生长部位化学成分差异显著,叶片所含化学成分种类及其量均高于其他部位,为淫羊藿以叶入药给出了依据,并提示应注意对市场上淫羊藿药材质量加以控制,如茎在药材中比例过高则会降低药材品质。
指纹图谱可以显示淫羊藿在炮制前后化学成分的变化,谭鹏等[96]对比炮制前后巫山淫羊藿指纹图谱,发现巫山淫羊藿在炮制后朝藿定C的峰面积减小,而淫羊藿苷的峰面积则有所增加。朱粉霞等[97]比较了朝鲜淫羊藿和柔毛淫羊藿炮制前后指纹图谱,发现二者在炮制前后指纹图谱有5处发生了变化;由此再结合药理研究,可以为阐释炮制机制提供依据。
不同品种间淫羊藿指纹图谱具有显著差异,可用于淫羊藿药材种类的鉴别,郭宝林等[98]将淫羊藿指纹图谱分为4个特征区,其中第2特征区主要由朝藿定A、朝藿定B、朝藿定C、淫羊藿苷4个色谱峰构成,简称为“ABCI”组峰。宋剑等[99]建立了3个品种(巫山淫羊藿、朝鲜淫羊藿、柔毛淫羊藿)淫羊藿指纹图谱,显示“ABCI”组峰中各峰分离度良好,各峰的组成和峰面积在种内较稳定,种间差异明显,能为淫羊藿药材的鉴别和质量控制提供有效依据。裴丽宽[100]分析8种药用淫羊藿指纹图谱,显示朝鲜淫羊藿具有可区别于其他种淫羊藿的独立特征峰,可作为鉴别依据,淫羊藿、粗毛淫羊藿也显示出具有可区分性的指纹特征,而巫山淫羊藿和箭叶淫羊藿种内图谱一致度低;“ABCI”组峰既是淫羊藿指纹图谱特征峰,同时又代表了淫羊藿的主要药效成分。Xie等[101]据此提出了“药效组分分类法”,认为具有相似“ABCI”组峰结构的药材即具有相似的药理活性,在应用中可归为一类,以简化淫羊藿质量控制的复杂度并可作为扩大药源的依据。
随着色谱技术的发展,一些新的色谱技术也被逐步应用到淫羊藿指纹图谱中。朱粉霞等[97]以UPLC法分别建立朝鲜淫羊藿和柔毛淫羊藿指纹图谱,朝鲜淫羊藿标出35个共有峰,柔毛淫羊藿标出13个共有峰,二者相似度均大于92%,且该法分析时间短、分离度高、重现性良好。HPLC-MS联用技术可对指纹图谱中的色谱峰进行结构辨认,进一步增强指纹图谱的特征性。窦建鹏等[102]建立了长白山区朝鲜淫羊藿高效液相色谱指纹图谱,检出13个共有峰,并通过HPLC-MS联用技术对13个峰进行了结构确认,其中11个为黄酮类成分,2个为生物碱类成分。
3 结语淫羊藿中含有丰富的化学成分并具有广泛的药理作用,现已被开发成多种成方制剂,如仙灵骨葆系列、益肾灵颗粒、益肾壮骨颗粒等,临床应用广且具有极大的开发潜力。然而,研究表明品种及生境因素对淫羊藿中化学成分的种类及其量均有较大的影响,直接影响了淫羊藿的临床疗效,《中国药典》2010年版中对淫羊藿的分类可能会降低淫羊藿的资源利用度,可根据淫羊藿所含的主要药效成分的类别及其量对淫羊藿的分类进行细化,将成分相似的淫羊藿等同使用[101],在提高淫羊藿资源利用度的同时还可以寻找并扩大药源;在淫羊藿中,除淫羊藿苷外,仍有多种成分具有较强的药理作用,仅将淫羊藿苷或朝藿定C作为质控指标不能全面地评价淫羊藿的整体药效,因此可以在指纹图谱的基础上结合“一测多评”技术,建立淫羊藿多指标成分控制的方法,以满足其复杂成分的质量控制需要;栽培品与野生品在药材品质上具有一定的差异,这种差异是否在临床使用的可接受范围内、如何控制栽培环境降低这种差异还需要进一步的观察和研究以实现栽培资源与野生资源的对接,从而解决野生资源的过度开发问题,并提高淫羊藿药材的稳定性和质量可控性;在淫羊藿中可检出重金属及有害元素,且某些产地样品中重金属及有害元素量较高[82],而《中国药典》中还没有关于淫羊藿中重金属及有害元素的限量标准,应考虑研究并建立相关评价标准,且栽培基地的选择也应注意排除当地土壤水质的影响。随着对淫羊藿的不断深入的研究,相信能够更好地实现对淫羊藿药材资源的可持续利用。
| [1] | 冉懋雄, 魏德生, 王晓春, 等. 贵州产淫羊藿资源与质量考察研究 [J]. 现代中药研究与实践, 2004, 18(1): 29-32. |
| [2] | 甘井山, 马 艳, 王宗艳, 等. 淫羊藿中化学成分的UPLC/Q-TOF-MS分析 [J]. 现代药物与临床, 2014, 29(4): 349-352. |
| [3] | 张华峰, 杨晓华. 淫羊藿的生物活性成分及其开发策略研究 [J]. 中草药, 2010, 41(2): 329-332. |
| [4] | 张玉萱, 徐玲玲. 淫羊藿总黄酮的药理作用研究进展 [J]. 实用临床医药杂志, 2012, 16(9): 125-128. |
| [5] | Zhang W P, Bai X J, Zheng X P, et al. Icariin attenuates the enhanced prothromboticState in atherosclerotic rabbits independently of its lipid-lowering effects [J]. Planta Med, 2013, 79(9): 731-736. |
| [6] | Yang L J, Lu D F, Guo J J, et al. Icariin from Epimedium brevicornum Maxim promotes the biosynthesisof estrogen by aromatase (CYP19) [J]. J Ethnopharmacol, 2013, 145(3): 715-721. |
| [7] | Li F, Gong Q H, Wu Q, et al. Icariin isolated from Epimedium brevicornum Maxim. attenuates learning and memory deficits induced by D-galactose in rats [J]. Pharmacol Biochem Behav, 2010, 96(3): 301-305. |
| [8] | Tong J S H, Zhang Q H, Huang X, et al. Icaritin causes sustained ERK1/2 activation and induces apoptosis in human endometrial cancer cells [J]. PLoS One, 2011, 6(3): 1-10. |
| [9] | Kang H K, Choi Y H, Kwon H, et al. Estrogenic/antiestrogenic activities of a Epimedium koreanum extractand its major components: in vitro and in vivo studies [J]. Food Chem Toxicol, 2012, 50(8): 2751-2759. |
| [10] | Islam M N, Kim U, Kim D H, et al. High-performance liquid chromatography-based multivariate analysis to predict the estrogenic activity of an Epimedium koreanum extract [J]. Biosci Biotechnol Biochem, 2012, 76 (5): 923-927. |
| [11] | 孙朋悦, 徐 颖, 文 晔, 等. 朝鲜淫羊藿的化学成分 (IV) [J]. 中国药物化学杂志, 1998, 8(2): 122-126. |
| [12] | 王明权, 彭 昕, 甘祺锋. 心叶淫羊藿的化学成分研究 [J]. 现代中药研究与实践, 2005, 19(2): 39-42. |
| [13] | Li H F, Guan X Y, Yang W Z, et al. Antioxidant flavonoids from Epimedium wushanense [J]. Fitoterapia, 2013, 83(1): 44-48. |
| [14] | 李文魁, 肖培根, 廖矛川, 等. 朝藿甙E的分离和结构 [J]. 高等学校化学学报, 1995, 16(12): 1892-1895. |
| [15] | 张红飞, 闫利华, 张启伟, 等. 柔毛淫羊藿叶黄酮类成分研究 [J]. 中国中药杂志, 2013, 38 (12): 1942-1946. |
| [16] | Li W K, Zhang R Y, Xiao P G. Flavonoids from Epimedium wanshanense [J]. Phytochemistry, 1996, 43(2): 527-530. |
| [17] | 崔祥龙, 邓玲玲, 黄胜阳. 箭叶淫羊藿三氯甲烷部位化学成分研究 [J]. 中国实验方剂学杂志, 2010, 16(13): 101-103. |
| [18] | 郭洪利, 王敏杰, 郑 金, 等. 心叶淫羊藿化学成分研究 [J]. 中国药学杂志, 2006, 41(14): 1060-1062. |
| [19] | 梁海锐, 阎文玟, 李 良, 等. 粗毛淫羊藿的化学成分研究 [J]. 中国中药杂志, 1993, 18(11): 677-679. |
| [20] | 崔祥龙, 黄胜阳. 箭叶淫羊藿黄酮类化学成分研究 [J]. 哈尔滨商业大学学报: 自然科学版, 2011, 27(1): 17-20. |
| [21] | Yuji I, Fusayoshi H, Keiichi S, et al. Three flavonol glycosides from Epimedium koreanum [J]. Phytochemisty, 1988, 27(3): 911-913. |
| [22] | 韩 冰, 沈 彤, 鞠建华, 等. 黔岭淫羊藿的化学成分研究 I [J]. 中国药学杂志, 2002, 37(5): 333-335. |
| [23] | 贾宪生, 吴家其, 茅 青. 粗毛淫羊藿根的化学成分研究 (II) [J]. 中国中药杂志, 1998, 23(12): 737-739. |
| [24] | Jiang F, Wang X L, Wang N L, et al. Two new flavonol glycosides from Epimedium koreanum Nakai [J]. J Asian Nat Prod Res, 2009, 11(5): 401-409. |
| [25] | Wang G J, Tsai T H, Lin L C. Prenylflavonol, acylatedflavonol glycosides and related compounds from Epimedium sagittatum [J]. Phytochemistry, 2007, 68(19): 2455-2464. |
| [26] | Sun P Y, Ye W, Zhang G F, et al. A new flavonal glycoside, epimedin K, from Epimedium koreanum [J]. Chem Pharm Bull, 1996, 44: 446-447. |
| [27] | Sun P Y, Chen Y J, Noriko S, et al. Studies on the consitituents of Epimedium koreanum III [J]. Chem Pharm Bull, 1998, 46: 355-358. |
| [28] | Li W K, Xiao P G, Tu G Z, et al. Flavonal glycosides from Epimedium koreanum [J]. Phytochemistry, 1995, 38(1): 263-265. |
| [29] | Li Y S, Liu Y L. Flavonol glycosides from Epimedium wushanense [J]. Phytochemisty, 1990, 29(10): 3311-3314. |
| [30] | Li W K, Pan J Q, Lv M J, et al. A 9, 10-dihydrophenanthrene derivate from Epimedium koreanum [J]. Phytochemistry, 1995, 39(1): 231-233. |
| [31] | Liang H R, Li L, Yan W M. New flavonal glycoside from Epimedium acuminatum [J]. J Nat Prod, 1993, 56(6): 943-945. |
| [32] | 阎文玫, 符 颖, 马 艳, 等. 心叶淫羊藿黄酮类化学成分研究 [J]. 中国中药杂志, 1998, 23(12): 735-736. |
| [33] | 杨 云, 张寒娟, 贺海花, 等. 心叶淫羊藿化学成分研究 [J]. 中草药, 2009, 40(7): 1026-1030. |
| [34] | 程 岩, 王乃利, 王新峦, 等. 朝鲜淫羊藿的化学成分 [J]. 沈阳药科大学学报. 2006, 23 (10): 644-647. |
| [35] | Mizuo M, Norio S, Sakura H, et al. Flavonal glycosides from Epimedium sagittatum [J]. Phytochemistry, 1988, 27(11): 3641-3643. |
| [36] | 李文魁, 张如意, 肖培根. 朝鲜淫羊藿化学成分的研究 [J]. 中草药, 1995, 26(9): 453-455. |
| [37] | 韩 冰, 沈 彤, 刘 东, 等. 黔岭淫羊藿化学成分的研究 Ⅱ [J]. 中国药学杂志, 2002, 37(10): 740-742. |
| [38] | 周颖欣, 贾敏鸽, 涂光忠, 等. 巫山淫羊藿根的化学成分研究 [J]. 中草药, 2005, 36(6): 817-818. |
| [39] | 贾宪生, 吴家其, 茅 青. 黔岭淫羊藿化学成分的研究 IV [J]. 中国药学杂志, 1999, 34(7): 442-444. |
| [40] | 贾宪生, 吴家其, 茅 青. 粗毛淫羊藿根的化学成分研究 [J]. 中国中药杂志, 1998, 23 (3): 162-164. |
| [41] | Li N, Song S J, Luo F. Studies of the chemical constituents of Epimedium koreanum Nakai [J]. Asian J Tradit Med, 2006, 1 (3/4): 117-120. |
| [42] | Dou J P, Liu Z Q, Liu S Y. Structure identifliication of a prenylflavonol glycoside from Epimedium koreanum by electrospray ionization tandem mass spectrometry [J]. Anal Sci, 2006, 22(3): 449-452. |
| [43] | Hu B H, Zhou L D, Liu Y L. New tetrasaccharide flavonol glycoside from Epimedium acuminatum [J]. J Nat Prod, 1992, 55(5): 672-675. |
| [44] | Zhang D W, Cheng Y, Zhang J C, et al. Cytotoxic effects of flavonol glycosides and nonflavonoid constituents of Epimedium koreanumon primary osteoblasts [J]. Pharm Biol, 2008, 46(3): 185-190. |
| [45] | Sun P Y, Ye W, Zhao J F, et al. Studies on the consitituents of Epimedium koreanum [J]. Chem Pharm Bull, 1995, 43(4): 703-704. |
| [46] | 李文魁, 肖培根, 廖矛川, 等. 朝藿甙-C的分离和结构 [J]. 高等学校化学学报, 1995, 16(2): 230-233. |
| [47] | 董晓萍, 肖崇厚, 张 蓉, 等. 粗毛淫羊霍化学成分的研究 [J]. 中国中药杂志, 1994, 19(10): 614-615, 639. |
| [48] | 张树军, 郭洪利, 赵树军, 等. 心叶淫羊藿化学成分研究 (II) [J]. 中草药, 2008, 39(3): 325-327. |
| [49] | 郑训海, 孔令义. 朝鲜淫羊藿化学成分研究 [J]. 中草药, 2002, 33(11): 964-967. |
| [50] | Li Y S, Liu Y L. Flavonol glycosides from Epimedium pubescens [J]. J Nat Prod, 1990, 53: 1337-1339. |
| [51] | Li W K, Xiao P G, Zhang R Y. A difuranoflavone from Epimedium koreanum [J]. Phytochemistry, 1995, 38(3): 807-808. |
| [52] | Tu F J, Dai Y, Yao Z H, et al. Flavonol glycosides from Epimedium pubescens [J]. Chem Pharm Bull, 2011, 59(11): 1317-1321. |
| [53] | Zhao H Y, Fan L, Zhou L, et al. 8-(3, 3-dimethylallyl)- substituted flavonoid glycosides from the aerial parts of Epimedium koreanum [J]. Helc Chim Acta, 2007, 90(11): 2186-2195. |
| [54] | Guo B L, Li W K, Yu J G, et al. Brevicornin, a flavonol from Epimedium brevicornum [J]. Phytochemisty, 1996, 41(3): 991-992. |
| [55] | 李文魁, 肖培根, 廖矛川, 等. 朝鲜淫羊藿中一种黄酮醇甙的化学结构 [J]. 高等学校化学学报, 1995, 16(10): 1575-1576. |
| [56] | 李 娜, 宋少江. 朝鲜淫羊藿中的一个新黄酮苷 [J]. 沈阳药科大学学报, 2006, 23(8): 505-506. |
| [57] | 李文魁, 张如意, 肖培根. 朝藿素B和朝藿素C的结构 [J]. 药学学报, 1994, 29(11): 835-839. |
| [58] | 李文魁, 潘景歧, 吕木坚, 等. 朝藿素D的分离和结构 [J]. 药学学报, 1996, 31(1): 29-32. |
| [59] | 梁海锐, 闫文玫, 李家实, 等. 巫山淫羊藿的化学研究 [J]. 药学学报, 1998, 23(1): 34-37. |
| [60] | Chen C C, Huang Y L, Sun C M, et al. New prenylflavones from the leaves of Epimedium sagittatum [J]. J Nat Prod, 1996, 59(4): 412-414. |
| [61] | Yap S P, Shen P, Mark S B, et al. New estrogenic prenyflavone from Epimedium brevicornum inhibits the growth of breast cancer cells [J]. Planta Med, 2005, 71(2): 114-119. |
| [62] | 姚春所, 张新华, 张 伟, 等. 淫羊藿中的新黄酮甙 [J]. 天然产物研究与开发, 2004, 16(2): 101-103. |
| [63] | 胡碧煌, 周立东, 刘永漋. 粗毛淫羊藿甙的分离和结构 [J]. 药学学报, 1992, 27(5): 397-400. |
| [64] | Luo G J, Ci X X, Ren R, et al. Isolation of two new prenylflavonols from Epimedium brevicornum and their effects on cytokine production in vitro [J]. Planta Med, 2009, 75(8): 843-847. |
| [65] | 李文魁, 肖培根, 潘景歧, 等. 朝鲜淫羊藿的化学成分 (III) [J]. 中国药学杂志, 1995, 30(8): 455-457. |
| [66] | 李遇伯, 孟繁浩, 鹿秀梅, 等. 淫羊藿化学成分的研究 [J]. 中国中药杂志, 2005, 30(8): 586-588. |
| [67] | 江 芳, 王新峦, 王乃利, 等. 朝鲜淫羊藿中的木脂素类化合物及其对大鼠骨肉瘤细胞UMR106增殖及分化的影响 [J]. 中草药, 2008, 39(9): 1281-1285. |
| [68] | Hiroyuri M, Toshio M, Akira U. Lignan and terpene glycosides from Epimedium saggittatum [J]. Phytochemitry, 1991, 30(6): 2025-2027. |
| [69] | 杨 云, 张寒娟, 朱振华, 等. 心叶淫羊藿化学成分研究 [J]. 中药材, 2009, 32 (7): 1051-1053. |
| [70] | Li H Z, Luo G J, Li H M, et al. A new aryltetrahydronaphthalene lignan from Epimedium brevicornum [J]. Chin Chem Lett, 2011, 22(1): 85-87. |
| [71] | 杨晓华, 张华峰, 王 瑛. 淫羊藿多糖的功能、提取与开发前景 [J]. 中国食品添加剂, 2008(S1): 184-187. |
| [72] | 李德耀. 淫羊藿多糖的分离纯化结构分析和免疫活性研究 [D]. 郑州: 郑州大学, 2005. |
| [73] | 饶金华, 刘文英, 江佳峪. 柱前衍生化高效液相色谱法分析淫羊藿多糖中单糖的组成 [J]. 时珍国医国药, 2007, 18(2): 366-367. |
| [74] | 安晓娟, 冯 琳, 宋红平, 等. 淫羊藿多糖的分离纯化及结构初步分析 [J]. 生物学杂志, 2012, 29(3): 39-41. |
| [75] | 刘春明, 刘志强, 窦建鹏, 等. 朝鲜淫羊藿中生物碱类新成分的分离提取及结构鉴定 [J]. 高等学校化学学报, 2003, 24 (12): 2215-2217. |
| [76] | Zhang X D, Oh M Y, Kim S, et al. Epimediphine, a novel alkaloid from Epimedium koreanum inhibits acetylcholinesterase [J]. Nat Prod Res, 2013, 27(12): 1067-1074. |
| [77] | 程 岩, 王新峦, 张大威, 等. 朝鲜淫羊藿中的非黄酮类化合物 [J]. 中草药, 2007, 38(8): 1135-1138. |
| [78] | 王丹红, 陈玉婷, 李 飞, 等. 巫山淫羊藿叶中挥发油成分的气相色谱-质谱分析 [J]. 时珍国医国药, 2007, 18(12): 3022-3023. |
| [79] | 施启红, 吕 磊, 李 玲, 等. 运用GC-MS技术对2种淫羊藿挥发性成分的比较分析 [J]. 药学实践杂志, 2011, 29(6): 445-448. |
| [80] | 回瑞华, 侯冬岩, 李铁纯, 等. 萃取淫羊藿挥发油的实验与分析 [J]. 分析试验室, 2005, 24(10): 63-66. |
| [81] | 陆 钊, 高 凯, 潘淑霞, 等. 加速溶剂萃取/气相色谱-质谱法分析朝鲜淫羊藿挥发油成分 [J]. 哈尔滨工业大学学报, 2011(8): 145-148. |
| [82] | 罗 莉, 李 燕, 杨瑞武, 等. 四川不同产地淫羊藿中无机元素的分析测定 [J]. 药物分析杂志, 2011, 31(6): 1045-1049. |
| [83] | 刘春明, 李 丽, 刘志强, 等. 制前后朝鲜淫羊藿化学成分的变化规律研究 [J]. 分析测试学报, 2004, 23(1): 67-69. |
| [84] | 李定芬, 高言明, 李 健, 等. 巫山淫羊藿炮制前后几种微量元素含量变化研究 [J]. 微量元素与健康研究, 2011, 28 (3): 35-36. |
| [85] | Huang Y L, Ou J C, Chen C F, et al. Three new 2-phenoxychromones from the leaves of Epimedium sagittatum [J]. J Nat Prod, 1993, 56(2): 275-278. |
| [86] | 孙朋悦, 文 晔, 徐 颖, 等. 朝鲜淫羊藿的化学成分 [J]. 药学学报, 1998, 33(12): 919-922. |
| [87] | 黄 蘅. 淫羊藿的显微鉴别研究现状 [J]. 中国中医药现代远程教育, 2010, 8(18): 250-251. |
| [88] | 舒 抒, 陈俊华, 钟国跃. 五种淫羊藿粉末的显微鉴别 [J]. 中药材, 2003, 26(11): 781-783. |
| [89] | 郭宝林, 王川易, 肖培根. 中药淫羊藿的DNA分子鉴定研究 [A]//第九届全国药用植物及植物药学术研讨会论文集 [C]. 海口: 中国植物学会药用植物及植物药专业委员会, 2010. |
| [90] | 王川易, 梁 云, 郭宝林, 等. 药用淫羊藿品种的分子鉴定研究—朝鲜淫羊藿的位点特异性PCR鉴定 [J]. 中国中药杂志, 2010, 35(14): 1799-1802. |
| [91] | Jiang Y, Ding C B, Zhang L, et al. Identification of the genus Epimedium with DNA barcodes [J]. J Med Plants Res, 2011, 5(28): 6413-6417. |
| [92] | 黄朝瑜, 赵陆华, 梅玲华, 等. 淫羊藿药材HPLC指纹图谱的研究 [J]. 中国天然药物, 2003, 1(3): 146-148. |
| [93] | 王丽霞, 王超展, 耿信笃. 淫羊藿属药材反相高效液相色谱指纹图谱及质量评估研究 [J]. 化学学报, 2006, 64(6): 551-555. |
| [94] | 易中宏, 郑一敏, 傅善全, 等. 巫山淫羊藿不同部位的高效液相色谱指纹图谱测定 [J]. 时珍国医国药, 2005, 16(5): 377-378. |
| [95] | 张 萍, 孔维军, 鄢 丹, 等. 基于淫羊藿苷测定及HPLC指纹图谱分析的淫羊藿药材质量差异评价 [J]. 中草药, 2010, 41(11): 1901-1904. |
| [96] | 谭 鹏, 于向红, 杨 蕾, 等. 巫山淫羊藿饮片炮制前后HPLC指纹图谱研究 [J]. 药物分析杂志, 2012, 32(4): 592-595. |
| [97] | 朱粉霞, 赵永刚, 贾晓斌, 等. 淫羊藿炮制前后UPLC-PDA-MS的指纹图谱研究 [J]. 化学学报, 2012, 70(5): 635-642. |
| [98] | 郭宝林, 裴利宽, 肖培根. 淫羊藿属植物黄酮类化合物的分类学意义再探 [J]. 植物分类学报, 2008, 46(6): 874-885. |
| [99] | 宋 剑, 李知遥, 贾继明, 等. 不同品种淫羊藿药材的指纹图谱研究 [J]. 现代中药研究与实践, 2010, 24(5): 16-18. |
| [100] | 裴丽宽, 郭宝林, 黄文华. 淫羊藿属主要资源种类的HPLC指纹图谱特征和种类鉴定 [J]. 中国中药杂志, 2008, 33(14): 1662-1668. |
| [101] | Xie P S, Yan Y Z, Guo B L, et al. Chemical pattern-aided classification to simplify the intricacy of morphological taxonomy of Epimedium species using chromatographic fingerprinting [J]. J Pharm Biomed, 2010, 52(4): 452-460. |
| [102] | 窦建鹏, 宋凤瑞, 刘志强, 等. 朝鲜淫羊藿的色谱指纹图谱及液相色谱/电喷雾串联质谱分析 [J]. 化学学报, 2009, 67(22): 2613-2618. |
 2014, Vol. 45
2014, Vol. 45



