2. 中国药科大学, 江苏 南京 210009
2. China Pharmaceutical University, Nanjing 210009, China
药对是复杂方剂的基础单位,研究药对物质基础有助于剖析中药配伍理论及其药理作用机制[1, 2],而中药共煎煮后的化学成分并非各单味药物化学成分的简单相加,其不同之处必然与药对疗效不同于单味药的事实有着本质联系[3, 4],药对是研究中药配伍规律的有效途径。
人参Ginseng Radix(GR)与白术Atractylodis Macrocephalae Rhizoma(AMR)药对,主治脾胃气虚诸证,出自《和剂局方》中的四君子汤,在后世的许多健胃方剂中应用非常广泛,一般用人参10~15 g,白术10~15 g[5, 6]。目前,围绕人参、白术单味药材的物质基础及药理活性研究较多[7, 8],但其配伍后化学成分研究很少,一些文献报道了人参与其他药材配伍的化学成分变化[9, 10],因此本研究以人参、白术这一经典药对为对象,比较人参、白术合煎液与单煎液化学成分及其量的差异,以期从化学成分变化的角度初步揭示人参-白术药对配伍的科学内涵。
1 材料与仪器美国Aglient公司Hypersil ODS(250 mm×4.6 mm,5 μm)型色谱柱;Agilent 1100型高效液相色谱仪,二元梯度泵,自动进样器、柱温箱和VWD检测器,Agilent科技有限公司;AL204型电子分析天平,瑞士Mettler Toledo公司;Aglient 1290液相色谱-质谱联用仪,LC-MS,DAD检测器和Q-TOF 6538质谱仪;Milli-Q超纯水系统,美国Millipore公司。
人参、白术药材由康缘大药房提供,经江苏康缘药业股份有限公司王振中研究员鉴定为五加科植物人参Panax gingseng C. A. Meyer的干燥根和菊科植物白术Atractylodes macrocephala Koidz. 的干燥根茎。甲醇(分析纯)购自南京化学试剂有限公司;乙腈(色谱纯)购自美国Tedia公司;超纯水由Milli-Q超纯水系统制得。白术内酯I(I,批号121127,质量分数≥98%)、白术内酯II(II,批号121220,质量分数≥98%)、白术内酯III(III,批号121105,质量分数≥98%)、人参皂苷Rc(Rc,批号121022,质量分数≥98%)、人参皂苷Rf(Rf,批号121024,质量分数≥98%)对照品购自成都菲普德科技有限公司;人参皂苷Re(Re,批号110754- 201324,质量分数92.7%)、人参皂苷Rb1(Rb1,批号110704-200420,质量分数≥98%)、人参皂苷Rg1(Rg1,批号110703-201128,质量分数98.0%)、人参皂苷Rb2(Rb2,批号111715-201203,质量分数93.8%)、人参皂苷Rd(Rd,批号111818-201202,质量分数94.2%)对照品购自中国食品药品检定研究院。
2 方法与结果 2.1 色谱条件色谱柱为Hypersil ODS(250 mm×4.6 mm,5 μm);流动相为乙腈-水溶液;梯度洗脱:0~35 min, 5%~35%乙腈;35~40 min,35%乙腈保持;40~80 min,35%~95%乙腈;检测波长为203 nm;柱温为25 ℃;体积流量为1 mL/min,进样量为20 μL。
2.2 混合对照品溶液与供试品溶液的制备 2.2.1 对照品溶液的制备精密称定经干燥24 h的I、II、III对照品各5.0 mg,置10 mL的量瓶中,用甲醇溶解并稀释至刻度,制成白术内酯混合对照品储备液,−4 ℃冰箱放置,备用。
精密称定经干燥过的Rd、Rc、Rb1、Rb2、Re、Rg1、Rf对照品各5.0 mg,置10 mL的量瓶中,用甲醇溶解并稀释至刻度,制成人参皂苷混合对照品储备液,−4 ℃冰箱放置,备用。
2.2.2 供试品溶液的制备人参、白术按1∶1(各取50 g)混和后,用10倍量水浸泡60 min后,煎煮2次,每次1 h;合并2次煎煮液,滤过,加水补足至20倍量,即得人参-白术合煎液;制备人参、白术单煎液,方法同上;将2种单煎液按1∶1混合,即为人参-白术合并液。精密量取合煎液、合并液与单煎液各100 mL,至水浴60 ℃挥干后,加入适量50%甲醇溶解后,转移至25 mL量瓶中,加入甲醇至刻度,摇匀,以0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.3 方法学考察 2.3.1 精密度试验取人参、白术合煎供试品溶液,连续进样5次,根据“2.1”项色谱条件测定,选择22个共有峰进行比较,结果表明各色谱峰相对保留时间的RSD均小于1.0%,各色谱峰相对峰面积的RSD均小于2.0%,表明仪器精密度良好。
2.3.2 重复性试验取同一批人参、白术药材按“2.2.2”项供试品溶液制备方法平行操作,制备5份人参-白术合煎供试品溶液,根据“2.1”项色谱条件测定,结果各色谱峰相对保留时间的RSD均小于1.0%,各色谱峰峰面积的RSD均小于3.0%,表明该方法重复性良好。
2.3.3 稳定性试验取同批人参-白术合煎供试品溶液,分别于0、4、8、12、24 h进样测定,对各色谱峰进行比较,结果各色谱峰相对保留时间的RSD均小于1.0%,各色谱峰的峰面积的RSD均小于3.0%,且色谱峰数目无变化,表明样品在24 h内稳定性良好。
2.4 色谱峰归属将人参、白术合煎液与单煎液、人参皂苷混合对照品及白术内酯混合对照品的图谱进行对比,对人参-白术合煎液中各色谱峰进行初步归属,见图 1。通过与混合对照品及人参、白术单煎液各色谱峰的保留时间比较,可知8~14号色谱峰为Rg1、Re、Rf、Rb1、Rc、Rb2、Rd;15、17、18号色谱峰为I、III、II;1、3~5、7、19、20、22号色谱峰为人参、白术共有峰,人参和白术药材中共有化合物较少,该共有峰可能为在此液相条件下出峰位置相同的化合物;2、6、16号色谱峰为人参特有,21号色谱峰为新出现的色谱峰。
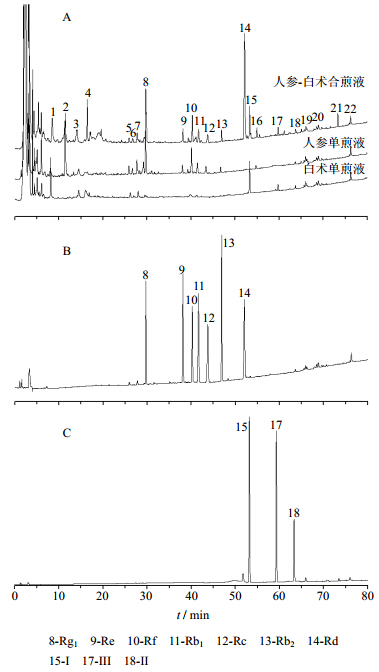 | 图 1 不同煎煮液样品 (A) 和人参皂苷 (B)、白术内酯 (C)混合对照品的HPLC图Fig. 1 HPLC of different decoctions (A), ginsenosides (B), and butenolide (C) reference substances |
将人参-白术合煎液与人参-白术合并液的图谱(图 2)进行比较,合煎液中4、8~10、14、15号色谱峰峰面积明显增加,2号色谱峰面积减少,其他色谱峰面积无明显变化,而合并液图谱中未见21号色谱峰,具体变化见表 1。相关成分变化情况的计算公式为变化比例=(合并液中峰面积-合煎液中峰面积) / 合并液中峰面积。
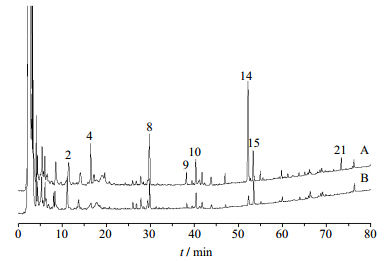 | 图 2 人参-白术合煎液 (A) 与合并液 (B) 的HPLC图Fig. 2 HPLC of GR-AMR co-decoction (A) and GR-AMR mixed decoction (B) |
| 表 1 人参-白术合并液与合煎液化学成分 Table 1 Chemical constituents of co-decoction and mixed decoction of GR and AMR |
质谱测试条件:ESI离子源;离子化方式:ESI (+/−);干燥气温度350 ℃;干燥气流量10 L/min;雾化气压力344.5 kPa;毛细管电压+4 000 V/−3 500 V;毛细管出口电压100 V,锥孔电压65 V;扫描范围m/z 100~1 500。
21号色谱峰浓缩液的质谱分析结果见图 3,其中tR=73.299 min,分子式为C42H70O12,相对分子质量为766.48,分子离子峰m/z: 784.52 [M+NH4]+, 767.49 [M+H]+, 749.48 [M+H-H2O]+, 879.47 [M+TFA-H]−, 811.48 [M+HCOOH-H]−, 765.48 [M-H]−。
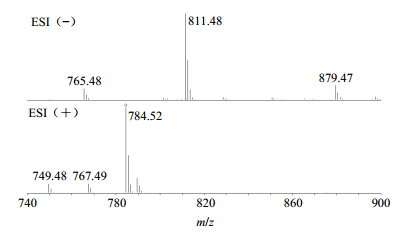 | 图 3 21号色谱峰ESI-MS谱Fig. 3 ESI-MS spectrum of peak 21 |
本实验采用HPLC法,比较了人参与白术药对配伍前后人参皂苷和白术内酯等成分的变化,发现配伍后Rg1、Rd、Re明显增加,Rf、I略有增加,表明2味药材合煎可增加人参皂苷成分及白术内酯等有效成分的提取率。通过合煎液与单煎液HPLC图的对比,发现合煎条件下产生了1个新色谱峰(峰21),而在合并液未见上述变化,表明合煎是导致人参皂苷类成分量增加及化学成分变化的原因,从化学成分变化的角度初步揭示了人参、白术药对配伍的科学内涵,复方化学成分不是各单味药的简单加和,而是发生了变化;这种变化不仅有成分量的变化,也有化学成分种类的变化。
本实验在此基础上运用MS检测出21号峰分子离子峰m/z 767.49 [M+H]+,参考相关文献报道[11]推断该物质为人参皂苷F4或人参皂苷Rg6,由人参皂苷Rg2分解得到。后续可通过LC-MS、NMR等手段对共煎液中新产生的化学成分及未知成分进行辨析,明确共煎液中的主要成分,对其药理作用进
行研究,进一步阐明化学成分与其生物效应之间的关系,并研究不同比例配伍对化学成分的影响,反映其变化规律。还可从吸收、代谢等角度对人参、白术配伍前后进行研究,全面阐明其药对配伍的科学性,揭示药对配伍的科学内涵。
| [1] | 王曼华, 孙化萍, 梁建卫. 经方"药对"配伍理论研究概况 [J]. 辽宁中医药大学学报, 2008, 10(1): 59-60. |
| [2] | 孙 洋, 陈 婷, 徐 强. 从药对的角度考察复方配伍规律 [J]. 世界科学技术—中医药现代化, 2004, 6(1): 17-20. |
| [3] | 吴 笛, 刘法锦, 廖彩震. 中药配伍对化学成分的影响 [J]. 中成药, 2003, 25(1): 152-154. |
| [4] | 原思通, 杜海燕, 夏 冲. 中药复方汤剂分煎合煎对溶出效果的影响 [J]. 中国中医药信息杂志, 1999, 6(7): 29-32. |
| [5] | 王鸿燕. 人参药对功用探析 [J]. 中华中医药学刊, 2009, 27(3): 649-651. |
| [6] | 王 付. 伤寒论现代研究丛书: 经方药对 [M]. 北京: 学苑出版社, 2005. |
| [7] | 黎 阳, 张铁军, 刘素香, 等. 人参化学成分和药理研究进展 [J]. 中草药, 2009, 40(1): 164-附2. |
| [8] | 陈 文, 何鸽飞, 姜曼花, 等. 白术的研究进展 [J]. 中草药, 2008, 39(5): 附4-附6. |
| [9] | 丁选胜, 戴德哉, 汤晓赟. 人参白虎汤配伍规律研究—不同配伍条件下钙离子含量变化 [J]. 中草药, 2004, 35(2): 156-158. |
| [10] | 汤响林, 易剑峰, 梁乾德, 等. 人参-附子配伍比例对人参皂苷成分溶出变化研究 [J]. 中草药, 2013, 1(1): 36-41. |
| [11] | 吴彦君. 人参皂苷Re碱降解产物的成分研究 [D]. 长春: 吉林大学, 2008. |
 2014, Vol. 45
2014, Vol. 45


