龙20 g、珍珠母40 g组成,13味中药中,珍珠母、磁石、当归、钩藤粉碎成细粉,过筛;其余黄芩等9味药加水煎煮2次,第1次3 h,第2次2 h,合并煎液,滤过,滤液减压浓缩成膏,加入珍珠母等细粉,混匀,制成颗粒,干燥,压制成1 000片,包糖衣,即得[1]。由于原清脑降压片中未列入非法添加降压类化学药物的检查和定量测定方法;原清脑降压片补充检验方法仅检测样品中非法添加氢氯噻嗪、盐酸异丙嗪。近年来降压类化学药物氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平等原料药物购买容易,完全可能被不法分子用来添加到清脑降压片等同类中成药中,且目前市场抽检结果显示已出现非法添加功效成分的案例[2, 3],因而有必要建立目前较普及的高效液相色谱测定方法,检测样品中上述5种降压类化学药物的量[4]。
1 仪器与试药AE240电子天平,瑞士Mettler Toledo公司;LC—20A全自动高效液相色谱仪,日本Shimadzu公司。
对照品氢氯噻嗪(批号100309-200702)、盐酸哌唑嗪(批号100164-200402)、盐酸异丙嗪(批号100422-200501)、利血平(批号100041-200311)和硝苯地平(批号100338-200502),所有对照品质量分数均>98%,均由中国食品药品检定研究院提供。甲醇、乙腈为色谱纯,水为重蒸馏水,其余试剂均为分析纯。清脑降压片,吉林福康医药生物科技有限公司,批号081201;河北安国药业集团有限公司,批号106307;湖南省回春堂药业有限公司,批号20090707;青海可可西里药业集团有限公司,批号20100318;西安澜泰药业有限公司,批号20100504;样品均由国家食品药品监督管理局市场监督办发文后,由相关企业提供。
2 方法与结果 2.1 色谱条件十八烷基硅烷键合硅胶为填充剂(APOLLO色谱柱C18:250 mm×4.6 mm,5 μm);以乙腈-0.2%磷酸水溶液进行梯度洗脱:0~10 min,20%~30%乙腈;10~25 min,30%~45%乙腈;25~35 min,45%~20%乙腈;体积流量为1.0 mL/min;柱温25 ℃;检测波长为251 nm,进样量为20 μL。理论塔板数按氢氯噻嗪峰计算应不低于4 000。
2.2 溶液的制备 2.2.1 对照品溶液的制备避光操作。取氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平对照品适量,精密称定,加甲醇制成含氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平各10 μg/mL的溶液,即得[5]。
2.2.2 供试品溶液的制备避光操作。取各厂家提供的清脑降压片内容物,研细,取约0.3 g,精密称定,置50 mL量瓶中,加入甲醇适量,超声处理(功率500 W,频率40 kHz)15 min,放冷,用甲醇稀释至刻度,摇匀,滤过,取续滤液稀释10倍,即得。
2.3 系统适应性试验取混合对照品溶液,注入液相色谱仪中,结果4种对照品理论板数均大于4 000;测得分离度为9.0,拖尾因子为0.97,连续进样5次,重复性试验RSD均小于2.0%,均符合《中国药典》2010年版规定。混合对照品溶液、供试品溶液和添加混合对照品溶液的供试品溶液的色谱图见图 1。
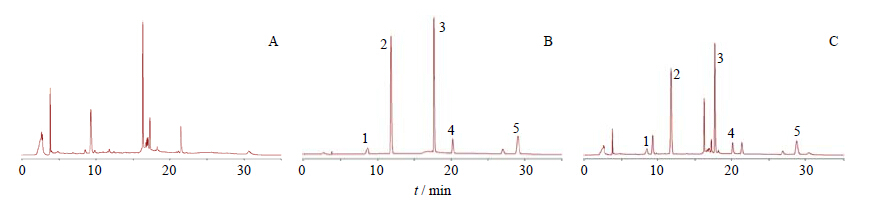 | 1-氢氯噻嗪 2-盐酸哌唑嗪 3-盐酸异丙嗪 4-利血平 5-硝苯地平 1-hydrochlorothiazide 2-prazosin hydrochloride 3-romethazine hydrochloride 4-reserpine 5-nifedipine图 1 供试品 (A)、混合对照品 (B) 和添加混合对照品的供试品 (C) 的HPLC图Fig. 1 HPLC of samples (A),mixed reference substances (B),and samples with mixed reference substances (C) |
避光操作。分别精密称取氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平对照品26.55、20.23、24.65、23.72、28.13 mg,加甲醇定容于50 mL量瓶中,溶解,制成含氢氯噻嗪531.0 μg/mL、盐酸哌唑嗪404.6 μg/mL、盐酸异丙嗪493.0 μg/mL、利血平474.4 μg/mL、硝苯地平562.6 μg/mL的溶液,作为对照品储备液。精密吸取各储备液,加甲醇制成系列浓度的混合对照品溶液。吸取系列浓度的混合对照品溶液各20 μL,注入液相色谱仪,依法测定,计算峰面积积分值(A),以进样量(C,μg)为横坐标,A均值为纵坐标,得回归方程、相关系数分别为氢氯噻嗪:A=742 033.061 6 C-5 158.151 3;R2=1.000 0(n=7);盐酸哌唑嗪:A=7 915 963.722 7 C-18 011.913 6;R2=1.000 0(n=7);盐酸异丙嗪:A=5 318 078.851 2 C-11 963.115 7;R2=1.000 0(n=7):利血平:A=905 053.723 1 C-4 167.185 2;R2=1.000 0(n=7);硝苯地平:A=1 770 098.555 4 C-10 408.571 9;R2=0.999 7(n=7)。结果表明氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平和硝苯地平分别在21.24~2 124.0 ng(r=1.000 0),16.184~1 618.4 ng(r=1.000 0),19.72~1 972.0 ng(r=1.000 0),18.976~1 897.6 ng(r=1.000 0)和22.504~2 250.4 ng(r=1.000 0)范围内有良好线性关系。
2.5 精密度试验精密吸取加入5种对照品的样品(批号081201)溶液20 μL,连续进样6次,测定A值的相对标准偏差(RSD)值。定量测定采用外标曲线法,结果氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平和硝苯地平峰面积的RSD值分别为0.84%、0.30%、0.60%、0.73%和0.78%,表明本法精密度较好。
2.6 稳定性试验实验避光操作。精密吸取加入5种对照品的样品(批号081201)溶液,室温下放置,按上述方法分别于0、1、2、4、10 h,测定其A值,结果氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平和硝苯地平峰面积的RSD值分别为0.80%、0.43%、1.43%、0.17%和0.31%,测定结果表明,样品溶液在10 h内较稳定。
2.7 加样回收率试验实验避光操作。取清脑降压片样品(批号081201)6份,每份约0.3 g,精密称定。分别精密加入含氢氯噻嗪106.2 μg/mL、盐酸哌唑嗪80.9 μg/mL、盐酸异丙嗪98.6 μg/mL、利血平94.9 μg/mL、硝苯地平112.5 μg/mL的混合对照品溶液1.0 mL,置50 mL量瓶中,依法制成供试品溶液[6]。精密吸取含氢氯噻嗪106.2 μg/mL、盐酸哌唑嗪80.9 μg/mL、盐酸异丙嗪98.6 μg/mL、利血平94.9 μg/mL、硝苯地平112.5 μg/mL的混合对照品溶液2.5 mL,置50 mL量瓶中,加甲醇至刻度,摇匀,作为对照品溶液。分别吸取供试品溶液和对照品溶液各20 μL,注入液相色谱仪,依法测定,计算回收率。结果氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平和硝苯地平的平均回收率分别为100.93%(RSD为1.52%,n=6)、101.61%(RSD为1.21%,n=6)、103.07%(RSD为1.08%,n=6)、97.58%(RSD为0.73%,n=6)和96.36%(RSD为0.48%,n=6),表明本法的准确性较好。
2.8 检测限实验避光操作。取混合对照品溶液,加甲醇稀释至适当质量浓度,按上述液相色谱方法,进样2 μL,测定。得信噪比为3时各非法添加成分的检出限,氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平的最低检测限分别为2.2、1.6、2.0、1.8、2.2 ng。
2.9 定量限避光操作。取混合对照品溶液,加甲醇稀释至适当浓度,按上述液相色谱方法,进样5 μL测定。得信噪比为10时各非法添加成分的定量限,氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平的最低定量限分别为5.5、4.0、5.0、4.5、5.5 ng。
2.10 样品测定取5批不同生产企业和批号的清脑降压片,分别按“2.2”项下方法进行处理,按“2.1”项下条件测定,并采用外标曲线法计算各被测成分的量。测定结果为5批样品中均未检出非法添加的氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平。
3 讨论 3.1 检测波长的选择在上述色谱条件下,精密吸取照品溶液20 μL,注入高效液相色谱仪,各色谱峰用PDA检测器在波长200~400 nm进行光谱扫描,盐酸异丙嗪的最大吸收波长在251 nm,盐酸哌唑嗪的最大吸收波长在246 nm,氢氯噻嗪、利血平和硝苯地平在251 nm波长处均有较大吸收,故选择251 nm作为5种降压类化学药物的HPLC检测波长[7]。
3.2 提取溶剂的选择氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平在甲醇中溶解度较好,均比在水中溶解度更好,故选择甲醇作为供试品的提取溶剂。
3.3 流动相的选择实验避光操作。取回收率试验的同一份供试品溶液,参照有关文献报道[8, 9],分别在流动相为不同比例、不同梯度的乙腈-0.2%磷酸水溶液进行不同比例的梯度洗脱,结果表明,选用前述梯度条件,氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平各峰峰形及分离度均较好,清脑降压片样品在相应位置上无干扰。按“2.2”项下方法制备供试品溶液,分别精密吸取供试品溶液20 μL,注入高效液相色谱仪,进行测定,结果表明此流动相条件下样品基本无干扰。
3.4 色谱柱耐用性比较运用不同品牌色谱柱,分别为岛津C18(250 mm×4.6 mm,5 μm)、大连依利特C18(250 mm×4.6 mm,5 μm)、APOLLO色谱柱C18(250 mm×4.6 mm,5 μm),取回收率试验的同一份供试品溶液[12],进样2次测定,在样品色谱图上,氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平各峰在35 min内实验结果表明:岛津C18(250 mm×4.6 mm,ODS-SP,5 μm)与大连依利特C18(250 mm×4.6 mm,5 μm)色谱柱不适用于本法,APOLLO色谱柱C18(250 mm×4.6 mm,5 μm)分离较好,可以运用于该实验。
3.5 柱温箱温度影响取回收率试验的同一份对照品溶液,分别在柱温箱温度为20、25、30、35、40 ℃进样测定。样品色谱图上,在柱温箱温度为20、25、30、35、40 ℃时,氢氯噻嗪、盐酸哌唑嗪、盐酸异丙嗪、利血平、硝苯地平各峰峰形及分离度均较好。其中,氢氯噻嗪、盐酸哌唑嗪、硝苯地平受柱温影响较大;盐酸异丙嗪、利血平受柱温影响较小。结果表明,本法适用的柱温箱温度25~35 ℃。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 朱 健,裘一婧,沈国芳. UPLC-MS/MS法快速检测减肥类保健品中13种非法添加化学成分 [J]. 中草药,2014,45(4):509-515. |
| [3] | 励 炯,沈国芳,朱 建,等. UPLC-MS/MS法测定抗风湿中成药中非法添加8种抗风湿性化学成分 [J]. 中草药,2014,45(18):2647-2651. |
| [4] | 药品检验补充检验方法和检验项目批准件 [S]. 2009032. |
| [5] | 程 正,万 庆,管玉云,等. HPLC法测定复方利血平片中氢氯噻嗪、盐酸异丙嗪和利血平的含量 [J]. 安徽医药,2010,14(1):38-40. |
| [6] | 彭芳玲,阳利龙,龙 荣,等. HPLC测定盐酸异丙嗪糖浆中盐酸异丙嗪的含量 [J]. 儿科药学杂志,2008,14(2):24-26. |
| [7] | 张 莉,田洪斌. HPLC法测定复方利血平片中利血平的含量 [J]. 中国药事,2008,22(11):997-1007. |
| [8] | 杨建林. 复方罗布麻片II中盐酸异丙嗪含量的RP-HPLC法测定 [J]. 安徽医药,2009,13(2):164-165. |
| [9] | 刘桂丽. HPLC法测定珍菊降压片中氢氯噻嗪和芦丁的含量 [D]. 上海:复旦大学,2011. |
| [10] | 娄志红,张秋生,姜连阁,等. HPLC法测定氨酚异丙嗪注射液中盐酸异丙嗪的含量和有关物质 [J]. 中国药事,2013,27(11):1207-1210. |
 2014, Vol. 45
2014, Vol. 45

