知柏地黄丸是由知母、黄柏、熟地黄、山茱萸(制)、牡丹皮、山药、茯苓、泽泻8味药材组成,具有滋阴降火的功效;用于治疗阴虚火旺、潮热盗汗、口干咽痛、耳鸣遗精、小便短赤[1],是常见的中药丸剂。盐酸小檗碱(BH)是黄柏中一种重要的药效成分,具有抗菌、抗炎、抗心律失常、降血糖、调节免疫和抗肿瘤等作用[2]。检测知柏地黄丸中BH的量对药品的质量控制具有十分重要的意义。
BH常用的分析方法有HPLC法、毛细管电泳法、共振光散射光谱法、胶束增稳荧光法等方法[3, 4, 5, 6]。这些方法都需要昂贵的仪器和复杂的前处理过程,因此造成实际测定时间过长,且不能方便地进行实地检测。本实验以BH的分子印迹模板为电活性物质,制备出BH选择性电极,用于测定知柏地黄丸中BH的量。
1 仪器与材料pH S—3C型精密酸度计,上海理达经贸有限公司;LC—20AT高效液相色谱仪,日本岛津公司;PXSJ—216型离子活度计,上海雷磁仪器厂;08—3G恒速磁力搅拌器,上海梅颖浦仪器仪表制造有限公司;KQ—250DB超声波清洗器,昆山市超声仪器有限公司。
BH原料药,上海华硕精细化学品有限公司,质量分数98.8%,批号20110322;BH对照品,中国食品药品检定研究院,质量分数≥98.0%,批号110713-200609;甲基丙烯酸(MAA)、乙二醇二甲基丙烯酸酯(EGDMA)、4-乙烯基吡啶、丙烯酰胺(AM)、聚氯乙烯(PVC)、偶氮二异丁腈(AIBN)购于阿拉丁试剂有限公司;邻苯二甲酸二丁酯(DBP)购于天津科密欧试剂有限公司;知柏地黄丸大蜜丸(批号130808、130809、130810)和浓缩丸(批号131002、131003、131004)购于当地药店,河南省宛西制药股份有限公司生产;甲醇为色谱纯,其余试剂均为分析纯,水为二次蒸馏水。
2 方法与结果 2.1 BH对照品溶液的配制称取40.8 mg的BH对照品,用200 mL的二次蒸馏水煮沸溶解,放冷,加入10 mL pH 4.0的0.1 mol/L醋酸缓冲溶液,定量转移至1 000 mL的量瓶中,用二次水定容,得0.1 mmol/L BH溶液,逐级稀释得一系列BH对照品溶液。
2.2 BH分子印迹模板的制备 2.2.1 功能单体的选择为提高BH分子印迹模板对BH测定的选择性,分别考察了AM、MAA、4-乙烯基吡啶作为功能单体制备的分子印迹模板对BH的结合常数分别为3.26、6.35、0.72 nmol/g。结果表明,采用MAA作为功能单体,结合常数最大,则制备的电极灵敏度和选择性最佳,所以选择MAA为功能单体。
2.2.2 各种原料比例的确定按照文献报道[7]的结论,目标分子-功能单体-交联剂的比例1∶4∶40为最佳,但由于BH的溶解度较小,在此体积中1 mmol的BH无法完全溶解,以此减少BH的量,至10 μmol时呈现良好的溶解性,所以选择BH的用量为10 μmol。
2.2.3 BH分子印迹模板的制备称取BH 10 μmol、MAA 5 mmol,溶于8 mL四氢呋喃中,超声30 min后加入EGDMA 20 mmol、20 mg AIBN,再超声处理10 min,通入氮气除氧10 min,密封反应器,在氮气保护下60 ℃水浴反应24 h,得黄色块状聚合物。经研钵研磨,过200目筛,得粒径小于74 μm的分子印迹聚合物(MIP)。将此聚合物用60 ℃二次蒸馏水反复多次洗涤滤过,至滤液用紫外分光光度计检测不出BH为止。聚合物经丙酮反复沉降后除去细颗粒,60 ℃下干燥至恒定质量,得BH分子印迹模板。同时制备不加BH的空白对照和不进行洗涤的MIP。
2.3 BH分子印迹-玻璃涂层离子选择性电极的制备将玻璃电极在蒸馏水中浸泡48 h,用二次蒸馏水冲洗干净,再用无水乙醇冲洗,吹干待用。
称取PVC粉0.20 g,用10 mL四氢呋喃溶解,再加BH分子印迹模板30 mg,DBP 0.20 mL,超声处理,使其分散均匀。将上述玻璃电极浸入到该液体中,缓慢取出,晾干后再浸入,如此反复多次,使玻璃电极表面均匀涂敷一层PVC膜,此即BH分子印迹-玻璃涂层电极。
2.4 电池电动势测量方法先将电极在0.1 mmol/L的BH溶液中浸泡活化2 h,用水冲洗后与饱和甘汞电极组成测量电池,连接离子活度计,测量双蒸水的空白电动势(E),待其稳定后即可测定待测液的电池E。测定一个溶液后用0.4%的NaOH溶液冲洗电极后再测定下一溶液,最后用标准曲线法测定知柏地黄丸中BH的量。
2.5 pH值的选择用HCl和NaOH溶液调节10 μmol/L的BH溶液的pH值,测量溶液在不同pH值下的E,作E-pH曲线。由图 1可知,当BH溶液pH值在2.6~5.4,E变化较小。为了便于控制溶液的pH值,选择pH 4.0作为测定溶液的pH值。
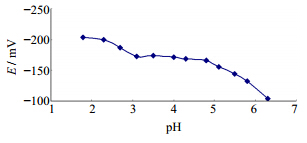 | 图 1 pH值的影响Fig. 1 Effectof pH value on electrode response |
依次测量BH浓度在0.1~100 μmol/L对照溶液的E,以E对BH溶液浓度的负对数(pC)做图,结果见图 2。BH的浓度在1~100 μmol/L,E-pC具有良好的线性关系,该曲线的线性方程为E=55.48 pC-446.09。Nernst响应斜率为55.48 mV/pC,r=0.999 2,检测限为0.561 μmol/L。
2.7 专属性试验采用独立溶液法测定一些常见的阴阳离子和知柏地黄丸中共存生物碱的选择性系数(Kij,为待测离子与干扰离子同电位时活度的比值),用以考察该方法的专属性,结果见表 1。常见的阴阳离子和知柏地黄丸中共存的其他生物碱对测定无显著性干扰,证明专属性良好。
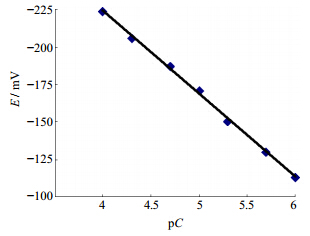 | 图 2 电极响应曲线Fig. 2 Response curve of electrode |
在制备工作曲线时,测定12次对照品溶液的E值,结果表明,所有对照品溶液E值的RSD均小于2.6%。
2.9 稳定性试验分别取知柏地黄丸大蜜丸和浓缩丸各20丸,研磨均匀,精密称取5 g用100 mL蒸馏水煮沸15 min后,趁热滤过并洗涤,合并滤液放冷,转移于250 mL量瓶中,加入2.5 mL pH 4.0醋酸缓冲液后用二次蒸馏水定容,得供试品溶液。室温放置,分别于0、2、
| 表 1 Kij测定结果 Table 1 Result of selective coefficient detection Kij |
4、6、8、12 h测定供试品溶液的E值,结果表明E的RSD为2.7%和3.1%,证明供试品溶液在12 h内稳定。
2.10 重复性试验分别取3批知柏地黄丸大蜜丸和浓缩丸,按“2.9”项所述方法制备供试品溶液,平行测定6次,RSD分别为0.67%、0.76%、0.62%和0.89%、0.92%、0.98%。结果表明该方法重复性良好。
2.11 电极的响应时间和使用寿命根据国际纯粹与应用化学联合会(IUPAC)的推荐,测试电极在100、10、10、1 μmol/L的BH溶液中的静态响应时间,结果表明该电极的静态响应时间均小于50 s。
检测所制备的电极在3个月内的Nernst响应性能,结果表明,试验期间电极的响应性能无显著性变化。则电极使用寿命大于3个月。
2.12 回收率试验分别取3个批次的知柏地黄丸大蜜丸和浓缩丸各20丸,研磨均匀,精密称取5 g,准确加入一定质量的BH原料药,用100 mL蒸馏水煮沸15 min后,趁热滤过并洗涤,合并滤液放冷,转移于250 mL量瓶中,加入2.5 mL醋酸缓冲液后用二次蒸馏水定容,按“2.4”项方法进行测定,进行回收率试验,结果见表 2,表明回收率良好。
2.13 样品的测定按“2.9”项方法制备供试溶液,按“2.4”项方法进行测定,并同时用《中国药典》2010年版方法进行对照。由表 3可知,测定结果准确度较为满意。
| 表 2 回收率试验 (n = 6) Table 2 Test of recoveryrate (n = 6) |
| 表 3 测定结果 (n = 6) Table 3 Results of determination (n = 6) |
采用分子印迹模板作为电活性物质制备了离子选择性电极,结果表明,测定的选择性和灵敏度有了一定程度的提高,但检测的上限较传统电活性物质制备的电极低,可能因为BH的溶解性较差,制备的分子印迹模板吸附量小所致。
分子印迹聚合物在制备之前,需对试剂进行纯化处理,除去试剂中所含的阻聚剂,能够显著提高分子印迹模板的吸附量。在离子选择性电极制备时要避免水分的引入,如果有微量水引入即能造成电极响应性能显著下降,甚至无明显的响应。
分子印迹聚合物因为对目标物具有良好的选择吸附性,被广泛应用于复杂基体中痕量和超痕量组分的分离和检测[8, 9, 10]。本方法相比于色谱法具有较大的优势,样品处理简单,无有机溶剂,测定速度快。但长期使用稳定性不够满意,所以在以后的研究中应加强稳定性的研究,使其能够商品化。
| [1] | 韩 磊, 宋艳丽. 知柏地黄丸的药理作用和临床应用研究进展 [J]. 中国药房, 2012, 23(15): 1430-1432. |
| [2] | 郑洪艳, 徐为人. 小檗碱药理作用研究进展 [J]. 中草药, 2004, 35(6): 113-116. |
| [3] | 易 博, 孙 赫, 原 源, 等. RP-HPLC法测定知母黄柏药对中新芒果苷、芒果苷和盐酸小檗碱 [J]. 中草药, 2007, 38(6): 856-858. |
| [4] | 孔 玲, 刘绍璞, 周贤杰. 同多钼酸根共振瑞利散射光谱法测定盐酸小檗碱 [J]. 西南师范大学学报: 自然科学版, 2003, 28(2): 252-257. |
| [5] | 王秀林, 张丽君, 刘 康, 等. 盐酸小檗碱含量测定的荧光新方法研究 [J]. 分析测试学报, 2012, 31(3): 322-326. |
| [6] | Geto A, Pita M, De Lacey A L, et al. Electrochemical determination of berberine at a multi-walled carbon nanotubes-modified glassy carbon electrode [J]. Sensor Actuat B-Chem, 2013, 183(5): 96-101. |
| [7] | Li N, Ng T B, Wong J H, et al. Separation and purification of the antioxidant compounds, caffeic acid phenethyl ester and caffeic acid from mushrooms by molecularly imprinted polymer [J]. Food Chem, 2013, 139(1/4): 1161-1167. |
| [8] | 郭海燕. 分子印迹-化学发光法在药物分析及农药残留分析中的应用 [D]. 西宁: 青海师范大学, 2013. |
| [9] | 蒋旭红, 吴嫦秋, 刘展眉. 茶碱分子印迹聚合物微球的合成及其性能研究 [J]. 中草药, 2013, 44(15): 2055-2058. |
| [10] | 郭智军. 磁性分子印迹聚合物制备及其应用的研究 [D]. 西宁: 青海师范大学, 2013. |
 2014, Vol. 55
2014, Vol. 55

