肺癌是严重威胁人类健康的恶性肿瘤之一,靶向治疗是肺癌的理想治疗手段。早期的肺部靶向制剂多是将药物包载于十几到几十微米的微球中,静脉注射后利用肺毛细血管床对粒径大于7 μm的微粒的机械截留作用将药物靶向至肺部[1]。然而,微球粒径超过毛细血管径,静脉注射可能堵塞血管,带来隐患。因此,有必要寻求一种新的肺靶向给药系统。
诸多研究[2, 3, 4, 5]证实,干粉吸入剂能有效地将药物输送至肺部,获得较高的肺部药物浓度,降低药物在其他器官的分布,减轻或避免药物的不良反应,已被用于慢性阻塞性肺病、肺结核、肺炎等肺部疾病的治疗。近年来,采用生物降解材料制备的微粒载药系统被广泛用于干粉吸入给药[6, 7]。在各种高分子聚合载体材料中,壳聚糖微球具有的独特的物理化学和生物学性质,使其尤其适用于肺部给药系统[8, 9, 10]:(1)壳聚糖与呼吸道和肺泡上皮细胞的生物相容性好,且具有良好的生物降解性;(2)壳聚糖带正电荷,能与肺泡黏膜的负电荷相互作用,提高黏附性,降低清除率,延长肺部滞留时间;(3)具有溶胀性,微球在湿润的肺部沉积后即可吸水溶胀,体积径增大,避免巨噬细胞的吞噬。
肺泡表面成分的70%~85%为磷脂类物质,以磷脂为主要材料的载体在肺部给药中具有生物相容性好、易吸收等独特优势。磷脂复合物是药物与磷脂按1∶1或1∶2的比例,以共价键结合而成的一种药物载体,能促进药物从亲水环境转移通过亲脂环境的上皮细胞膜进入细胞,最后到达血液。能否将磷脂复合物和壳聚糖微球结合成一个复合载体——磷脂复合物壳聚糖微球(PS-CMs),用于难溶性成分的肺部给药,利用壳聚糖微球的优势增加药物的肺部沉积量,避免肺部清除,利用磷脂复合物促进药物的肺泡吸收,进而增加肺部的药物浓度,提高疗效,成为有待探索的课题。
姜黄素(curcumin,Cur)是从姜科植物姜黄的根茎中提取的有效成分之一,可抑制肺癌A549细胞的增殖、转移并诱导其凋亡[11, 12],延长恶性转移瘤动物的存活期[13]。为发挥Cur对肺癌的治疗作用,必须将其有效地输送至肺部并吸收。然而,Cur水溶性极低,限制了跨膜转运和吸收,口服生物利用度不足1%,注射给药则因大量增溶辅料的应用存在潜在的安全性问题。因此,有必要研究其治疗肺癌的新给药途径和给药系统。
研究采用喷雾干燥法制备Cur-PS-CMs,对其工艺进行了优化,制备出理论空气动力学径小于5 μm,体外肺部有效沉积率达到59%的Cur-PS-CMs,并对微球的性质、结构进行了表征。研究结果可为进一步探讨PS-CMs吸入给药的体内肺靶向性和吸收机制奠定基础,为研发吸入给药的肺靶向给药系统提供参考。
1 仪器与材料D101—S型磁力搅拌器,江苏省金坛市荣华仪器制造有限公司;JY92—II DN超声波细胞粉碎机,宁波新芝生物科技股份有限公司;BT—100恒流泵,上海泸西分析仪器厂有限公司;梅特勒-托利多EL2046型电子天平,上海精天电子仪器有限公司;BS—1E恒温振荡培养箱,金壇市精达仪器制造厂;MalvernMastersizer2000型激光粒度仪,英国Malvern公司;ZS90纳米粒度及Zeta电位仪,马尔文公司;UV3100紫外,天美科技有限公司;S3000扫描电子显微镜(SEM),日本Hitachi;Veco Multimode原子力显微镜(AFM),美国Veco公司;200PC热分析仪,德国Netzsch;YC—015A微型实验室有机溶剂喷雾干燥机,上海雅程仪器设备有限公司;MSALXD—3型X射线衍射仪,北京普析通用仪器有限责任公司;两级玻璃撞击器(按《中国药典》2010年版附录X H的规格,自制);药粉吸入器,泰安凯瑞特高分子有限公司。
Cur(批号120513,质量分数>95%),杭州绿天生物科技有限公司;大豆磷脂(PC,批号120819,质量分数>90%),上海太伟药业有限公司;壳聚糖(CS,脱乙酰度93.2%,黏度112 mPa∙s),金湖甲壳制品有限公司;3号空心胶囊,新仓县亚利大胶丸有限公司;其余试剂均为分析纯。
2 方法与结果 2.1 Cur的测定参考文献方法[14],采用分光光度法于420 nm处测定Cur的量。精密称取Cur 7.5 mg,甲醇定容至100 mL,得质量浓度为75 μg/mL的储备液。精密吸取1.0、0.5、0.25、0.1、0.05 mL储备液,用甲醇- 0.1 mol/L盐酸(1∶1)定容至10 mL,得不同质量浓度的Cur对照品溶液,420 nm处测定吸光度(A)值,计算回归方程。结果在0.375~7.5 μg/mL的范围内,Cur在420 nm的A值与质量浓度呈线性关系,回归方程为A=0.159 9 C+0.008 7,r=0.999 9。
2.2 Cur磷脂复合物(Cur-PS)水分散液的制备及性质参照文献方法[15]制备Cur-PS水分散液并进行表征。将0.5 g Cur、1.0 g大豆磷脂溶于50 mL无水乙醇中,50 ℃水浴搅拌(1 000 r/min)5 h后匀速注入到2 000 mL纯水中,继续搅拌(1 000 r/min)30 min,即得。另取等量Cur,用50mL无水乙醇溶解,匀速注入到2 000mL纯水中,继续搅拌30 min,得Cur水分散液(作对照)。
分别取Cur-PS水分散液和Cur水分散液少许,点于云母片上,自然干燥后用AFM观察形态。将水分散液稀释后直接用纳米粒度及Zeta电位仪测定粒径和Zeta电位。4℃,30 000 r/min离心2 h,取上清液测定游离药物量(WF);另精密量取适量水分散液,甲醇稀释后测定药物总量(WT)。按下式计算复合率:复合率=(WT-WF) / WT。
Cur-PS水分散液呈淡黄色乳光,室温放置7 d后外观无明显变化;Cur水分散液放置12 h已有明显的絮状物和沉淀生成。AFM下Cur-PS呈良好的球形,分散均匀,而Cur水分散液可见大量杂乱物质(图 1)。Cur-PS的平均粒径为(42.51±8.05)nm(n=3),平均Zeta电位为(-13.37±1.94)mV(n=3),平均复合率为(90.27±2.04)%(n=3)。
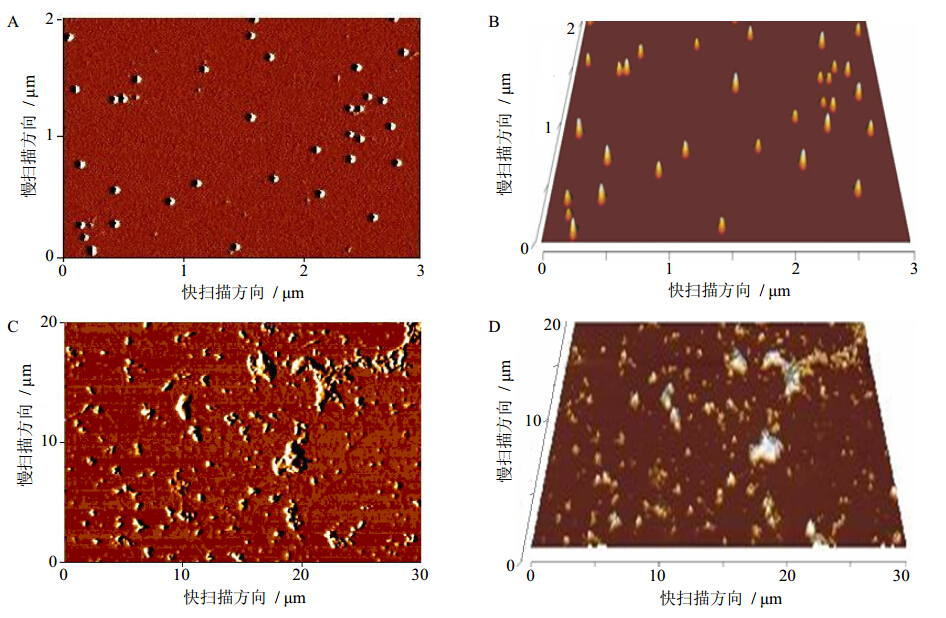 | 图 1Cur-PS分散液 (2 d,A;3 d,B) 和Cur水分散液 (2 d,C;3 d,D) 的AFM电镜图 Fig. 1 AFM electron micrographs ofCur-PS dispersion (2 d,A; 3 d,B)and Cur dispersion (2 d,C; 3 d,D) |
称取一定量的壳聚糖,用200 mL 1%的醋酸水溶液溶解,加入到2 000 mL Cur-PS水分散液中,混合均匀,搅拌条件下(2 000 r/min)以1 mL/min的速率滴加三聚磷酸钠(TPP)溶液,静置过夜,弃上清液后喷雾干燥,条件如下:进口温度为140 ℃,喷雾压力为0.3 MPa,供液速度为3 mL/min,风机频率为20 Hz。工艺条件见表 1。
| 表 1 Cur-PS-CMs的工艺条件 Table 1 Technology of Cur-PS-CMs |
用2000 mL同质量浓度的Cur水分散液代替Cur-PS水分散液,其余条件同F7,同法制备Cur-壳聚糖微球(Cur-CMs)。
2.4 微球的评价 2.4.1 载药量(DL)取微球适量,精密称定质量(W),加混合溶剂(甲醇-0.1mol/L盐酸1∶1)30 mL,探头超声后用0.45 μm微孔滤膜滤过,稀释一定倍数后于420 nm测定A值,计算Cur质量浓度(ρ),按下式计算DL:DL=ρ×30×稀释倍数 / W。
2.4.2 吸湿性取一定量微球,精密称定质量(W0),放置于25 ℃、相对湿度为75%的饱和NaCl溶液中,平衡7 d后取出,精密称定微球质量(W1),按下式计算吸湿率:吸湿率=(W1-W0) /W0。
2.4.3 流动性将微球粉末通过下孔径为5 mm的玻璃漏斗,从6 cm的高度缓慢、均匀地落入平板上,形成圆锥体。测量圆锥体的高度(h)和基底的直径(d),按下式计算休止角(θ):tanθ=2 h/d[16]。
2.4.4 振实密度(ρtap)精密称取一定质量(W)微球置于封底的1 mL塑料注射器筒中,将注射器从5 cm高度落下,反复振实500次,读取微球体积(V),按下式计算ρtap:ρtap=W/V[17,18]。
2.4.5 粒径及分布激光粒度测定仪测定微球的平均体积径(Dv)、d0.1、d0.5和d0.9,按下式计算跨距(span):span=(d0.9-d0.1)/d0.5[18]。
2.4.6 理论的空气动力学径按下式计算理论的空气动力学粒径(Da):Da=(ρtap/ρ0)1/2∙Dv,其中ρ0=1 g/cm3[16,18]。
2.4.7 体外沉积性质按照《中国药典》2010年版二部附录X H的方法进行。在一级沉积瓶D中,加7 mL无水乙醇作为吸收液,在二级沉积瓶H中加入30 mL无水乙醇作为吸收液。取胶囊1粒(装约20 mg微球,精密称定质量),置吸入装置内,吸入装置用适宜橡胶接口与模拟喉部B呈水平紧密相接,用手指按压装置两侧按钮,将胶囊刺破,开启真空泵,调节流量使其达到60 L/min,10 s后取下吸入器。取出胶囊,收集胶囊内的残留药物,用甲醇-0.1 mol/L盐酸(1∶1)溶解并定容至一定体积,测定Cur的量。用甲醇-0.1 mol/L盐酸(1∶1)分别淋洗吸入装置、模拟喉部、模拟颈部、1级分布瓶和2级分布瓶(包括导管内、外壁及垫片凸出物的表面),洗液分别收集于一定体积的量瓶中,超声并定容至刻度,测定Cur的量。按下式计算有效部位沉积率(FF)和排空率(ED):FF=2级分布瓶的药量/胶囊中的总药量,ED=1-胶囊中剩余的药量/胶囊中的总药量[19]。
不同工艺条件制备的微球的性质考察见表 2,体外沉积结果见表 3。由表 2、3可知,壳聚糖与磷脂的比例对Cur-PS-CMs的性质有很大影响:增加壳聚糖的用量,DL降低,吸湿性增强,流动性变差,平均体积径减小但振实密度增大,使理论空气动力学径先降后升。壳聚糖-磷脂为3∶1时,理论的空气动力学径最小,体外有效沉积率和有效沉积量最大。壳聚糖与TPP的质量比和TPP的浓度对Cur-PS-CMs的影响较小。不同工艺制备的微球排空率无明显差异,几乎都能全部从胶囊中排出。
| 表 2 Cur-PS-CMs的工艺条件 (x±x, n=3) Table 2 Characteristic of microspheres prepared with different technologies (x±x, n=3) |
| 表 3 不同工艺条件制备的微球的体外沉积(x±x, n=6) Table 3 Deposition in vitro of microspheres prepared with different technologies (x±x, n=6) |
分别对Cur、空白磷脂复合物-壳聚糖微球(PS-CMs)、Cur原料药与空白磷脂复合物-壳聚糖微球的机械混合物(Cur+PS-CMs)、Cur-PS-CMs(F7)和Cur-CMs进行测试。工作条件:升温范围为40~240℃;升温速率为10 ℃/min;参比物为空铝坩埚;气氛为氮气(质量分数为99.99%)。结果见图 2。Cur在171.6 ℃时有明显的吸热峰,PS-CMs在90.9 ℃有1个宽峰;Cur+PS-CMs图谱中,微球的宽峰移至86.2 ℃,Cur的吸热峰移至167.9 ℃;Cur-CMs分别在89.4 ℃和175.1 ℃显示出微球和Cur的吸热峰,说明Cur的存在状态与原料药相同;Cur-PS-CMs无Cur的吸热峰,微球的宽峰迁移至79.9 ℃,说明,在Cur-PS-CMs中Cur仍以磷脂复合物的形式存在。
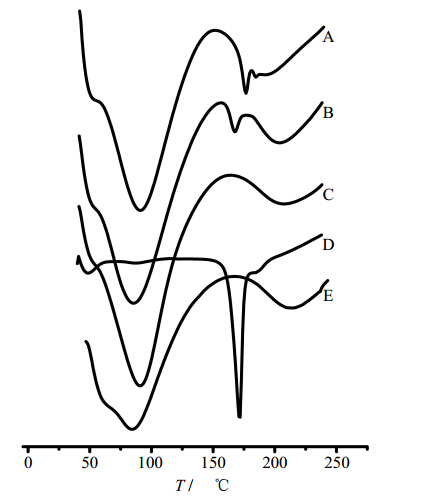 | 图 2 Cur-CMs (A)、Cur+PS-CMs (B)、PS-CMs (C)、Cur (D) 和Cur-PS-CMs (E) 样品的DSC图谱 Fig. 2 DSC of Cur-CMs (A),Cur + PS-CMs (B),PS-CMs (C),curcumin (D),and Cur-PS-CMs (E) |
项。工作条件:Cu靶/石墨单色器,管压为36V,管流为20 mA,步宽为0.01°,扫描速度为2°/min,采样时间为1 s,扫描范围为5°~40°。各样品的XRD图谱见图 3。图 3显示,Cur在8.9°、14.3°、17.3°等处有多个特异性的结晶衍射峰;PS-CMs和Cur- PS-CMs的XRD图谱无明显的晶型峰;Cur与PS-CMs物理混合物的峰形为2种物质的叠加,Cur在8.9°和17.3°的特征峰明显;Cur-CMs也显示出Cur的多个特征衍射峰。可见,在Cur-CMs中,Cur以原始的微晶形式存在;在Cur-PS-CMs中,Cur仍与磷脂复合,未从复合物中解离出来。结果与DSC一致。
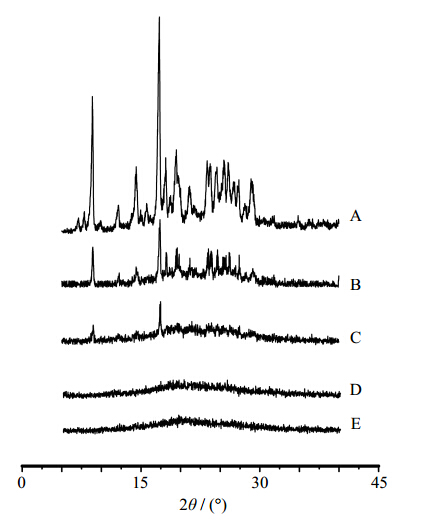 | 图 3 Cur (A)、Cur-CMs (B)、Cur+PS-CMs (C)、Cur-PS-CMs (D) 和PS-CMs (E) 样品的XRD图谱 Fig. 3XRD spectra ofCur (A),Cur-CMs (B),Cur + PS-CMs (C),Cur-PS-CMs(D),and PS-CMs (E) |
采用SEM观察Cur-PS-CMs(F7)和Cur-CMs的形态。结果可见,Cur-PS-CMs为外形饱满,表面较光滑的球形,大小均匀;Cur-CMs球形差,表面多褶皱、凹陷多(图 4)。 3 讨论
本课题组前期已采用离子凝聚法(滴入法、注入法)和乳化交联法制备Cur-PS-CMs,其粒径分别为(1.11±0.08)mm、(16.19±4.91)μm和(77.48± 19.37)μm[13],均不符合肺部给药的需求。本研究利用喷雾干燥法将磷脂复合物(PS)包载于壳聚糖微球(CMs)中,最终制备出了可用于吸入给药,将药物递送至肺部的干粉吸入剂。工艺研究发现,壳聚糖与磷脂的质量比是影响微球性质的主要因素。当壳聚糖-磷脂小于1∶1时,壳聚糖太少,无法克服磷脂的半固体性质,因此收集瓶中难以收得干燥的细粉,样品均黏附于干燥塔壁上。当壳聚糖-磷脂为1∶1时,收集瓶壁上有较多细粉出现,但用刷子收集时易聚集黏结成细小颗粒,使得测得的体积径较大,振实体积大而密度小,休止角小而流动性好。随着壳聚糖用量的增加,磷脂复合物壳聚糖微球(PS-CMs)的粉末性增强,体积径减小但振实密度增大,休止角增大,吸湿性增强。当壳聚糖-磷脂为3∶1时,Cur-PS-CMs具有较佳的载药量、吸湿性和理论的空气动力学径。
 | 图 4 Cur-PS-CMs (×500,a;×6 000,b) 和Cur-CMs (×700,c;×4 000,d) 微球的SEM图 Fig. 4 SEM figures of Cur-PS-CMs (× 500,a; × 6 000,b) and Cur-CMs (× 700,c; × 4 000,d) |
本研究采用《中国药典》2010年版收载的2级玻璃撞击器对微球进行了初步的体外肺部沉积考察。研究结果显示,壳聚糖与磷脂的比例显著影响有效沉积率,3∶1时的有效沉积率明显高于其他比例,与理论空气动力学径的结果一致。此外,交联剂TPP的浓度也是影响体外沉积的一个重要因素,TPP浓度过高或过低,都会导致有效沉积率降低。实验过程中发现,TPP浓度为3%时,喷雾干燥前的Cur-PS-CMs粒径大,3 h的沉降体积比约为75%;浓度为0.2%时,沉降减慢,12 h的沉降体积比仍高于80%,说明喷干前的2种Cur-PS-CMs粒径差异明显。而粒度分析仪测得的2种Cur-PS-CMs粉末粒径差异却不大。分析原因,可能是由于用0.2%的TPP交联后制得Cur-PS-CMs粉末经过旋风分离器时,只有达到一定大小的粒子才能沉降于收集瓶中,其余粒径很小的粒子则随气流带走,这也与实验中观察到的收集瓶中产品明显减少的现象一致。
对比Cur-CMs和Cur-PS-CMs的性质发现,两者在吸湿性、休止角、振实密度方面无明显差异,Cur-CMs的有效沉积率略小于Cur-PS-CMs。分析其原因,可能与微球的形态有关。扫描电镜观察到Cur-PS-CMs具有良好的球形,表面光滑,而Cur-CMs表面多皱缩凹陷,球形差。良好的球形结构使其更容易随气流分散,因而具有较好的沉积性。
欲达到利用磷脂复合物促进药物吸收的目的,磷脂复合物需从壳聚糖微球中完整的释放出来。DSC和XRD证实,在Cur-PS-CMs中Cur不以原始的结晶形式存在,提示Cur-PS未发生解离,仍保持了复合状态,为复合物的完整释放提供了前提。本实验仅对Cur-PS-CMs的制备和体外沉积进行了研究,Cur-PS-CMs的释药过程和机制,体内肺部沉积和吸收,肺靶向性评价等试验正在进行,将另文发表。
PS-CMs成功构建的关键在于药物-磷脂复合物水分散液的制备。研究过程中,曾用冬凌草甲素做过比较。冬凌草甲素与磷脂在乙醇中可成功复合,但注入水中后复合物即发生解离。这是因为冬凌草甲素的羟基为醇羟基,与磷脂形成的分子间连接并不紧密,遇到较高介电常数的水迅速被隔开。Cur的羟基为酚羟基,与磷脂产生的分子间氢键作用强,遇水后仍能稳定存在。PS-CMs的成功构建有望为具有酚羟基或羧基等基团与磷脂紧密结合的、治疗肺部疾病的难溶性药物提供一种新的药物载体。
| [1] | 阎 洲, 裴元英. 紫杉醇肺靶向微球的制备及体内外评价 [J]. 中国临床药学杂志, 2006, 15(4): 226-229. |
| [2] | Stegemann S, Kopp S, Borchard G, et al. Developing and advancing dry powder inhalation towards enhanced therapeutics [J]. Eur J Pharm Sci, 2013, 48(1/2): 181-194. |
| [3] | Roa W H, Azarmi S, Al-Hallak M H D K, et al. Inhalable nanoparticles, a non-invasive approach to treat lung cancer in a mouse model [J]. J Control Rel, 2011, 150(1): 49-55. |
| [4] | Zhang Y, Wang X L, Lin X, et al. High azithromycin loading powders for inhalation and their in vivo evaluation in rats [J]. Int J Pharmaceut, 2010, 395(1/2): 205-214. |
| [5] | 王守斌, 王 博, 孙歆慧, 等. 吸入制剂的研究进展 [J]. 现代药物与临床, 2013, 28(2): 232-235. |
| [6] | Hirota K, Kawamoto T, Nakajima T, et al. Distribution and deposition of respirable PLGA microspheres in lung alveoli [J]. Colloid Surf B: Biointerfaces, 2013, 105C: 92-97. |
| [7] | Alipour S, Montaseri H, Tafaghodi M. Preparation and characterization of biodegradable paclitaxel loaded alginate microparticles for pulmonary delivery [J]. Colloid Surf B: Biointerfaces, 2010, 81(2): 521-529. |
| [8] | Jafarinejad S, Gilani K, Moazeni E, et al. Development of chitosan-based nanoparticles for pulmonary delivery of itraconazole as dry powder formulation [J]. Powder Technol, 2012, 222: 65-70. |
| [9] | Al-Qadi S, Grenha A, Remuñán-López C. Microspheres loaded with polysaccharide nanoparticles for pulmonary delivery: Preparation, structure and surface analysis [J]. Carbohyd Polym, 2011, 86(1): 25-34. |
| [10] | 周闻舞, 顾海铮. 壳聚糖微/纳米粒在定向给药系统中的应用研究 [J]. 药物评价研究, 2010, 33(4): 290-295. |
| [11] | 岳 秀, 蒋幼凡, 刘 晓, 等. 姜黄素通过Wnt信号转导通路抑制肺癌细胞A549增殖的研究 [J]. 重庆医科大学学报, 2008, 33(12): 1454-1457. |
| [12] | Shei L S, Lai K C, Hsu S C, et al. Curcumin inhibits the migration and invasion of human A549 lung cancer cells through the inhibition of matrix metalloproteinase-2 and -9 and vascular endothelial growth factor (EGF) [J]. Cancer Lett, 2009, 285(2): 127-133. |
| [13] | Kunnumakkara A B, Anand P, Aggarwal B B. Curcumin inhibits proliferation, invasion, angiogenesis and metastasis of different cancers through interaction with multiple cell signaling proteins [J]. Cancer Lett, 2008, 269(2): 199-225. |
| [14] | 唐 勤, 孙晓辉, 陈 豪, 等. 制备方法和工艺对姜黄素-磷脂复合物-壳聚糖微球体外性质的影响 [J]. 中草药, 2012, 43(12): 2377-2385. |
| [15] | 张继芬, 唐 勤, 莫 婷, 等. 姜黄素磷脂载体的表征及肠吸收研究 [J]. 中国药学杂志, 2012, 47(21): 1736-1740. |
| [16] | Nolan L M, Li J H, Tajber L, et al. Particle engineering of materials for oral inhalation by dry powder inhalers. II-sodium cromoglicate [J]. Int J Pharm, 2011, 405(1/2): 36-46. |
| [17] | Le V N P, Robins E, Flament M P. Agglomerate behaviour of fluticasone propionate within dry powder inhaler formulations [J]. Eur J Pharm Biopharm, 2012, 80(3): 596-603. |
| [18] | Kho K, Hadinoto K. Dry powder inhaler delivery of amorphous drug nanoparticles: Effects of the lactose carrier particle shape and size [J]. Powder Technol, 2013(233): 303-311. |
| [19] | 严翠霞, 江文明, 陈桂良, 等. 吸入粉雾剂粒径测定方法的评价: 3种撞击器的比较 [J]. 药物分析杂志, 2011, 31(7): 1296-1299. |
 2014, Vol. 45
2014, Vol. 45


