2. 山东大学药学院 天然产物化学生物学教育部重点实验室, 山东 济南 250012
2. Key Laboratory of Chemical Biology, Ministry of Education, School of Pharmaceutical Sciences, Shandong University, Jinan 250012, China
没药为橄榄科植物地丁树Commiphora myrrha Engl. 或哈地丁树C. molmol Engl. 分泌的胶状树脂,为常用树脂类中药,具有散血祛瘀、消肿定痛之功效。除上述两种没药属植物,本属其他植物的胶状树脂亦常作为没药入药使用,如穆库尔没药C. mukul (Hook. ex Stocks) Engl.。本属植物中主要含有萜类、甾体类、木脂素类等化学成分,具有抗肿瘤、抗微生物、抗炎、镇痛等药理作用[1,2,3]。
穆库尔没药为没药属中的一种重要植物,主要分布于印度的拉贾斯坦、古加拉特、卡纳塔克等地区,在非洲东部的埃塞俄比亚等国家亦有分布。前人对该种植物化学成分研究较多,分离鉴定了一系列甾体、倍半萜、二萜、三萜、长链脂肪醇等化合物[1,2,3]。本课题组围绕没药属植物开展了次生代谢产物分离鉴定、生物转化和抗肿瘤作用机制的研究工作,并分离鉴定了一系列倍半萜、三萜、甾体等化合物[4,5,6,7,8]。在此基础上,针对穆库尔没药开展了系统的化学成分研究,以期获得结构新颖的化合物,丰富本属植物的化学结构多样性。本实验从穆库尔没药树脂醋酸乙酯提取物中分离获得2个吉玛烷型倍半萜化合物,分别鉴定为1α,8α,12α-三羟基-2β-甲氧基- 8,12-环氧吉玛烷-7(11),9-二烯-6-酮 [1α,8α,12α- trihydroxy-2β-methoxy-8,12-epoxygermacra-7(11),9- dien-6-one,1]、1α,8β,12α-三羟基-2β-甲氧基-8,12-环氧吉玛烷-7(11),9-二烯-6-酮 [1α,8β,12α- trihydroxy-2β-methoxy-8,12-epoxygermacra-7(11),9-dien-6-one,2]。2个化合物均为新化合物,分别命名为穆库尔素A(1)和穆库尔素B(2)。
1 仪器与材料Bruker Avance 600型核磁共振波谱仪,API4000型质谱仪和Waters GCT飞行时间高分辨气质联用仪。石油醚、醋酸乙酯、三氯甲烷、丙酮均为分析纯;薄层色谱用硅胶(Silica gel GF254)及柱色谱用硅胶(200~300目)均由青岛海洋化工厂生产;Sephadex LH-20凝胶购自Pharmacia Bioteck公司。
没药药材于2007年9月购自瑞士Dixa AG药材公司,产地为埃塞俄比亚。药材为干燥的胶状树脂,呈颗粒状,大小均一,直径约0.5 cm,淡黄色或桔黄色,表面具有光泽。质坚脆,具有芳香气味。由山东大学药学院生药学研究所向兰教授鉴定为穆库尔没药Commiphora mukul (Hook. ex Stocks) Engl.。标本(20070930CM)存于山东大学药学院生药学研究所。
2 提取与分离穆库尔没药树脂3.0 kg,粉碎,以醋酸乙酯为提取溶剂,索氏提取器提取36 h,减压浓缩得浸膏220 g。取100 g浸膏,采用硅胶柱色谱,以石油醚-醋酸乙酯梯度洗脱(100∶0→0∶100),并采用薄层色谱法合并相同部分,得10个馏份Fr. 1~10。Fr. 9
(27 g)采用硅胶柱色谱,以石油醚-醋酸乙酯梯度洗脱(85∶15→50∶50)得8个组分Fr. 9a~9h。Fr. 9f采用制备薄层色谱,石油醚-三氯甲烷-丙酮(50∶50∶20)为展开剂分离制备获得化合物1和2,共22 mg。
3 结构鉴定化合物1和2为一对无法分离的异构体(图 1),由其氢谱中峰面积比值推断两者在混合物中比例为3∶1。碳谱信号均裂分,而氢谱信号部分裂分,可能因个别位置异构化引起,遂在混合物状态下进行结构解析。
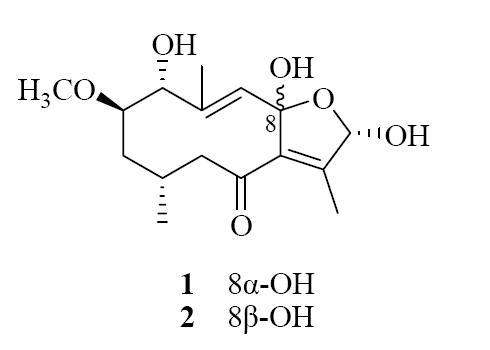 | 图 1 化合物1和2的化学结构式Fig. 1 Chemical structures of compounds 1 and 2 |
化合物1和2为白色粉末,以石油醚-丙酮(7∶3)为展开剂在薄层色谱板上展开,Rf值为0.30,10% H2SO4-EtOH试剂加热后显粉红色斑点。ESI- MS谱中显示m/z: 313.5 [M+H]+;其分子式通过HR-EI- MS(m/z 294.149 0 [M-H2O]+,计算值294.146 7)结合NMR波谱数据(表 1)推断为C16H24O6,不饱和度为6。化合物1/2的1H和13C-NMR数据结合HMQC谱可推断,1/2结构中分别含有3个甲基、2个亚甲基、1个次甲基、4个连氧碳、2个双键、1个酮羰基 (δC 206.2/206.4)、1个甲氧基 (δC 57.1/57.1)。
| 表 1 化合物1和2的核磁共振波谱数据 (CDCl3) Table 1 NMR data of compounds 1 and 2 (CDCl3) |
对2个化合物的波谱数据分别单独解析确定其结构。化合物1为其中量较大的组分,1H-1H COSY谱中,H-2 (δH 3.57) 与H2-3 (δH 1.43和1.65) 和H-1 (δH 5.05) 相关;H-4 (δH 2.35) 与H2-3 (δH 1.43和1.65) 和H2-5 (δH 2.03和3.10) 相关;H-4 (δH 2.35) 与H3-15 (δH 1.06) 相关;由此确定分子中1个自旋耦合系统(图 2中黑线所示结构片段)。HMBC谱中存在下列相关关系:H3-14 (δH 1.76) 与C-1 (δC 87.5),C-9 (δC 124.2),C-10 (δC 143.8);H-9 (δH 5.37) 与C-8 (δC 120.3);H2-5 (δH 2.03和3.10) 与C-6 (δC 206.4);H3-13 (δH 1.79) 与C-6 (δC 206.4),C-7 (δC 138.5),C-11 (δC 140.3),C-12 (δC 101.8),C-8 (δC 120.3);H-12 (δH 5.61) 与C-8 (δC 120.3)(图 2)。根据上述HMBC相关关系将由1H-1H COSY谱推断出的结构片段(图 2中黑线所示)与HMQC确定的结构单元相连接,推出1的平面结构为1,8,12-三羟基-2-甲氧基-8,12-环氧吉玛烷-7(11),9-二烯-6-酮。采用同样的方法确定化合物2与1具有相同的平面结构。
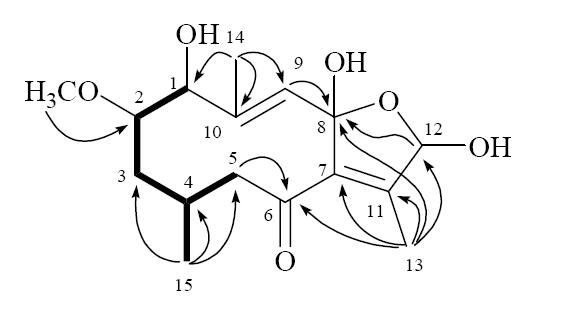 | 图 2 化合物1和2的主要1H-1H COSY (▬)和HMBC (H→C) 相关Fig. 2 Key 1H-1H COSY (▬) and HMBC (H→C) correlations of compounds 1 and 2 |
化合物1与2的相对构型通过NOESY谱和3D模拟确定。化合物1的NOESY谱中,H3-14 (δH 1.76) 与H-9 (δH 5.37) 相关,表明C-9位双键构型为顺式 (Z)。化合物1的NOESY谱存在下述相关关系:H-1 (δH 5.05) 与H3-14 (δH 1.76)、H-2 (δH 3.57) 和-OCH3 (δH 3.36);H-2 (δH 3.57) 与H-5α (δH 3.10);H3-15 (δH 1.06) 与 H-2 (δH 3.57)、H-5α (δH 3.10) 和H-5β (δH 2.03)(图 3-a)。结合文献报道的吉玛烷型倍半萜单晶[9]和Chem 3D模拟的方法,建立了化合物1 A环的构型,并对A环中碳原子不同构型的组合进行了空间距离测量,以确证化合物的立体构型,分为以下3个步骤:
(1)C-2构型确证:当H-2为α构型,2-OCH3为β构型时,H-2与H-5α和H-5β的距离分别为0.286和0.398 nm(图 3-a),与实测NOESY谱中H-2 (δH 3.57) 与H-5α (δH 3.10) 相关一致(若2个氢原子间存在NOE相关,其空间距离小于0.3 nm);当H-2为β构型,2-OCH3为α构型时,H-2与H-5α、H-5β的空间距离分别为0.415和0.510 nm,不存在NOE相关。因此确证H-2为α构型,2-OCH3为β构型。
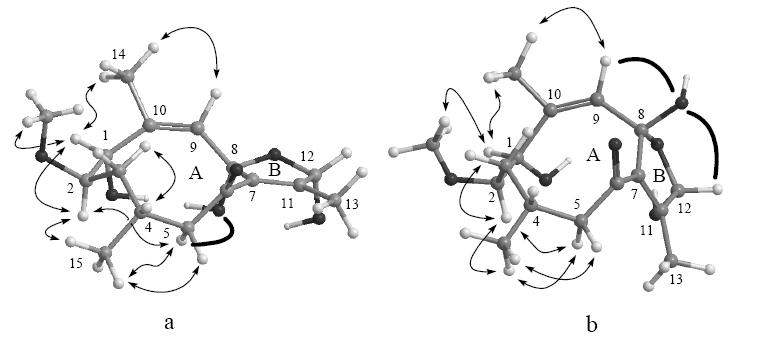 | 图 3 化合物1 (a) 和2 (b) 的主要NOESY (↔) 相关和OH去屏蔽效应 (▬) Fig. 3 Key NOESY (↔) correlations and OH defielding effect (▬) of compounds 1 (a) and 2 (b) |
(2)C-1构型确证:当H-1为β构型,1-OH为α构型时,H-1与H3-14、H-2和-OCH3的空间距离分别为0.207、0.283、0.289 nm(图 3-a),与实测NOESY谱中H-1 (δH 5.05) 与H3-14 (δH 1.76)、H-2 (δH 3.57) 和2-OCH3 (δH 3.36) 相关一致;当H-1为α构型,1-OH为β构型时,H-1与H3-14、H-2和2-OCH3的空间距离分别为0.303、0.239、0.373 nm,在此构型条件下H-1与H3-14、2-OCH3不存在NOE相关。因此确证H-1为β构型,1-OH为α构型。
(3)C-4构型确证:当H-4为β构型,15-CH3为α构型时,15-CH3与H-2空间距离为0.248 nm(图 3-a),与实测NOESY谱中H3-15 (δH 1.06) 与H-2 (δH 3.57) 相关一致;当H-4为α构型,15-CH3为β构型时,15-CH3与H-2空间距离为0.335 nm,不存在NOE相关。因此确证15-CH3为α构型。
由此确定化合物1 A环中1-OH、2-OCH3、15-CH3的相对构型分别为α、β、α构型。同理,根据化合物2的NOESY谱中的相关关系(图 3-b),推断出2与1具有相同的A环构型。
化合物B环中8-OH和12-OH的相对构型通过分析羟基去屏蔽效应对2个化合物1H-NMR谱数据的差异确证。1与2的3个位置H-5α、H-9和H-12的氢化学位移值存在差别。2中H-9 (δH 5.50) 化学位移值与1中H-9 (δH 5.37) 相比向低场位移0.13,此差别为8β-OH去屏蔽效应引起(图 3-b粗线所示),因此确证2中8-OH与H-9处于相同方向为β构型,而1中8-OH与H-9处于相反方向为α构型。同理,8β-OH对H-12的去屏蔽效应(图 3-b粗线所示)造成2中H-12 (δH 5.80) 比1中H-12 (δH 5.61) 向低场位移0.19,确定2个化合物中的12-OH均为α构型。而8α-OH对H-5α去屏蔽效应(图 3-a粗线所示)引起1中H-5α (δH 3.10) 比2中H-5α (δ H 3.04) 向低场位移0.06。
因此确定化合物1和2的结构分别为1α,8α,12α-三羟基-2β-甲氧基-8,12-环氧吉玛烷-7(11),9-二烯-6-酮和1α,8β,12α-三羟基-2β-甲氧基-8,12-环氧吉玛烷-7(11),9-二烯-6-酮,并分别命名为穆库尔素A和B(mukulsin A和B)。
| [1] | Shen T, Li G H, Wang X N, et al. The genus Commiphora: A review of its traditional uses, phytochemistry and pharmacology[J]. J Ethnopharmacol, 2012, 142(2): 319-330. |
| [2] | Shen T, Lou H X. Bioactive constituents of myrrh and frankincense, two simultaneously prescribed gum resins in Chinese traditional medicine[J]. Chem Biodivers, 2008, 5(4): 540-553. |
| [3] | 沈涛, 娄红祥. 没药的化学成分及其生物活性[J]. 天然产物研究与开发, 2008, 20(2): 360-366. |
| [4] | Shen T, Zhang L, Wang Y Y, et al. Steroids from Commiphora mukul display antiproliferative effect against human prostate cancer PC3 cells via induction of apoptosis[J]. Bioorg Med Chem Lett, 2012, 22(14): 4801-4806. |
| [5] | Shen T, Wan W Z, Yuan H Q, et al. Secondary metabolites from Commiphora opobalsamum and their antiproliferative effect on human prostate cancer cells[J]. Phytochemistry, 2007, 68(9): 1331-1337. |
| [6] | Shen T, Yuan H Q, Wan W Z, et al. Cycloartane-type triterpenoids from the resinous exudates of Commiphora opobalsamum[J]. J Nat Prod, 2008, 71(1): 81-86. |
| [7] | Shen T, Wan W Z, Wang X N, et al. Sesquiterpenoids from the resinous exudates of Commiphora opobalsamum (Burseraceae)[J]. Helv Chim Acta, 2008, 91(5): 881-887. |
| [8] | Shen T, Wan W Z, Wang X N, et al. A triterpenoid and sesquiterpenoids from the resinous exudates of Commiphora myrrha[J]. Helv Chim Acta, 2009, 92(4): 645-652. |
| [9] | Dekebo A, Dagne E, Hansen L K, et al. Crystal structures of two furanosesquiterpenes from Commiphora sphaerocarpa[J]. Tetrahedron Lett, 2000, 41(50): 9875-9878. |
 2014, Vol. 45
2014, Vol. 45


