2. 四川省自然资源科学研究院, 四川 成都 610041;
3. 四川大学生命科学学院, 四川 成都 610041
2. Sichuan Academy of Natural Resources Sciences, Chengdu 610041, China;
3. School of Life Sciences, Sichuan University, Chengdu 610041, China
藏药坐珠达西为丸剂剂型,由佐塔、红花、木香、诃子、余甘子、石榴子、安息香、唐古特乌头、马钱子等35味药物组成,功效为疏肝、健胃、清热、愈溃疡、消肿,用于“木布”病迁延不愈、胃脘嘈杂、消化不良、浮肿、水肿等[1],为藏药治疗慢性胃炎的常用药物。原制剂标准进行了2项理化反应鉴别和船形乌头薄层鉴别及丸剂的相关检查。马肖等[2]在此基础上又对熊胆、牛黄、木香、丁香进行了薄层鉴别,对马钱子中的马钱子碱进行了液相定性鉴别,对西红花中的西红花苷I进行了高效液相色谱定量测定。但是该药物组成药味较多,仅依靠少数指标的定量测定难以控制其内在质量。
该药物中诃子在藏药中被视为“药中之王”,具有很好的解毒功效,邪气聚于脏腑的内源性毒性和食物、药物中毒等外源性毒性都能驱解[3];余甘子系藏族常用药,能清热凉血、消食健胃,用于血热血瘀、消化不良、腹胀等症[4];石榴子能温中健脾,治疗厌食、胃寒、脘胀等症[5];此3种药物中均含有没食子酸,可用没食子酸作为三者的综合定量标准。木香中医常用以治疗胃部胀满、呕吐、腹痛和腹泻等消化不良症状,具有芳香健胃、行气止痛的功效,是常用理气药,主要成分为木香烃内酯和去氢木香烃内酯[6];红花藏医常用来治疗肝病、血病和进行培元健身,其主要成分有西红花苷I、西红花苷II[7];安息香具有开窍醒神、行气活血、镇惊息风等功效,其主要成分有苯甲酸[8]。在组成坐珠达西的药味中,还含有绿原酸和山柰酚。本研究针对上述8种指标性成分建立的多波长HPLC定量测定方法,并测定了2个厂家,共5个批次(四川阿坝州藏医院:批号20130926、20130823、20130703、20120618;金诃藏药:批号20120612)的样品,为更好地控制该药生产规范提供参考依据。
1 仪器与材料Waters 2695/2996型高效液相色谱仪,2996PDA检测器,Empower化学工作站;KQ5200E型超声波清洗器,昆山超声仪器有限公司;Metiler AE240S型电子天平,梅特勒-托利上海有限公司。
对照品没食子酸(批号111109,质量分数≥98.0%),苯甲酸(批号120807,质量分数≥98.0%),木香烃内酯(批号120322,质量分数≥98.0%),去氢木香烃内酯(批号120321,质量分数≥98.0%),西红花苷I(批号120714,质量分数≥98.0%),西红花苷II(批号110925,质量分数≥98.0%),四川省维克奇生物科技有限公司;对照品绿原酸(批号121125,质量分数≥98.0%),山柰酚(批号120718,质量分数≥98.0%),成都普菲德生物技术有限公司。坐珠达西(丸剂)供试品,批号20130926、20130823、20130703、20120618,四川阿坝州藏医院藏医药研究所制;批号20120612,金诃藏药股份有限公司。流动相甲醇为色谱纯(Oceanpak公司),提取用甲醇为分析纯(质量分数≥99.5%,成都市科龙化工试剂厂),磷酸为分析纯(质量分数≥85.0%,成都市科龙化工试剂厂),水为纯净水。
2 方法和结果 2.1 色谱条件Kromasil C18色谱柱(250 mm×4.6 mm,5 μm);流动相甲醇(A)-0.05%磷酸溶液(B),梯度洗脱:0~8 min,13%~20% A;8~20 min,20%~38% A;20~30 min,38%~50% A;30~45 min,50%~70% A;45~65 min,70%~80% A;体积流量为1 mL/min;柱温30 ℃;进样量10 μL;没食子酸、苯甲酸、山柰酚、木香烃内酯和去氢木香烃内酯检测波长为225 nm,绿原酸检测波长为352 nm,西红花苷I和西红花苷II检测波长为455 nm。按照上述色谱条件进行测定,各组分间分离度良好,对照品及样品的色谱图见图 1。
 | A1~A3-对照品 B1~B3-样品 1-没食子酸 2-绿原酸 3-苯甲酸 4-山柰酚 5-木香烃内酯 6-去氢木香烃内酯 7-西红花苷I 8-西红花苷II,图 4同 A1—A3-reference substances B1—B3-sample 1-gallic acid 2-chlorogenic acid 3-benzoic acid 4-kaempferol 5-costunolide 6-dehydroepiandrosterone costunolide 7-crocin I 8-crocin II,Fig. 4 is same图 1 对照品和样品HPLC图 Fig. 1 HPLC of reference substances and samples |
取没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯适量,精密称定,加甲醇分别制成含1.012、1.102、1.016、1.080、1.004、1.098 mg/mL的溶液;再取西红花苷I、西红花苷II适量,精密称定,加稀乙醇分别制成含1.070、1.064 mg/mL的溶液,即得各对照品溶液。分别精密吸取上述对照品溶液各2.7、1.3、0.9、1.7、3.5、3.0、0.5、0.2 mL于25 mL量瓶中,加甲醇定容至刻度,即得混合对照品溶液。
2.3 供试品溶液的制备取坐珠达西粉末1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密封,称定质量,超声提取30 min。冷却至室温后称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液即得。
2.4 线性关系的考察将“2.2”项下混合对照品溶液依次稀释1、2、4、8、16倍,分别精密吸取不同倍数和原混合对照品溶液10 μL进样,以进样质量浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,得到线性回归方程及相关系数,见表 1。
|
|
表 1 对照品的线性关系和范围 Table 1 Linearities and ranges of reference substances |
精密吸取“2.2”项下稀释1倍的混合对照品溶液,按“2.1”项下色谱条件,连续进样6次,每次10 μL,记录峰面积,计算峰面积的RSD。结果显示没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II峰面积的RSD分别为0.89%、0.49%、0.87%、0.93%、0.42%、0.44%、0.72%、0.58%,表明仪器精密度良好。
2.6 重复性试验取同一份坐珠达西样品(批号20130703)粉末6份,按“2.3”项下确定的方法平行制备供试品溶液,按“2.1”项下色谱条件进行分析。结果显示没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II质量分数的RSD分别为0.73%、1.99%、2.23%、1.12%、1.68%、2.19%、2.11%、2.07%,表明该方法重复性良好。
2.7 稳定性试验取一份坐珠达西样品(批号20130703)粉末,按“2.3”项下方法制备供试品溶液,分别于0、2、4、6、8、10、12、24 h时进样10 μL,按“2.1”项下色谱条件进行分析,计算各成分峰面积的RSD。结果显示供试品溶液中没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II峰面积的RSD分别为1.85%、2.02%、2.65%、3.32%、3.76%、1.38%、3.49%、2.25%,表明供试品溶液在24 h内稳定。
2.8 加样回收率试验称取已测定的坐珠达西样品(批号20130703)粉末6份,每份约1 g,精密称定,置于具塞锥形瓶中,加入各对照品溶液(使得对照品量相当于样品中相应成分量的50%~120%)适量,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,计算各对照品的回收率和RSD,结果没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II的平均加样回收率为100.17%、97.99%、101.42%、100.54%、99.13%、99.82%、98.11%,97.13%,RSD为2.1%、2.9%、5.2%、4.2%、3.3%、5.3%、2.0%、3.4%。
2.9 样品测定取各批次的坐珠达西样品粉末,按“2.3”项下的方法制备供试品溶液,每个样品平行2份,并按“2.1”项下的色谱条件进行测定,每份测定2次,计算各样品中没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II的量,结果见表 2。
|
|
表 2 5批样品中8种成分的测定 (n=4) Table 2 Contents of eight constituents in five batches of samples (n=4) |
参考文献方法[9],以上述测定的8个成分质量分数为数据库。以SIMPCA-12.0软件进行PCA和偏最小二乘法(PLS)分析。坐珠达西样品HPLC的PCA打分图见图 2,聚类分析(HCA)对PCA进行聚类分析柱状图见图 3,荷载图见图 4。结果显示:图 2和图 3中坐珠达西样品清晰地聚为2大类,阿坝州藏医院产样品聚为1类,金诃藏药产样品聚为1类;同时四川产样品不同批次间又分2组。图 4表明本实验中用于定量测定的8个指标峰对坐珠达西内在质量贡献较大。
 | 图 2 样品的PCA图 Fig. 2 PCA plot of samples |
 | 图 3 坐珠达西样品PCA打分图的HCA分析图 Fig. 3 HCA analysis by PCA scores of Zuozhudaxi samples |
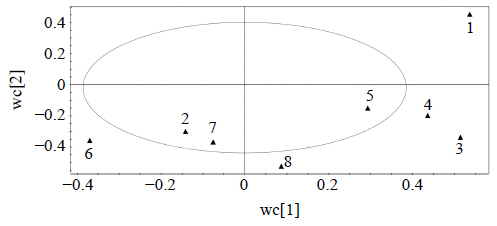 | 图 4 坐珠达西样品的PCA荷载图 Fig. 4 PCA plot of Zuozhudaxismaples |
本研究建立了同时测定藏药坐珠达西中8种成分的HPLC方法,并测定了2个厂家5批10个样品中的8种成分。该方法简单准确,具有较好的重复性和稳定性。
3.1 检测波长的确定采用PDA二极管阵列检测器,分别对8种成分在190~700 nm进行全波长扫描。结果显示没食子酸、绿原酸、苯甲酸、山柰酚、木香烃内酯、去氢木香烃内酯、西红花苷I和西红花苷II分别在210、352、230、204、225、225、455、455 nm处有最大吸收。为了兼顾8种成分的最大吸收波长,同时降低工作量,经多次实验验证最终确定没食子酸、苯甲酸、山柰酚、木香烃内酯和去氢木香烃内酯5个样品的检测波长为225 nm,绿原酸的检测波长为352 nm,西红花苷I和西红花苷II的检测波长为455 nm。
3.2 供试品提取方法的考察本研究分别考察了甲醇超声提取,甲醇回流,甲醇回流后酸解3种提取方法对坐珠达西样品中8种成分提取效果的影响,结果以甲醇超声提取的效果最好,加热回流和加酸对样品中的8种成分都有一定的破坏作用,最终确定采用甲醇25 mL超声提取30 min作为供试品溶液的制备方法。
3.3 流动相的确定分别考察了乙腈-0.05%磷酸水溶液和甲醇- 0.05%磷酸水溶液2种流动相,结果显示乙腈-0.05%磷酸水溶液作为流动相时杂峰很多且多拖尾现象,严重影响8种成分的检测,甲醇-0.05%磷酸水溶液作为流动相上述现象较为缓和,最终选择甲醇- 0.05%磷酸水溶液进行优化作为洗脱流动相。
3.4 聚类分析本研究以所测8个成分为数据库进行了聚类分析,结果显示青海产样品和四川产样品各聚为一类,同时四川产样品又分为2组,表明四川和青海2个厂家内在质量差异较大;同一厂家不同生产年生产的坐珠达西内在质量差异也较大。由于坐珠达西生产工艺较为一致,因此说明不同地区的厂家和批次生产过程中,原药材料的质量控制和生产工艺的控制存在较大的波动,这可能是由于不同地区的藏药厂在生产过程中,使用了同物异名、或不同采收季和生产年限的原药材所致,需要进一步完善原药材和成品的质量标准。
同时经打分图分析可知,本实验中用于测定的8个指标峰对坐珠达西内在质量贡献较大,而其中以峰1(没食子酸)、峰3(苯甲酸)、峰4(山柰酚)、峰6(去氢木香烃内酯)和峰8(西红花苷II)对坐珠达西的质量贡献尤为明显。上述分析表明8个指标成分的定量测定有助控制坐珠达西的内在质量。
| [1] | 中华人民共和国卫生部标准?藏药 [S]. 1995. |
| [2] | 马 肖, 王兰霞, 赵建邦, 等. 提高坐珠达西质量标准的研究 [J]. 药物分析与检验, 2012, 29(3): 250-253. |
| [3] | 罗光伟, 陈建江. 诃子的药理作用研究进展 [J]. 云南中医中药杂志, 2012, 33(11): 78-80. |
| [4] | 沙 磊, 张兰珍, 徐义侠, 等. RP-HPLC法测定余甘子中诃黎勒酸、没食子酸、粘酸-2-O-没食子酸酯的含量 [J]. 药物分析杂志, 2011, 31(2): 293-295. |
| [5] | 王秋霞, 贾美艳, 唐荣平, 等. 石榴籽化学成分及应用研究进展 [J]. 特产研究, 2006, 28(1): 53-55. |
| [6] | 张建春, 蔡雅明, 周德斌, 等. 木香的研究进展 [J]. 甘肃科技, 2010, 26(27): 170-173. |
| [7] | 中国科学院西北高原生物研究所. 藏药志 [M]. 西宁: 青海人民出版社, 1991. |
| [8] | 王 峰, 鄢琼芳, 华会明. 安息香属植物化学成分及药理作用研究进展 [J]. 广东药学院学报, 2009, 25(5): 541-544. |
| [9] | 高 飞, 傅超美, 胡慧玲, 等. HPLC-UV技术用于川木香煨制前后代谢物轮廓差异研究 [J]. 中草药, 2013, 44(5): 547-551. |
 2014, Vol. 45
2014, Vol. 45


