2. 浙江维康药业有限公司, 浙江 丽水 323000
2. Zhejiang Weikang Pharmacyeutical Industry Co., Ltd., Lishui 323000, China
穿心莲为爵床科穿心莲属穿心莲Andrographis paniculata (Burm. f.) Nees的干燥地上部分,具有清热解毒、凉血消肿的功效。临床上用于感冒发热、咽喉肿痛、口舌生疮、顿咳劳嗽、泄泻痢疾、热淋涩痛、痈肿疮疡、毒蛇咬伤等[1]。
穿心莲片为穿心莲单味药材经加工制成的片剂,一直是《中国药典》收载品种并广泛应用于临床。穿心莲有效成分有穿心莲内酯、去氧穿心莲内酯、脱水穿心莲内酯等,其中脱水穿心莲内酯为主要有效成分,具有抗炎、解热作用,临床用于呼吸道及肠道感染性疾病有较好疗效[2]。但是穿心莲内酯类化合物难溶于水,其片剂在临床应用中溶出度较低,影响疗效[3,4]。本实验旨在通过优化穿心莲片的生产工艺路线,制备新型中药制剂穿心莲软胶囊,该剂型具有生物利用度高、吸收迅速、稳定性好、便于服用等优点[5,6]。同时,通过方法学研究,并对溶出度等进行考察,更有效地控制穿心莲软胶囊的质量。
1 仪器与材料RGY6—20型软胶囊机,北京长征天民高科技有限公司。LC—10AT vp型输液泵,SDP—10A vp型检测器,JS—3050色谱工作站,日本岛津公司。
脱水穿心莲内酯对照品(批号110854-200305、0854-9902)均由中国食品药品检定研究院提供。穿心莲药材[经浙江省丽水市食品药品检验所李建良副主任中药师鉴定为爵床科植物穿心莲Andrographis paniculata (Burm. f.) Nees的干燥地上部分]、穿心莲软胶囊(编号01~17)均由浙江维康药业有限公司提供。蜂蜡、司盘80、大豆油、PEG 400安徽山河药用辅料股份有限公司。所用试剂甲醇为色谱纯,水为双蒸水,其他试剂均为分析纯。
2 方法与结果 2.1 穿心莲提取物制备按《中国药典》2010年版穿心莲片项下规定进行提取[7]。取穿心莲药材1 000 g,用85%乙醇热浸提取2次,每次2 h,合并提取液,滤过,滤液回收乙醇,浓缩至适量,干燥得浸膏,称质量为105.5 g。
2.2 软胶囊内容物制备制备软胶囊内容物用辅料包括稀释剂、助悬剂、乳化剂等。
2.2.1 稀释剂的考察稀释剂用来增加药物的流动性,保证制剂装量准确稳定、药品安全有效并能顺利灌装。常见的稀释剂为植物油和PEG 400。植物油为传统的内容物稀释剂,适用于水不溶性药物或脂溶性药物,油类能增加甾体药物的溶解度同时低黏度的油类能增加内容物的流动性。PEG 400为常用的水溶性基质,无色黏稠液体,有轻微特殊气味,略有吸湿性。本实验考虑到穿心莲有效成分有穿心莲内酯、去氧穿心莲内酯、脱水穿心莲内酯等,因此选用大豆油作为稀释剂。同时对大豆油的用量进行考察,以溶解性和流动性作为考察指标,见表 1。结果表明最佳投料比为干膏-大豆油(1∶4)。
|
|
表 1 稀释剂大豆油用量考察 Table 1 Investigation of soybean oil consumption |
药材提取物的干膏与大豆油混合,流动性很好,但是会慢慢沉积,不利于灌装,必须加入一定量的助悬剂和乳化剂来改善内容物的流动性,提高药液的稳定性和沉降比。选用常见的助悬剂蜂蜡和不同的乳化剂,考察混悬液的稳定性,见表 2。结果表明大豆油-蜂蜡-司盘80最佳投料比为1∶0.065∶0.013。
|
|
表 2 助悬剂和乳化剂考察 Table 2 Investigation of suspending agent and emulsifying agent |
综合上述考察结果,穿心莲软胶囊最佳处方(1 000粒)配比为穿心莲1 000 g(干膏量为105.5 g),司盘80 5.5 g、蜂蜡27.5 g、大豆油422 g。
2.3 软胶囊囊壳的制备软胶囊的囊壳材料有明胶、增塑剂、附加剂、水等。囊材对软胶囊的崩解有一定影响,软胶囊的质量与囊壳材料的选择和配伍密切相关。
本实验采用不同的比例配料,放入500 mL抽滤瓶中,65 ℃水浴熔化,自动搅拌化胶,同时抽真空,真空度95 kPa左右,经5 h后保温放置1 h,滤过胶液,取一部分胶液测定黏度及其他性能,一部分胶液在铁板上均匀铺成一薄层(先在下面抹一层液体石蜡),放置于次日观察胶皮性能再作评价,见表 3。结果表明,经筛选,综合评价配方明胶-甘油-水(100∶40∶100)所制得的胶皮质量好。
|
|
表 3 胶囊壳配方考察 Table 3 Capsule shell formula |
软胶囊按压制法制备[5]。取大豆油与蜂蜡混匀,加热至约70 ℃使蜂蜡完全熔融,搅拌冷却至35 ℃以下,加入穿心莲浸膏粉,搅拌均匀,胶体研磨均匀,抽真空消去气泡,备用;取明胶-甘油-水(100∶40∶100),加入水浴式化胶罐,搅拌,熔融,保温1 h,抽真空无明显气泡,过80目筛网,放入胶桶保温(≥60 ℃),静置2~6 h。在18~26 ℃、相对湿度不超过50%的环境下用软胶囊压制机,填入上述物料,压制出软胶囊。在25 ℃、相对湿度25%~30%条件下,干燥16 h,即得。
2.5 工艺验证为了进一步考察优选工艺的生产可操作性,进行了6批中试试验,按《中国药典》2010年版一部附录I L“胶囊剂”项下有关规定,对6批样品进行了性状、装量差异、崩解时限以及指标成分测定等方面检查,结果均符合规定,见表 4。结果表明各工序产品得率基本稳定,该制备工艺具有可操作性。
|
|
表 4 6批中试试验产品生产数据 Table 4 Six batches of production data |
色谱柱为Kromasil C18柱(150 mm×4.6 mm,5.0 μm),流动相为甲醇-水(60∶40),体积流量1.0 mL/min,柱温30 ℃,进样量20 μL,检测波长254 nm。
2.6.2 溶液的制备(1)对照品溶液:精密称取置五氧化二磷干燥器中干燥至恒定质量的脱水穿心莲内酯对照品1.06 mg,置10 mL量瓶中,加甲醇适量振摇使溶解,再加甲醇稀释至刻度,密塞,摇匀,即得。
(2)供试品溶液:取装量差异下的穿心莲软胶囊内容物(批号20041102)约0.2 g,精密称定,置25 mL量瓶中,加无水乙醇25 mL超声提取30 min,冷至室温,加无水乙醇至刻度,密塞,摇匀,滤过,精密量取续滤液5 mL,置水浴上蒸干,残渣加甲醇分次使溶解,滤过,移入5 mL量瓶中,自同一滤器上加甲醇稀释至刻度,密塞,摇匀,即得。
(3)阴性对照溶液:按处方组成,取除穿心莲外的其他辅料,按制备工艺要求制成阴性对照样品,再按“供试品制备”项下方法制成阴性对照品溶液。
2.6.3 线性关系考察精密称取脱水穿心莲内酯对照品10 mg,置5 mL量瓶中,加甲醇适量振摇使溶解,再加甲醇稀释至刻度,密塞,摇匀,作为对照品溶液。精密吸取对照品溶液25、50、100、150、200 μL置2 mL量瓶中,加甲醇稀释至刻度,分别进样20 μL,测定峰面积。回归方程及相关系数分别为Y=313 614 X-267 456,R2=0.999 9,脱水穿心莲内酯在25~200 μg/mL与峰面积呈良好的线性关系。
2.6.4 样品测定取11批样品,按“供试品溶液的制备”方法制备供试品溶液,按上述色谱条件测定,记录峰面积,计算脱水穿心莲内酯的量,见表 5。结果表明,11批样品中含脱水穿心莲内酯最高为7.58 mg/粒,最低为5.18 mg/粒,平均每粒含脱水穿心莲内酯为6.46 mg,考虑到药材来源,制剂生产等各种因素,参考原穿心莲片质量标准将穿心莲软胶囊含量限度定为每粒含脱水穿心莲内酯不得少于4.5 mg。
|
|
表 5 样品测定 (n = 2) Table 5 Determination of samples (n = 2) |
按照《中国药典》2010年版二部附录XC溶出度测定项下第一法[7],转速100 r/min,以人工胃液900 mL为溶出介质,分别注入圆底烧杯中,加温使介质温度保持在(37.0±0.5)℃。以6粒为单位,精密称量2份,分别放入转篮内,启动转速,测定脱水穿心莲内酯的溶出度。分别在10、20、30、45、60 min时取样2 mL,经微孔滤膜(0.45 μm)滤过后,精密吸取滤液20 μL,注入高效液相色谱仪,按上述色谱条件测定峰面积,计算平均累积溶出率。结果表明,脱水穿心莲内酯累积溶出率在45 min后均大于87%,故选择45 min时测定溶出度即可。取穿心莲软胶囊3批(编号09、14、15),分别以6粒为单位,精密称量,按上述方法测定样品溶出度,结果分别为87.79%、89.10%、88.35%。表明不同批次样品的溶出度之间无明显差异,溶出曲线见图 1。
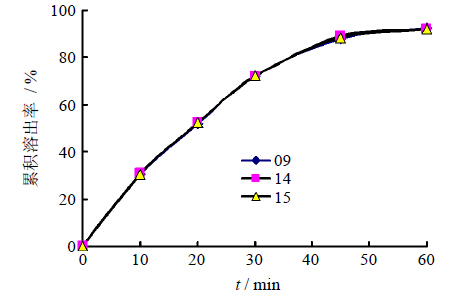 | 图 1 3批样品溶出曲线 Fig. 1 Dissolution curves of three batches of samples |
目前原片剂质量标准中,采用崩解时限检查衡量溶出情况,但是崩解试验结果往往不能很好反映溶出情况,尤其是有效成分内酯类化合物难溶于水。大量试验证实脱水穿心莲内酯从片剂中溶出的速率较慢,故需要对剂型进行改进。本实验结合原剂型的生产工艺进行优化,制备开发穿心莲软胶囊,旨在为临床提供一种便于服用且溶出快的新制剂。软胶囊作为中成药新剂型之一,综合了中药制剂毒副作用小、服用方便、吸收快、生物利用度高等优点。
在原片剂质量标准基础上,采用HPLC法测定穿心莲软胶囊中脱水穿心莲内酯,开展方法学研究。实验结果表明,该法操作简便、快速、重现性好,可有效控制穿心莲软胶囊的质量。本实验对经不同时间后的溶出情况进行了研究,建立了适宜的溶出度检测方法,以保证制剂的质量。
| [1] | 王 红, 张学东, 郭信芳. 穿心莲药材及穿心莲片的质量标准探讨 [J]. 西北药学杂志, 2002, 17(2): 63-64. |
| [2] | 张 静, 琚小龙, 李治坤, 等. HPLC法测定穿心莲软胶囊中脱水穿心莲内酯的含量 [J]. 安徽医药, 2003, 7(6): 453-454. |
| [3] | 宋 英, 陆静冉, 沈 鸣, 等. HPLC法测定穿心莲滴丸中脱水穿心莲内酯的溶出度 [J]. 中成药, 2012, 34(1): 178-180. |
| [4] | 胡向青, 巴晓雨, 赫 福, 等. 穿心莲内酯原料中有关物质和稳定性研究 [J]. 现代药物与临床, 2013, 28(4): 523-527. |
| [5] | 王贤英, 谢香菊, 李胜容. 金泽冠心软胶囊制剂工艺研究 [J]. 中国药业, 2013, 22(15): 59-61. |
| [6] | 张 静, 琚小龙, 李治坤, 等. HPLC法测定穿心莲软胶囊中脱水穿心莲内酯的含量 [J]. 安徽医药, 2003, 7(6): 453-454. |
| [7] | 中国药典 [S]. 一部. 2010. |
| [8] | 杨洪武, 田 原, 杨 明, 等. 提高穿心莲片溶出度的新工艺研究 [J]. 辽宁中医杂志, 2008, 35(3): 434. |
 2014, Vol. 45
2014, Vol. 45

 ,
,