巴戟天Morindae Officinalis Radix(MOR)为茜草科植物巴戟天Morinda officinalis How. 的干燥根,味甘、辛,性微温,具有补肾阳、强筋骨、祛风湿之功效[1],是我国著名的“四大南药”之一。巴戟天含有糖类、环烯醚萜苷类、蒽醌类和有机酸类等化学成分[2,3,4]。有研究表明,巴戟天中寡糖类成分量较高,且具有较强的促进免疫和抗抑郁作用[5],为巴戟天主要有效成分之一。《中国药典》2010年版收载了巴戟天、巴戟肉、盐巴戟天和制巴戟天4种饮片规格,规定了药材按干燥品计算,含耐斯糖(C24H42O21)不得少于2.0%,但尚无巴戟天饮片的质量标准。
近年来,已有巴戟天药材指纹图谱研究的相关文献报道[6,7],但关于巴戟天不同炮制品的指纹图谱比较研究较少。鉴于巴戟天生品强筋骨、祛风湿力胜;盐炙后功专入肾,增强补肾助阳作用;甘草炙后增强补益作用,补肾益气养血,本实验对巴戟天生品及其不同炮制品各10批次饮片进行寡糖类成分HPLC-CAD指纹图谱比较研究,并进行相似度评价,为控制饮片质量及解析炮制机制提供一定的依据。
1 仪器与材料日本岛津LC—20AT高效液相色谱仪(SPD—M20A检测器,LC—20AB泵,SIL—20A自动进样器,CTO—20A柱温箱,CBM—20A系统控制器,LC Solution LC工作站),Corona CAD电雾式检测器(美国ESA公司),Shodex Asahipak NH2柱(250 mm×4.6 mm,5 μm,日本昭和仪器有限公司);METTLER AE240电子分析天平(瑞士Mettler公司);KQ—250DB型数控超声波清洗器(昆山市超声仪器有限公司);电热恒温干燥箱(上海市跃进医疗器械一厂)。
对照品果糖(批号100231,质量分数≥99.0%)、D-无水葡萄糖(批号110833,质量分数≥99.0%)、蔗糖(批号292-64121,质量分数≥99.0%),购于中国食品药品检定研究院;蔗果三糖(批号DCG6626,质量分数≥99.0%)、耐斯糖(批号292-64121,质量分数≥99.0%),购于日本Wako公司;蔗果五糖(批号120605,质量分数≥95.0%),购于Megazyme公司;乙腈为色谱纯(瑞典Oceanpak公司);水为娃哈哈纯净水;其他试剂均为分析纯。
巴戟天样品共10批,采自不同产地,来源分别为广西、福建永定、广东韶关、广东德庆、广东梅州、福建南靖、广西百色、广西苍梧、福建、广东普宁,编号分别为S1~S10,经辽宁中医药大学中药鉴定教研室翟延君教授鉴定,为茜草科植物巴戟天Morinda officinalis How. 的根,标本保存在辽宁中医药大学中药炮制工程技术研究中心。
2 方法与结果 2.1 样品制备巴戟天、巴戟肉、盐巴戟、制巴戟均按照《中国药典》2010年版所载制备方法制备,各10批。
生巴戟:取原药材,除去杂质及木心,洗净,晒干。
巴戟肉:取净巴戟天药材置蒸器内蒸透,趁热除去木心,切段干燥。
盐巴戟:取净巴戟天药材,用2%食盐水拌匀,闷润,待盐水被吸尽后蒸透,趁热除去木心,切段干燥。
制巴戟:取甘草煎汤,去渣,取净巴戟天药材,加药材量6%甘草汁同置锅内文火煮至甘草汁被吸尽,趁热除去木心,切段干燥。
2.2 色谱条件色谱柱为Shodex Asahipak NH2柱(250 mm×4.6 mm,5 μm),检测器为Corona CAD电雾式检测器,流动相为乙腈-水,梯度洗脱70 min(表 1),柱温25 ℃,进样量10 μL。CAD参数:气压241.36 kPa,量程100 pA。
|
|
表 1 流动相梯度洗脱条件 Table 1 Gradient conditions of mobile phase |
精密称取果糖、D-无水葡萄糖、蔗糖、蔗果三糖、耐斯糖和蔗果五糖对照品适量,加水配制成质量浓度分别为1.00、1.03、1.02、1.15、1.06、1.12 mg/mL混合对照品溶液。
2.3.2 供试品溶液制备精密称取生巴戟及不同炮制品粉末(过40目筛),各0.5 g,加醋酸乙酯30 mL,超声提取30 min,滤过弃去,挥干,残渣加70%乙醇50 mL,超声提取30 min,滤液于80 ℃水浴蒸干,残渣用水溶解定容至25 mL量瓶,0.45 μm微孔滤膜滤过,滤液作为供试品溶液。
2.4 方法学考察 2.4.1 精密度试验取同一份供试品溶液,连续进样6次,计算各色谱峰的相对保留时间和相对峰面积的RSD,结果显示,各色谱峰相对保留时间RSD在0.19%~2.89%,相对峰面积的RSD在0.07%~1.69%,均小于3%,表明仪器性能良好,符合指纹图谱的要求。
2.4.2 重复性试验取同一批次巴戟天粉末,平行制备6份供试品溶液,按上述色谱条件进样,计算各色谱峰相对保留时间和相对峰面积的RSD,结果显示,各色谱峰相对保留时间的RSD在0.19%~1.36%,相对峰面积的RSD在0.05%~1.42%,均小于3%,表明方法重复性良好,符合指纹图谱的要求。
2.4.3 稳定性试验取同一份供试品溶液,分别在0、2、4、8、12、24 h进样,按上述色谱条件进行测定,计算各色谱峰的相对保留时间和相对峰面积的RSD,结果显示,各色谱峰相对保留时间RSD在0.40%~2.51%,相对峰面积的RSD在0.37%~1.53%,均小于3%,表明供试品溶液在常温24 h之内稳定,符合指纹图谱的要求。
2.5 样品测定分别将10批次巴戟天生品、巴戟肉、盐巴戟和制巴戟按照“2.3.2”项下方法制备供试品溶液,取10 μL注入高效液相色谱仪,记录70 min色谱图,供试品色谱中以耐斯糖(S)的色谱峰的保留时间为1,计算共有峰的相对保留时间。色谱图见图 1。
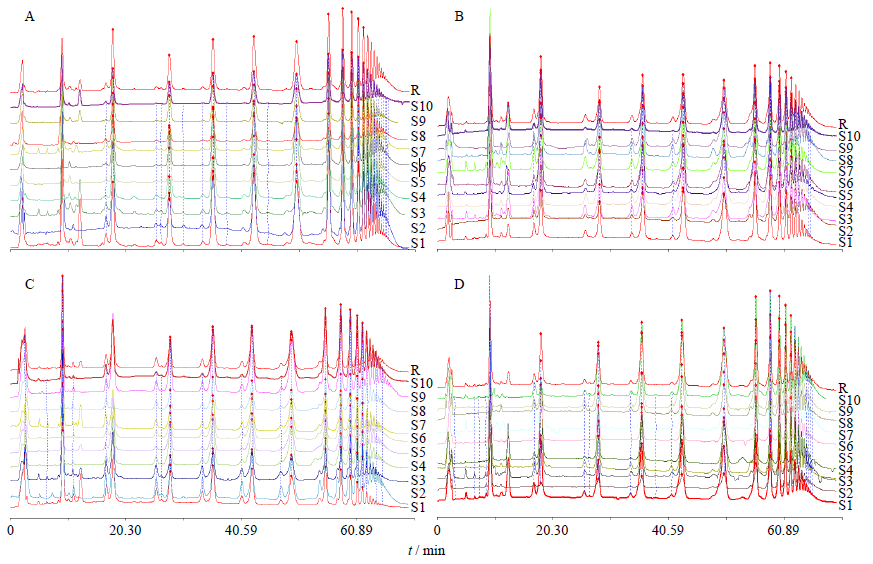 | 图 1 10批巴戟天生品 (A)、巴戟肉 (B)、盐巴戟 (C) 和制巴戟 (D) 的HPLC-CAD指纹图谱 Fig. 1 HPLC-CAD fingerprints of 10 batches of crude MOR (A),MORwithout duramen (B),salt-broiled MOR (C),and MOR Preaparatum (D) |
根据国家药典委员会《中药色谱指纹图谱相似度评价系统》,选取10批巴戟天生品的指纹图谱,以中位数法筛选峰面积,建立巴戟天生品对照指纹图谱。其中保留时间为(35±1)min的峰为耐斯糖的指纹峰,与相邻峰分离度较好,出峰位适中,其峰高与峰面积适中,故选定耐斯糖色谱峰为参照峰(S),标定10个共有峰,采用已知的对照品对共有峰进行指认,确定1~6号峰(1号峰为果糖,2号峰为葡萄糖,3号峰为蔗糖,4号峰为蔗果三糖,5号峰为耐斯糖,6号峰为蔗果五糖)为主要特征峰;巴戟肉、盐巴戟和制巴戟对照指纹图谱建立方法同生品,也确定10个共有峰,见图 2。
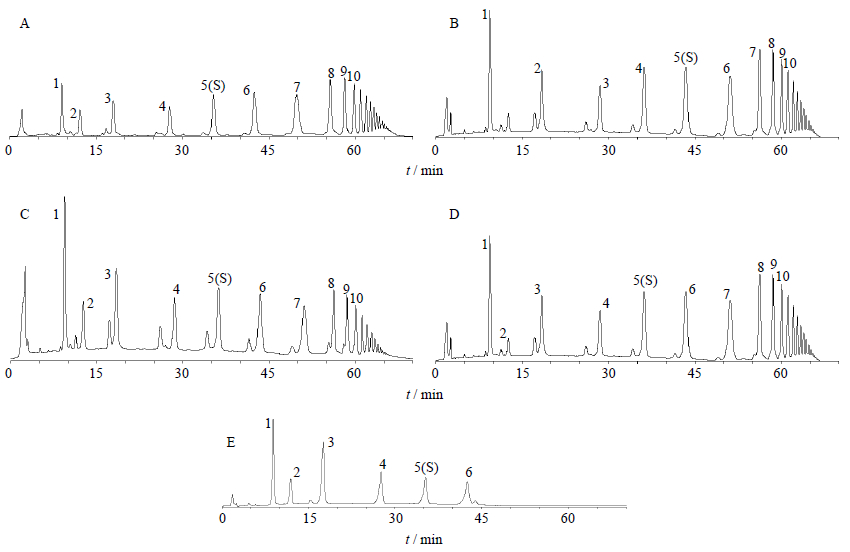 | 1-果糖 2-葡萄糖 3-蔗糖 4-蔗果三糖 5-耐斯糖 6-蔗果五糖 1-fructose 2-glucose 3-sucrose 4-1-kestose 5-nystose 6-1,1,1-kestopentaose图 2 巴戟天生品 (A)、巴戟肉 (B)、盐巴戟 (C) 和制巴戟 (D) 的对照指纹图谱及混合对照品 (E) 的HPLC色谱图 Fig. 2 Reference fingerprint of crude MOR (A),MOR without duramen (B),salt-broiled MOR (C),and MOR Preaparatum (D),and HPLC of mixed reference substances (E) |
参考《中药注射剂指纹图谱研究的技术要求(暂行)》[8]对指纹图谱进行相关技术参数的计算,结果显示,10批巴戟天生品(SS1~10)指纹图谱中共有峰的相对保留时间的RSD均小于0.38%;10批巴戟肉(RS1~10)指纹图谱中共有峰的相对保留时间的RSD均小于1.32%;10批盐巴戟(YS1~10)指纹图谱中,共有峰的相对保留时间的RSD均小于0.60%;10批制巴戟(ZS1~10)指纹图谱中共有峰的相对保留时间的RSD均小于0.20%。通过《中药色谱指纹图谱相似度评价系统》计算巴戟天生品、巴戟肉、盐巴戟天和制巴戟天指纹图谱相似度,结果见表 2~5。
|
|
表 2 10批巴戟天生品相似度 Table 2 Fingerprint similarity of 10 batches of crude MOR |
|
|
表 3 10批巴戟肉相似度 Table 3 Fingerprint similarity of 10 batches of MORwithout duramen |
|
|
表 4 10批盐巴戟相似度 Table 4 Fingerprint similarity of 10 batches of salt-broiled MOR |
|
|
表 5 10批制巴戟相似度 Table 5 Fingerprint similarity of 10 batches of MORPreaparatum |
通过对同一产地巴戟天(S4)炮制前后的特征图谱比较,研究发现巴戟天炮制品与原药相比,特征图谱差异很小。但其原药材经炮制后,主要成分量均有显著的增加,其中盐巴戟中寡糖类成分的量增加幅度最大。结果见表 6。
|
|
表 6 巴戟天生品与不同炮制品中寡糖测定结果 Table 6 Determination of oligosaccharides in crude MOR and MOR Preaparatum |
本实验中引入的电雾式检测器(CAD),又称荷电气溶胶检测器,是一种新型通用型检测器,基于其独特的检测原理,它不依赖于被检测物的化学结构,对不同结构的化合物有统一的响应,对无紫外吸收化合物的检测,与UV、折光指数检测器(RID)和ELSD相比,更加灵敏、准确。因此,巴戟天药材的寡糖类成分指纹图谱制备采用CAD检测器为宜。
本实验选用了Agilent、Dismond和Thermo C18色谱柱以及Shodex Asahipak NH2色谱柱,考察了甲醇-水(等度洗脱)、乙腈-水(等度洗脱)、乙腈-水(梯度洗脱),最终优选出了Shodex Asahipak NH2色谱柱,乙腈-水(梯度洗脱),能较好地使样品中各色谱峰分离且出峰最多。
果糖(1号峰)、葡萄糖(2号峰)、蔗糖(3号峰)、蔗果三糖(4号峰)和蔗果五糖(6号峰)均为巴戟天药材中的指标性成分,但耐斯糖(5号峰)在指纹图谱中峰位适中,峰形对称性好,相对稳定,且《中国药典》2010年版又选取耐斯糖为指标进行定量测定,因此选其作为参照峰。
通过对巴戟天药材及炮制品的HPLC指纹图谱的研究,可以看出巴戟天炮制前后其主要峰群有一定的相似性,表明巴戟天炮制后,其主要成分无明显变化。但是炮制品HPLC图谱共有峰1、2、3、4、5、6号峰面积增大,其原因是采用不同辅料炮制后,使溶出率改变。其中盐巴戟天中寡糖类成分量增加幅度最大,说明盐炙巴戟天有利于寡糖类成分的溶出,制巴戟天寡糖量较生品明显增加,可能是因为甘草中糖量也较高,起到了叠加的作用,巴戟肉寡糖量也明显高于生品,说明炮制时除去木心具有实验依据,具体原因及炮制过程中成分的变化有待结合药效学进行深入研究。
本实验首次建立了巴戟天不同炮制品寡糖类成分的HPLC-CAD特征图谱检测方法,该方法精密性、重复性良好,为巴戟天不同炮制品的鉴别及巴戟天加工炮制过程中的质量控制提供依据。因此,笔者建议巴戟天饮片质量标准研究应充分考察不同产地及生品与各炮制品之间的差异,建立科学、合理的质量评价体系。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | Masayuki Y, Shoko Y, Hirokonish I, et al. Chemical constituents of Chinese natural medicine, Morindae Radix, the dried roots of Morinda officinalis How.: Structures of morindolide and morofficinaloside [J]. Chem Pharm Bull, 1995, 43(9): 1462-1472. |
| [3] | 史 辑, 姜永粮, 贾天柱. 巴戟天属植物化学成分研究进展 [J]. 广州化工, 2009, 37(9): 46-51. |
| [4] | 朱孟勇, 赫长胜, 王彩娇. 巴戟天多糖对骨质疏松大鼠骨密度及血清微量元素的影 [J]. 中草药, 2010, 41(9): 1513-1515. |
| [5] | 徐超斗, 张永祥, 杨 明, 等. 巴戟天寡糖的促免疫活性作用 [J]. 解放军药学学报, 2003, 19(6): 466-468. |
| [6] | 程学仁, 罗文汇, 孙冬梅, 等. 巴戟天药材高效液相色谱指纹图谱初步研究 [J]. 中国药业, 2010, 19(13): 8-9. |
| [7] | 郭念欣, 李颖春, 蔡佳良, 等. 不同生长年限的巴戟天化学成分的指纹图谱 [J]. 中国实验方剂学杂志, 2011, 17(11): 65-68. |
| [8] | 中药注射剂指纹图谱研究的技术要求 (暂行) 的通知 [S]. 2001. |
 2014, Vol. 45
2014, Vol. 45


