2. 天士力制药集团股份有限公司, 创新中药关键技术国家重点实验室, 天津 300410;
3. 天津天士力之骄药业有限公司, 天津 300400
2. State Key Laboratory of Key Technologies of Innovation in Traditional Chinese Medicine, Tasly Pharm, Tianjin 300410, China;
3. Tianjin Tasly Pride Pharmaceutical Co., Ltd., Tianjin 300400, China
加味逍遥方最早源自宋代《太平惠民和剂局方》中逍遥散,在后世使用过程中,根据患者治疗情况,增加栀子和牡丹皮两味药从而形成新方,具有疏肝解郁、活血调经的作用[1]。临床上可用于治疗抑 郁[2, 3]、失眠[4]、妇科类疾病[5]。现有加味逍遥方质量控制的方法主要为薄层色谱法及指标性成分含量控制[6]。然而,加味逍遥方处方复杂,涉及十味药,目前暂时还无法通过控制提取物中的含量指标来全面控制质量。故可采用指纹图谱法,从整体上分析复杂化学物质的组成,是被国内外广泛接受的中药质量评价模式。目前中药指纹图谱的评价大多采用计算相似度的方法,主要包括夹角余弦法[7]、相关系数法[8]。本实验采用UPLC-UV指纹图谱,可较为全面表征加味逍遥方的成分,且具有快速、准确的优势。
1 仪器与试药Watets 超高效液相色谱仪-AcquityTM(美国 waters 公司),Empower色谱工作站,梅特勒分析百万分之一天平XP6,梅特勒电子分析天平ML503,梅特勒电子分析天平XS205(梅特勒公司),AS系列超声波清洗机(天津奥特赛恩斯仪器有限公司)。
加味逍遥提取为实验室自制产品,批号20150507、20150508、20150509、20150510、20150511、20150512、20150512、20150513、20150514、20150515,共10批。
对照品栀子苷(批号110749-201316)、芍药苷(批号110736-201438)和甘草苷(批号111610-201106)均购自中国食品药品检定研究院,供含量检测;甘草酸铵(EDQM)、苯甲酰芍药苷(批号20140419)、芍药内酯苷(批号20130825)由天津马克生物公司,供含量检测;乙腈为色谱纯(Merck公司),磷酸为色谱纯(天津市风船化学试剂科技有限公司),水为超纯水(MILLI-Q型超纯水器制备),其他试剂为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 供试品溶液的制备取加味逍遥提取物,精密称取0.15 g于10 mL量瓶,用超纯水定容,超声至提取物完全溶解,用0.22 μm的滤膜滤过,作为供试品溶液。
2.1.2 对照品溶液的制备精密称取栀子苷对照品,溶解于色谱甲醇中,配置成质量浓度为93.688 μg/mL的对照品溶液。
2.1.3 单味药水提取溶液制备按照药典药材比例进行单提,精密称取柴胡15 g、当归15 g、白芍15 g、白术15 g、茯苓15 g、甘草12 g、丹皮22.5 g、栀子22.5 g、薄荷3 g;、生姜5 g,分别加100 mL水,保持沸腾2.5 h,放冷,离心,过0.22 μm滤膜,即得单水提液。
2.2 色谱条件的确立 2.2.1 检测波长的确定200~400 nm全波长扫描,经比较后发现238 nm处基线平稳,出峰多,因此确定检测波长为238 nm。
2.2.2 流动相的选择本实验比较了甲醇-水、乙腈-水、乙腈-0.05%磷酸水溶液、乙腈-0.1%磷酸水溶液4种流动相洗脱系统,结果发现,乙腈-0.05%磷酸水溶液梯度洗脱时,色谱峰的峰形和分离度均较好,所以选择乙腈-0.05%磷酸水溶液作为流动相。洗脱梯度,见表 1。
| 表 1 液相梯度洗脱条件 Table 1 UPLC gradient elution conditions |
实验中考察了UPLCTM HSS T3色谱柱(100 mm×2.1 mm,1.8 μm)、UPLCTM BEH C18色谱柱(100 mm×2.1 mm,1.7 μm)和UPLCTM BEH Shield RP18色谱柱(50 mm×2.1 mm,1.7 μm),比较后发现,UPLCTM HSS T3色谱柱(100 mm×2.1 mm,1.8 μm)出峰多,分离效果较好,所以选择UPLCTM HSS T3色谱柱(100 mm×2.1 mm,1.8 μm)进行后续研究。
2.2.4 色谱条件的确立根据以上研究,最终确立的色谱条件为:采用超高效液相色谱法,以UPLCTM HSS T3色谱柱(100 mm×2.1 mm,1.8 μm)为分析柱,流动相为0.05%磷酸水溶液(A)-乙腈(B);柱温40℃,体积流量为0.3 mL/min,检测波长238 nm;进样量2 μL;分析时间29 min,结果见图 1。
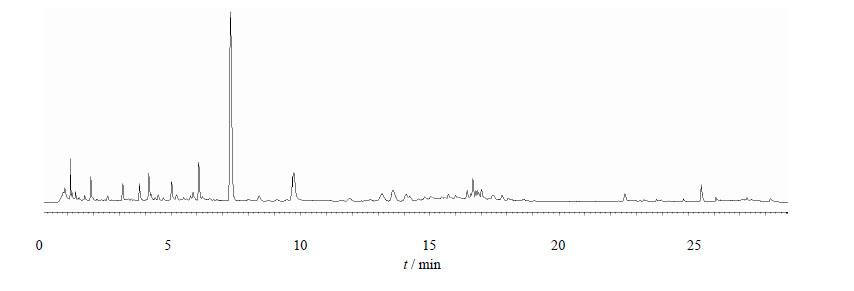 | 图 1 加味逍遥提取物逍遥散的指纹图谱 Fig. 1 UPLC fingerprint of extract of Modified Xiaoyao |
取同一供试品溶液(批号 20150507),按上述色谱条件,连续进样6次,相似度软件计算相似度,结果相似度值均大于0.98,表明色谱分析系统稳定,仪器精密度较好。
2.3.2 稳定性试验取同一供试品溶液(批号20150507),分别在0、1、2、4、8、12、24 h进行检测,用相似度软件计算相似度,结果相似度值均大于0.98,表明24 h内供试品溶液稳定。
2.3.3 重复性试验取同一批号制剂6份(批号20150507),制备供试品溶液,按上述色谱条件方法进行检测,6份供试品溶液测得的色谱指纹图谱,用相似度软件计算相似度,结果相似度值均大于0.98,表明重复性良好。
2.4 结果 2.4.1 样品指纹图谱采集分别精密吸取对照品溶液2 μL、供试品溶液2 μL,注入高效液相色谱仪,按上述色谱条件进行测定,记录色谱图。测定10批加味逍遥提取物的指纹图谱。
2.4.2 共有峰的确定根据10批加味逍遥提取物进样结果,对保留时间在2~25 min的色谱峰进行积分,选择吸收强,稳定性好,特征明显的色谱峰作为共有峰。8号峰(即栀子苷)因其在各批样品中含量较高,峰形稳定,与其他峰分离良好,选作内参比峰。以色谱峰对内参比峰的相对保留时间定性,通过筛选,共标定34个共有峰,见图 2。
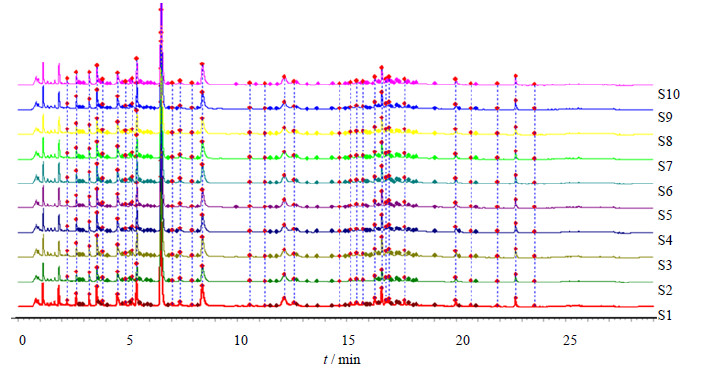 | 图 2 10批加味逍遥提取物的UPLC指纹图谱 Fig. 2 UPLC fingerprints of 10 batches of extract of Modified Xiaoyao |
采用国家药典委员会的中药色谱指纹图谱相似度评价系统(2012年版),对10批逍遥提取物的指纹图谱进行分析,以色谱峰的平均值建立对照指纹图谱,利用相关系数法计算指纹图谱的相似度。由于参照峰栀子苷的响应非常高,故分别计算了全谱峰匹配、34个共有峰匹配及33个共有峰匹配(去栀子苷),结果相似度值均不小于0.97,结果见表 2~4。
| 表 2 加味逍遥提取物10批全峰匹配相似度计算结果 Table 2 Similarity caculations of 10 batches of extract of Modified Xiaoyao |
| 表 3 加味逍遥提取物10批34个共有峰匹配相似度计算结果 Table 3 Similarity caculations of 10 batches of extract of Modified Xiaoyao of 34 common peaks |
| 表 4 加味逍遥提取物10批33个共有峰(去栀子苷)匹配相似度计算结果 Table 4 Similarity caculations of 10 batches of extract of Modified Xiaoyao of 33 common peaks (without geniposide ) |
共有峰归属认定利用平均值生成加味逍遥提取物的共有模式(图 3、4)。以《中国药典》2015年版加味逍遥散配方比例按“2.2”项下制备加味逍遥方各单味药及其对照组方的样品,用“2.2.4”项下色谱条件进样生成指纹图谱,以保留时间和紫外光谱确认各共有峰的来源(图 5)。来源于薄荷的是8、24、25号峰,来源于栀子的是1、2、3、4、5、6、 9、10、11、12、14、22、23、24、25、26、27、28号峰,来源于当归的是7、16号峰,来源于生姜的是30、34号峰,来源于丹皮的是7、8、15、17、29号峰,来源于甘草的是18、19、20、21、31、32、33号峰,来源于白芍的是13、15、29号峰。在加味逍遥提取物的10味药中,柴胡、茯苓、白术没有色谱峰显示在共有模式中,由于茯苓中的成分绝大部分为多糖,白术为挥发油和多糖,在此系统内无法出峰,而柴胡中含量较高的为皂苷,但在水提过程中降解或转化,所以这3味药物没有色谱峰出现。
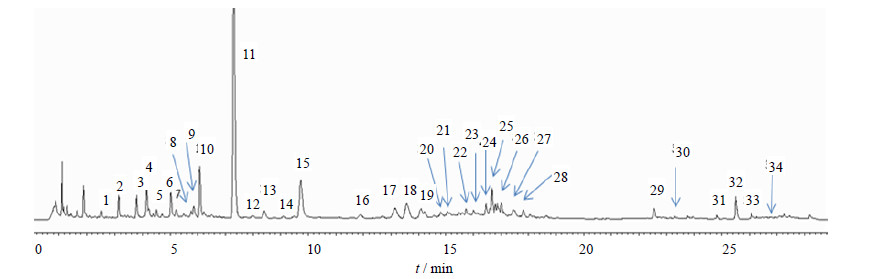 | 图 3 加味逍遥提取物对照指纹图谱 Fig. 3 UPLC reference fingerprint of extract of Modified Xiaoyao |
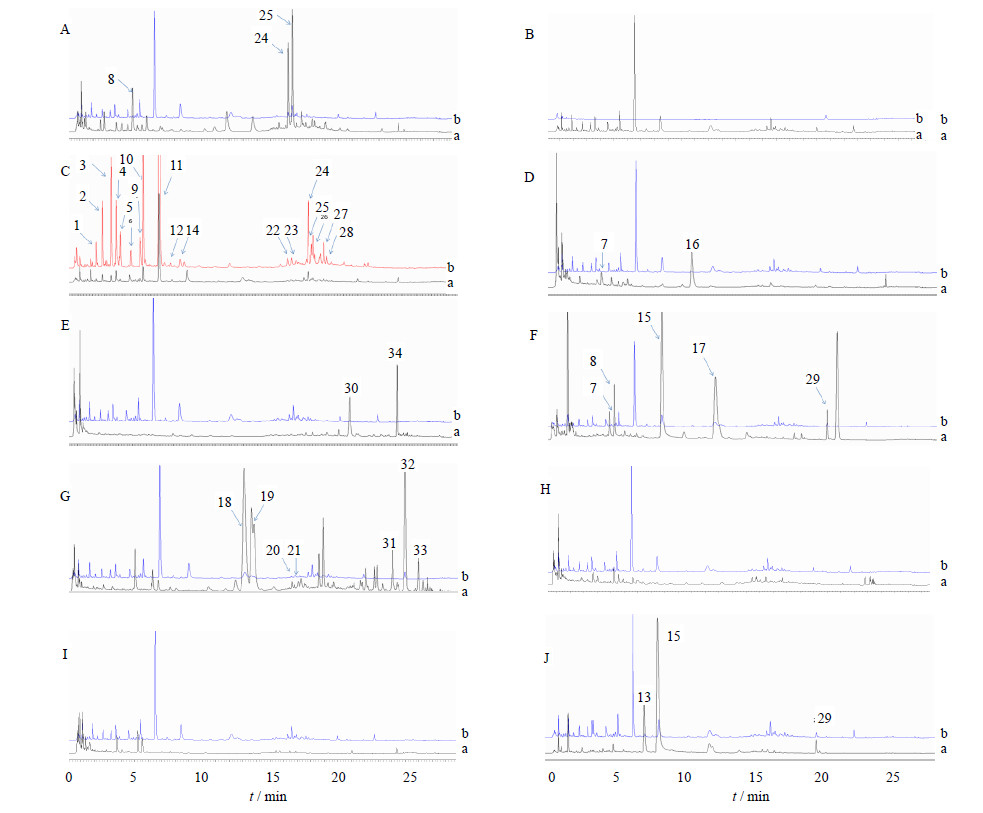 |
A-薄荷;B-茯苓;C-栀子;D-当归;E-生姜;F-丹皮;G-甘草;H-柴胡;I-白术;J-白芍;a为加味逍遥提取物色谱图;b为单水提药材色谱图 A-Menthae haplocalycis Herba; B-Poria; C-Gardeniae Fructus; D-Angelicae sinensis Radix; E-Zingiberis Rhizoma Recens; F-Moutan Cotex; G-Glycyrrhizae Radix et Rhizoma; H-Bupleuri Radix; I-Atractylodis macrocephalae Rhizoma; J-Paeoniae Radix alba; a-Chromatogram of extract of Modified Xiaoyao; b- Chromatogram of extract of single Chinese medicine 图 4 加味逍遥提取物与单味药对照色谱图 Fig. 4 UPLC of extract of Modified Xiaoyao and single Chinese medicine |
 | 图 5 各共有峰紫外光谱图 Fig. 5 UV spectrum of common peaks |
本实验建立了加味逍遥提取物UPLC指纹图谱,采用国家药典委员会的中药色谱指纹图谱相似度评价系统软件(2012年版),生成了加味逍遥提取物指纹图谱的共有模式,确定了34个共有峰,计算了10批加味逍遥提取物的指纹图谱的3种相似度,分别采用全谱匹配计算相似度,34个共有峰匹配计算相似度和33个共有峰(去栀子苷峰)计算相似度,结果3种相似度计算结果均大于0.97,说明栀子苷的大峰没有影响到指纹图谱的相似度计算,34个共有峰的相似度结果可信。
本实验明确了34个共有峰的药材归属,并通过标准品和LC-MS等方法确定了峰11、13、15、16、18、29、32、34分别为栀子苷、芍药内酯苷、芍药苷、阿魏酸、甘草苷、苯甲酰芍药苷、甘草酸和6-姜辣素,为加味逍遥方定量指标的选择和确定提供了参考。
对于加味逍遥方此类药味多、成分复杂的中药复方,仅通过含量检测难以全面的控制质量。指纹图谱中包含着大量反映复方的内在化学物质信息的数据和变量[9],虽无法对全含量进行检测,但可有效获取样品与样品的批间差异,较为全面的控制工艺过程中的质量。
| [1] | 焦少珍, 韩凤梅, 陈 勇. RP-HPLC法同时测定加味逍遥口服液中栀子苷、芍药苷和丹皮酚的含量[J]. 湖北大学学报(自然科学版), 2007, 02: 196-198. |
| [2] | 陈 琳. 加味逍遥胶囊治疗62例轻中度抑郁症气郁化火证临床疗效观察[D]. 北京: 北京中医药大学, 2014. |
| [3] | 马克信. 轻中度抑郁症伴焦虑有效方药的筛选与疗效评价[D]. 北京: 中国中医科学院, 2014. |
| [4] | 李 艳, 徐碧云, 肖 芳, 等. 加味逍遥散对心理应激性失眠患者睡眠的影响[J]. 中国中西医结合杂志, 2009, 03: 208-211. |
| [5] | 姜 华, 张武德. 加味逍遥散治疗妇科病的心得体会[J]. 中国中医药信息杂志, 2001, 06: 59-60. |
| [6] | 石勇强. 加味逍遥丸的制备与质量控制[J]. 医学信息(中旬刊), 2011, 01: 335-337. |
| [7] | 王龙星, 肖红斌, 梁鑫淼, 等. 一种评价中药色谱指纹谱相似性的新方法: 向量夹角法[J]. 药学学报, 2002, (9): 713-717. |
| [8] | 田润涛, 谢培山. 色谱指纹图谱相似度评价方法的规范化研究 (一)[J]. 中药新药与临床药理, 2006, (1): 40-42, 54. |
| [9] | 刘万仓, 孙 磊, 于孟琦, 等. 中药指纹图谱模式识别研究进展[J]. 国际药学研究杂志, 2010, 06: 446-450. |
 2016, Vol. 39
2016, Vol. 39


