2. 天津市工业微生物重点实验室, 天津 300457
2. Tianjin Key Laboratory of Industrial Microbiology, Tianjin 300457, China
高血脂症是指机体代谢或运转异常而造成的血浆中脂质含量高于正常水平的病理状态。随着人们生活习惯的改变,患高血脂病的人群呈逐年上升的趋势[1, 2]。此外,高血脂症还会诱发糖尿病、脂肪肝、动脉粥样硬化等多种并发症[3],严重影响人们的生活质量,因此高血脂症的研究治疗越来越受到人们的关注。
利拉鲁肽是诺和诺德公司研发的一种胰高血糖素样肽(GLP-1)受体激动剂。研究表明此药可改善β细胞功能、减轻患者体重、降低收缩压并改善血脂谱等心血管状况[4]。此外,临床应用及研究还提示利拉鲁肽还可降低食欲,延缓胃排空,由此减轻患者体质量[5, 6, 7],具有减肥降血脂功效。本实验通过建立高血脂小鼠模型,并给予低、高剂量利拉鲁肽及阴性(生理盐水)、阳性(辛伐他汀)对照药物,通过检测体质量、总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白(LDL-C)、高密度脂蛋白(HDL-C)等指标的变化,在动物水平上明确利拉鲁肽的调血脂及体质量控制作用。
1 材料 1.1 药品与试剂利拉鲁肽注射液(丹麦诺和诺德制药公司,批号CP50925,规格为3 mL׃18 mg);辛伐他汀片(山东鲁抗医药集团赛特有限责任公司,批号111203,规格20 mg/片);小鼠TC、TG、LDL-C、HDL-C体外诊断试剂盒(中生北控生物科技股份有限公司)。基础饲料和高脂饲料(中国人民解放军军事医学院实验动物中心)。
1.1.1 小鼠基础饲料组成成分基础饲料由北京华阜康生物科技有限公司提供,其主要营养成分见表 1。
| 表 1 基础饲料主要营养成分 Table 1 Major nutrition of normal fat diet |
基础饲料78.8%、猪油10%、蛋黄粉10%、胆固醇1%、基础饲料78.8%、脱氧胆酸盐0.2%
1.2 仪器H1650-W微量台式高速离心机(长沙高新技术产业开发区湘仪离心机仪器有限公司);Synergy4多功能酶标仪(BioTek公司);TXB2202L精密电子天平(上海燕恒实业有限公司)。
1.3 动物健康雄性6周龄SPF级昆明种小鼠40只,体质量18~22 g,动物合格证号:SCXK-(军)2009-003,由军事医学科学院卫生学环境医学研究所动物实验中心提供。小鼠置于笼内恒温饲养(24±1)℃,湿度50%~60%。饲养过程中,每天观察小鼠生长情况,补充饲料及饮用水。垫料每2~3天更换1次。每日自然光照。
2 方法 2.1 研究方法将40只小鼠用基础饲料正常饲养1周后,眼部取血,称体质量,根据体质量随机分为5组,分别为对照组、模型组、阳性组及利拉鲁肽低、高剂量组,每组8只。对照组给予基础饲料并ip生理盐水;模型组给予高脂饲料,并ip生理盐水;阳性组给予高脂饲料并ig辛伐他汀10 mg/kg;利拉鲁肽低、高剂量组给予高脂饲料并ip利拉鲁肽200、400 μg/kg[8, 9]。连续4周。实验期间,每天定量定点给粮,每周定时称体质量,密切观察小鼠的进食量及精神状态。末次给药后隔夜禁食,颈椎脱臼法处死小鼠,摘眼球取血。测定小鼠血清中TC、TG、LDL-C、HDL-C指标。
2.2 检测方法饲养4周后,检测小鼠体质量、血清中TC、TG、LDL-C、HDL-C水平。小鼠体质量用电子天平称取,血脂指标按试剂盒说明书操作。TC采用血清TC测定试剂盒(CHOD-PAP法),TG采用TG测定试剂盒(GPO-PAP法),LDL-C采用LDL-C测定试剂盒(直接法-表面活性剂消除法),HDL-C采用HDL-C测定试剂盒(直接法-过氧化氢酶清除法)。计算动脉粥样硬化指数(AI)及抗动脉粥样硬化指数(AAI)。
AI =(TC−HDL-C)/ HDL-C
AAI = HDL-C/TC
2.3 统计学方法所有数据采用SPSS 17.0统计学软件进行分析,计量资料采用表示,两独立样本比较采用t检验,多组间比较采用方差分析,组间两两比较采用LSD-t检验。
3 结果与分析 3.1 小鼠高脂模型的建立对实验结束时对照组与模型组进行比较,结果见表 2,小鼠饲喂高脂饲料28 d后,模型组血清TC、TG和LDL-C的浓度与对照组相比均明显升高,且差异极显著(P<0.01),此外血清HDL-C浓度有所降低,表明高脂血症小鼠模型的建立成功。
| 表 2 饲喂普通饲料与高脂饲料小鼠血脂的变化($\bar x \pm s$,n = 8) Table 2 Change of serum cholesterol in mice with normal fat diet and high fat diet($\bar x \pm s$,n = 8) |
高血脂症往往伴随着肥胖的发生,因此体质量的变化与药物的降血脂作用有着密切的关系。在实验过程中,每组小鼠都皮毛光滑,食欲正常,未出现异常状况,无自然死亡。每7天给小鼠称1次体质量,结果见表 3,在14 d以后,模型组与对照组比较差异显著,21 d时辛伐他汀组和利拉鲁肽低、高剂量组与模型组比较均差异显著,28 d时利拉鲁肽高剂量组与模型组比较出现了明显差异,这表明利拉鲁肽对降低高血脂小鼠的体质量有一定作用,且效果好于阳性对照药物辛伐他汀(10 mg/kg)。
| 表 3 利拉鲁肽对高脂血症小鼠体质量的影响($\bar x \pm s$,n = 8) Table 3 Effectof Liraglutide on body weight of mice with hyperlipemia($\bar x \pm s$,n = 8) |
为确定利拉鲁肽对高血脂小鼠的调血脂作用,本实验按照200、400 μg/kg的剂量、采用注射给药的方式连续给予模型小鼠利拉鲁肽4周后,眼部取血测定各项血脂指标。图 1-A结果表明与模型组小鼠相比,辛伐他汀组和利拉鲁肽低、高剂量组小鼠血清中TC、TG、LDL-C水平明显降低(P<0.05);与辛伐他汀组相比,利拉鲁肽低、高剂量组小鼠的TC、TG降低的更明显(P<0.01)。图 1-B结果显示,与模型组相比,辛伐他汀组和利拉鲁肽低、高剂量组小鼠血清中TC/HDL-C、TG/HDL-C和LDL-C/ HDL-C的比例均明显降低,表明利拉鲁肽可显著降低高血脂小鼠血清TC、TG、LDL-C等病理指标,具有很好的降血脂功效。与辛伐他汀组比较,利拉鲁肽低、高剂量组小鼠血清中LDL-C/ HDL-C明显降低,高剂量组TG/HDL-C也明显 降低。
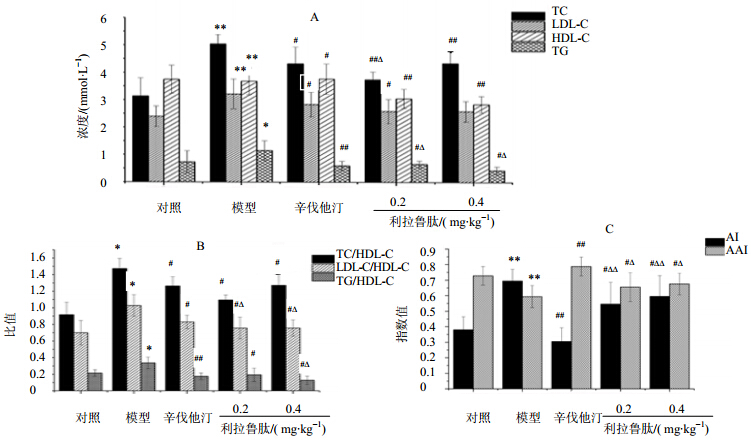 | A-对小鼠血清中TC、TG、LDL-C、HDL-C的影响;B-对TC/HDL-C、TG/HDL-C、LDL-C/HDL-C比值的影响; C-对动脉粥样硬化指数(AI)、抗动脉粥样硬化指数(AAI)的影响 与对照组比较:P<0.05,**P<0.01;与模型组比较:#P<0.05,##P<0.01;与辛伐他汀组比较:∆P<0.05,∆∆P<0.01 A- Effect of Liraglutide on serum TC,TG,LDL-C,and HDL-C levels in mice; B- Effect of Liraglutide on serum TC/HDL-C,TG/HDL-C,and LDL-C/HDL-C ratios in mice; C- Effect of Liraglutide on AI and AAI levels in mice P < 0.05,**P < 0.01 vs control group; #P < 0.05,##P < 0.01 vs model group; ∆P < 0.05,∆∆P < 0.01 vs simvastatin group图 1 利拉鲁肽对高血脂小鼠血脂水平的影响Fig. 1 Effect of Liraglutide on serum cholesterol in mice with hyperlipemia |
AI是一个衡量动脉硬化程度的指标,数值越高,代表硬化的程度越严重。研究表明[10, 11],TC、TG、LDL-C是动脉粥样硬化的危险因素,而HDL-C却是动脉粥样硬化的保护因素。通过计算得到的AI和AAI的数据见图 1-C。模型组的AI跟对照组相比,极显著性升高;辛伐他汀组的AI与模型组相比,极显著性降低;利拉鲁肽低、高剂量组的AI较模型组显著性降低;然而利拉鲁肽降低AI的程度没有辛伐他汀组好。结果表明辛伐他汀和利拉鲁肽均能显著降低AI,从而降低动脉粥样硬化发生的概率。
与对照组相比,模型组的AAI极显著降低;辛伐他汀组和利拉鲁肽高剂量组的AAI较模型组显著升高。表明辛伐他汀和利拉鲁肽均能显著性地提高AAI,对预防心血管疾病具有显著的效果。
4 讨论利拉鲁肽是一种GLP-1受体激动剂,在很大程度上与内源性GLP-1保持着相似的生物效应。而GLP-1是一种由肠道细胞产生及分泌的多肽激素,该激素以葡萄糖浓度相关性方式促进胰岛β细胞分泌胰岛素,并减少胰岛α细胞分泌胰高血糖素从而调节血糖水平,降低血糖[12, 13, 14]。同时GLP-1还具有保护β细胞的作用,刺激胰岛β细胞的增殖和分化,抑制胰岛β细胞凋亡,增加胰岛β细胞数量[15, 16],此外,GLP-1还可作用于胰岛α细胞,强烈地抑制胰高血糖素的释放,并作用于胰岛δ细胞,促进生长抑素的分泌,生长抑素又可作为旁分泌激素参与抑制胰高血糖素的分泌。有研究认为,GLP-1降血糖作用还包括抑制胃肠道蠕动和胃液分泌,抑制食欲及摄食,延缓胃内容物排空等[17, 18]。
利拉鲁肽是GLP-1的类似物,与人GLP-1具有97%同源性,是在GLP-1第34位将赖氨酸替换为精氨酸并在第26位增加了1个16碳棕榈酰脂肪酸侧链。与GLP-1相比,利拉鲁肽在皮下注射后形成胶束,有助于减缓DDP-4引起的降解速度,因此其对DPP-4和中性内肽酶(NEP)降解都很稳定,半衰期明显延长,仅需每日1次皮下注射就能起到良好的降糖作用。一些临床研究已提示利拉鲁肽很可能在改善2型糖尿病患者血糖平衡的同时,还具有降低血脂、减轻体质量的作用,这为肥胖症的治疗提供了一个非常好的前景。
本实验研究结果在动物水平上证实:利拉鲁肽可显著降低高血脂小鼠血清中TC、TG和LDL-C水平和减轻体质量,利拉鲁肽还能显著降低AI,提高AAI,降低动脉粥样硬化发生的概率,对预防心血管疾病具有显著的效果。从而为利拉鲁肽的临床合理应用及新型调血脂、减肥药物的研发提供了新的理论参考。
| [1] | 刘小燕, 林炳柱. 高龄体检血脂检验分析研究[J]. 中外医疗, 2014, 33(10):30-31. |
| [2] | 张晓红, 李奇临. 冀东油田体检人员体重指数与高血压病、高血脂和糖尿病的相关性分析研究[J]. 中国医学创新, 2013, 10(2):39-40. |
| [3] | 常凤, 李彦龙, 赵文艳. 黑龙江省中青年脑力劳动者血红蛋白、血糖、血脂、肝功能体检结果分析及运动干预对策研究[J]. 哈尔滨体育学院学报, 2012, 30(6):21-24. |
| [4] | 高妍. 调控β细胞, 直击糖尿病——GLP-1利拉鲁肽的基础与临床[J]. 中华内分泌代谢杂志, 2009, 25(6):增录6a-1-增录6a-4. |
| [5] | 安娜, 郑民浩, 祁晶晶, 等. 利拉鲁肽对超重和肥胖2型糖尿病患者的心血管保护[J]. 农垦医学, 2014, 36(1):6-11. |
| [6] | 母义明. 将试验结果转化为临床实践指导——利拉鲁肽研究的荟萃分析[J]. 中国糖尿病杂志, 2011, 19(5):398-400. |
| [7] | 张红. 利拉鲁肽治疗2型糖尿病的临床观察[J]. 中外医疗, 2012, 31(28):101-102. |
| [8] | Egefjord L, Gejl M, Moller A, et al. Effects of liraglutide on neurodegeneration, blood flow and cognition in Alzheimer's disease-protocol for a controlled, randomized double-blinded trial[J]. Dan Med J, 2012, 59(10):A4519-4520. |
| [9] | McClean P L, Parthsarathy V, Faivre E. The diabetes drug liraglutide Prevents degenerative processes in a mouse model of Alzheimer's Diaease[J]. Neurosci, 2011, 31(17):6587-6594. |
| [10] | 杨永宗. 中国动脉粥样硬化病理生理学研究近况[J]. 中国动脉硬化杂志, 2004, 12(4):481-489. |
| [11] | 王浩然, 于春江. 动脉粥样硬化发生机制及药物治疗的研究进展[J]. 首都医科大学学报, 2012, 31(6):828-833. |
| [12] | Fan Y, Dong L, Weizhi M, et al. GLP-1 biology and GLP-1 based antidiabetic therapy[J]. Journal of Chinese Pharmaceutical Sciences, 2013, 22(1):7-27. |
| [13] | 宋智慧, 王璐, 纪立伟, 等. GLP-1类似物在2型糖尿病中的临床应用进展[J]. 中国新药杂志, 2013, 22(5):542-546. |
| [14] | 王小彦, 王玉丽, 徐为人. 近几年治疗糖尿病热点靶点的研究进展[J]. 药物评价研究, 2012, 35(1):42-45. |
| [15] | Yonggan L. Changming C, Rong H, et al. GLP-1 is effect on function of the pancreatic bate cell[J]. Chinese Journal of Geriatric Care, 2008, 6(3):5-18. |
| [16] | Ulrich W, Guido H, Andreas W, et al. Pharmacological profile of lixisenatide:A new GLP-1 receptor agonist for the treatment of type 2 diabetes[J]. Regulatory Peptides, 2010, 164(2):58-64. |
| [17] | 郭智慧, 史丽萍. GLP-1与糖尿病的研究进展[J]. 河北联合大学学报:医学版, 2012, 14(1):40-43. |
| [18] | 王丽茹. GLP-1类似物治疗糖尿病的研究[J]. 中国煤炭工业医学杂志, 2011, 14(1):141-143. |
 2016, Vol. 39
2016, Vol. 39


