2. 浙江省药品化妆品审评中心, 浙江 杭州 310012
2. Zhejiang Province Medicine and Cosmetics Review Center, Hangzhou 310012, China
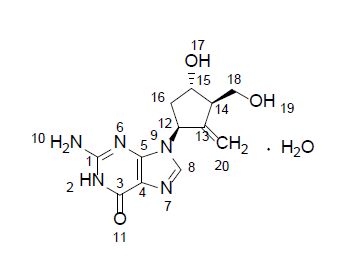
恩替卡韦(entecavir)是环戊酰鸟苷类似物,由百时美施贵宝(BMS)公司研发,2005年4月获得FDA批准用于乙型肝炎的治疗(图 1)。本品种各国药典中均未收载,样品贵重且对照品不易获取。使用质量平衡法测定样品含量时,需要测定样品HPLC纯度,水分含量、残留溶剂以及炽灼残渣等,消耗数克或更多样品,耗时5~7 d,使质量平衡法的应用受到一定限制。使用一种少量样品(少于100 mg),快速(小于1 h)的恩替卡韦含量测定方法就显得十分必要。
|
图 1 恩替卡韦结构 Fig. 1 Structure of entecavir |
氢核磁共振定量法(qNMR)已经在化学及药学等各方面得到广泛应用[1, 2, 3],中国、美国及英国等各国药典均收载此法[4, 5, 6]。qNMR测定样品含量时不需要对照品,无需引入校正因子,不受样品中水分及残留溶剂干扰,具有良好的应用前景。本文以恩替卡韦为样品,利用内标法,通过比较样品和内标的称样量,相对分子质量与相应的核磁响应信号峰面积,测定了恩替卡韦含量,并对这种方法进行了系统的方法学验证。
1 仪器与试药Ascend 500型核磁共振仪(瑞士布鲁克公司),14.1T超导磁体,5 mm双核z-梯度探头及Topspin3.2试验控制及数据处理软件;高效液相色谱AT30(Shimadzu);Mettler Toledo XP205电子天平。
恩替卡韦(BMS,批号6033331,HPLC测定质量分数99.5%),氘代DMSO(Sigma,北京金欧翔科贸公司分装),1,4-二硝基苯(TCI Chemical,质量分数>99.0%)。
2 方法与结果 2.1 样品溶液制备精密称取恩替卡韦及内标物质(1,4-二硝基苯)适量,置同一离心管中,精密加入2.0 mL氘代DMSO溶解,配制成浓度分别约为40 mmol/L的溶液,取约0.65 mL溶液转入5 mm核磁管中备用。平行配制5份样品。
2.2 实验条件采用zg30脉冲序列在恒温(25℃)下获取1H-NMR谱。具体试验参数设置如下:谱宽(SWH)10 000 Hz,射频中心频率(O1P)3089 Hz,采样点数(TD)64 K,采样时间(AQ)3.28 s,弛豫时间(D1)15 s,采样次数(NS)16,空扫次数(DS)2,增益(RG)81。
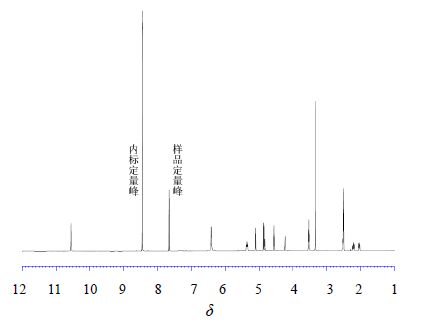
2.3 图谱测定结果采集图谱,采集样品和内标物质的核磁共振响应峰(图 2)。
|
图 2 恩替卡韦样品与内标物质的核磁共振响应峰 Fig. 2 NMR peaks of entecavir sample and internal standard |
1,4-二硝基苯与恩替卡韦均易溶于氘代N,N-二甲基甲酰胺,且1,4-二硝基苯的响应信号出现在δ8.45,与恩替卡韦的所有响应信号有良好的分离,互不干扰。于是将1,4-二硝基苯选为内标物。
2.5 方法学研究 2.5.1 线性关系表 1分别准确称取9.56、12.17、17.68、22.03、30.24 mg 的恩替卡韦和1,4-二硝基苯,制备 5个待测样品,按“2.2”项下试验条件测定1H-NMR谱,记录积分面积,以δ7.66处样品定量峰和δ8.45处内标峰面积比值为纵坐标,样品和1,4-对硝基苯质量比为横坐标做线性回归,回归方程为:y= 0.150 8x - 0.013 5,R2>0.999。恩替卡韦在0.03~0.12 mmol线性关系良好。
|
|
表 1 恩替卡韦的1H-NMR谱解析 Table 1 1H-NMR analysis of entecavir |
取供试品溶液,按“2.2”项下条件连续测定6次,记录积分面积,计算定量峰和内标峰面积比值,其相对标准偏差RSD=1.1%。
2.5.3 重复性平行配制3份样品,按“2.2”项下条件进行测定,以定量峰与内标峰面积比值计算恩替卡韦的平均含量为93.8%,RSD为0.7%。
2.5.4 稳定性取同一供试品溶液分别在0、1、4、12 h进行测定,比较恩替卡韦相应峰面积,RSD为1.05%,表明供试品溶液室温放置12 h稳定。
2.6 定量结果平行配制3份样品,采用δ7.66处恩替卡韦样品核磁共振响应信号与δ8.45处内标信号,按下式计算恩替卡韦质量分数。
| Ws(%)= | (As/ns)×Ms×mr | ×Wr×100% |
| (Ar/nr)×Mr×ms |
其中,As为恩替卡韦定量峰的峰面积,ns为恩替卡韦定量峰包含的质子数,Ms为恩替卡韦的分子量,Ar为内标的峰面积,nr为内标峰包含的质子数,Mr为内标的分子量,ms为称取的恩替卡韦质量,mr为称取的内标质量,Wr为内标的质量百分含量。经计算,样品中恩替卡韦含量分别为93.0%、94.3%和94.0%,平均含量为93.8%,RSD为0.70%,证明试验结果的重复性较好。
3 讨论 3.1 与其他含量测定结果比较为了验证核磁共振定量技术测定含量结果的准确性,本实验同时利用高效液相色谱法测定了恩替卡韦的含量。HPLC纯度为100.0%,卡氏水分仪测定样品中含水量为6.1%,炽灼残渣结果为0.06%。根据质量平衡法计算,样品中恩替卡韦(%)=(100%−水分−炽灼残渣)×HPLC纯度=93.8%,与qNMR定量结果一致。但是耗时从质量平衡法的数天减少至1 h,具有很大的优势。
3.2 仪器参数设定弛豫延迟时间(D1)是核磁共振定量试验中最重要的参数之一。D1每次脉冲发射前的等待时间,只有设定足够长的弛豫延迟时间才能使上次脉冲激发后的样品完全回到基态。短的弛豫延迟时间会影响积分结果,增加误差。Pauli等[7]提出,在氢核磁共振定量试验中,弛豫延迟时间应大于等于5倍的纵向弛豫时间(T1)。本实验利用inverse-recovery技术测定了样品中氢的纵向弛豫时间,结果均小于3 s,于是试验的弛豫延迟时间设定为15 s。试验表明结果良好。
为了定量分析的准确,氢核磁共振定量试验中的信噪比应在150:1以上。在实验条件下,扫描16次的信噪比大于200,满足定量要求。
3.3 积分方法实验发现,在核磁共振定量试验中,手动积分峰面积比自动积分更能真实反映试验结果,重现性更好。为了保证积分值的准确性,在手动调整相位后,以样品或内标响应峰与基线的重合处为起点和终点进行积分。
3.4 应用利用氢核磁共振定量技术测定恩替卡韦含量,无需使用对照品,样品制备过程简单,整个测定过程快速准确,结果可靠。这种方法可以作为常用的质量平衡法、含量法等的有效补充,有效应用于样品含量测定。
| [1] | Holzgrabe U. Quantitative NMR spectroscopy in pharmaceutical applications [J]. Prog Nucl Magn Reson Spectrosc, 2010, 57(2): 229-240. |
| [2] | 魏宁漪, 周 颖, 胡昌勤. 愈创木酚磺酸钾异构体的NMR定量分析 [J]. 中国药学杂志, 2011(12): 953-955. |
| [3] | 于小波, 沈文斌, 相秉仁. 定量核磁共振技术及其在药学领域中的应用进展 [J]. 药学进展, 2010(01): 17-23. |
| [4] | 中国药典. 二部 [S]. 2010 |
| [5] | USP35-NF30[S]. 2012. |
| [6] | BP 2013[S]. 2013. |
| [7] | Pauli G F, Godecke T, DC Jaki B U, et al, Quantitative 1H-NMR development and potential of an analytical method: an update [J]. J Nat Prod, 2012(75): 834-851. |
 2015, Vol. 38
2015, Vol. 38


