2. 天津中医药大学 中药学院, 天津 300193
2. College of Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
菊花为菊科菊属植物菊Chrysanthemum morifoliuin Ramat.的干燥花,既是名贵的观赏花卉也是药食同源植物。每年9~11月份菊花盛开时分批采收,阴干、焙干或熏蒸后晒干,菊花茶是喜闻乐见的健康饮品,菊花酒也是金秋时节必喝佳酿。中医理论认为菊花性甘、味苦,微寒;归肺、肝经;可散风,平肝明目,清热解毒。临床上菊花主要用于治疗风热感冒、头痛眩晕、目赤肿痛、眼目昏花及疮痈肿毒[1]。在多类中成药里菊花都为主要成分,如桑菊饮颗粒、杞菊地黄丸及菊花茶调散等;菊花还被制成大量的保健品供人们使用,如菊花药枕、菊花床垫等。菊花种类繁多,在药材市场上就有杭菊、亳菊、贡菊、滁菊、祁菊、怀菊、济菊和黄菊8大主流商品[2]。国内外对菊花的研究报道也非常多,为了进一步研究与开发利用该植物的,对近20年来国内外对菊花的化学成分、药理活性研究作一概述,尤其对菊花中所含有的萜类及有机酸类化合物进行了总结,为以后这两类化合物的药理学研究提供基础。
1 化学成分已有的研究表明菊花中主要含有黄酮、萜类及有机酸等化学成分。
1.1 黄酮类化合物菊花中所含的黄酮类化合物主要为黄酮类、黄酮醇类和二氢黄酮类。
1.1.1 黄酮类菊花中所含的黄酮类成分主要有金合欢素(1)[3]、金合欢素-7-O-β-D-葡萄糖苷(2)[4]、金合欢素-7-O-(6″-O-丙二酰基)-β-D-吡喃葡萄糖苷(3)[4]、金合欢素-7-O-半乳糖苷(4)[5]、刺槐苷(5)[4]、金合欢素-7-O-(3″-O-乙酰基)-β-D-吡喃葡萄糖苷(6)[6]、金合欢素-7-O-(6″-O-乙酰基)-β-D-半乳糖苷(7)[5],金合欢素-7-O-α-L-鼠李糖基-(1→6)[(2-O-乙酰基)-β-D-葡萄糖基-(1→2)]-β-D-葡萄糖苷(8)[7]、芹菜素(9)[3]、芹菜素-7-O-β-D-葡萄糖苷(10)[4]、芹菜素-7-O-(6″-O-丙二酰基葡萄糖苷)(11)[4]、芹菜素-7-O-葡萄糖醛酸苷(12)[4]、芹菜素-7-O-芸香糖苷(13)[4]、芹菜素-7-O-(6''-O-乙酰基)-β-D-葡萄糖苷(14)[5]、芹菜素-7-甲醚(15)[8]、木犀草素(16)[3]、木犀草素-7-O-β-D-葡萄糖苷(17)[4]、木犀草素-7-O-(6''-O-丙二酰基)-β-D-葡萄糖苷(18)[4]、木犀草素-7-O-葡萄糖醛酸苷(19)[4]、木犀草素-7-O-芸香糖苷(20)[4]、木犀草素-7,3′-二-O-β-D-葡萄糖苷(21)[4]、香叶木素-7-O-二-β-D-葡萄糖苷(22)[5]、木犀草素-4'-甲氧基-7-O-(6''-O-乙酰基)-β-D-葡萄糖苷(23)[6]、香叶木素(diosmetin,24)[9]、香叶木素-7-O-β-D-葡萄糖苷(25)[10]、香叶木素-7-O-葡萄糖醛酸苷(26)[4]、香叶木素-7-O-β-D-(6''-O-p-羟苯乙酰基)-葡萄糖苷(27)[9]、香叶木素-7-O-(6''-O-丙二酰基)-β-D-葡萄糖苷(28)[4]、香叶木素-7-O-半乳糖苷(29)[5]、香叶木素-7-O-(6''-乙酰基)-β-D-葡萄糖苷(30)[5]、香叶木素-7-O-β-D-(6''-O-丙二酸单酰)-葡萄糖苷(31)[11]、scolimoside(32)[9]、牡荆黄素-2-O-鼠李糖苷(33)[12]、异泽兰黄素(eupatilin,34)[13]、麦黄酮(tricin,35)[13]、5,7,3′,4′-四羟基-6,5′-二甲氧基黄酮(36)[13]、5,3′,4′-三羟基-6,7-二甲氧基黄酮(37)[14]。
1.1.2 黄酮醇类菊花中的黄酮醇类成分主要有槲皮素(38)[3]、槲皮素7-O-β-D-葡萄糖苷(39)[4]、槲皮素3-O-β-D-葡萄糖苷(40)[4]、槲皮素-7-O-(6''-O-丙二酰基)-β-D-葡萄糖苷(41)[4]、槲皮素3,7-二-O-β-D-葡萄糖苷(42)[4]、芦丁(43)[4]、槲皮素-7-O-半乳糖苷(44)[5]、槲皮素-3-O-半乳糖苷(45)[12]、栎素(46)[12, 15]、山柰酚(47)[12]、杨梅黄素(48)[12]、异鼠李素-3-O-β-D-半乳糖苷(49)[16]、六棱菊亭(artemetin,50)[17]、3,5-二羟基-4′,6,7,8-四甲氧基黄酮(51)[17]、蒙花苷(linarin,52)[18]等。
1.1.3 二氢黄酮类菊花中的二氢黄酮类化合物主要有柚皮素(53)[19]、柚皮素-7-O-β-D-葡萄糖苷(54)[4]、圣草酚(55)[5]、圣草酚-7-O-β-D-葡萄糖苷(56)[5]、圣草酚7-O-β-D-葡萄糖醛酸苷(57)[4]、橙皮素(hesperetin,58)[20]、橙皮苷(59)[21]等。
1.1.4 花色素类花色素类主要有花青色素3-O-(6''-O-丙二酰基)-β-D-葡萄糖苷(60)[22]、花青色素3-O-(3'',6''-O-二丙二酰基)-β-D-葡萄糖苷(61)[22]、花青色素3-O-β-D-葡萄糖苷(62)[22]。
1.2 萜类化合物菊花所含有的萜类化合物主要包括单萜、倍半萜和三萜等。
1.2.1 三萜类三萜类化合物涉及类型较多,主要有蒲公英烷(taraxastane)型、齐墩果烷(oleanane)型、乌苏烷(ursane)型、羽扇烷(lupane)型、taraxerane型、环木菠萝烷(cycloartane)型、大戟烷(tirucallane)型、达玛烷(dammarane)型、豆甾烷(stigmastane)型和羊毛烷(lanostane)型,部分化合物结构见图 1。
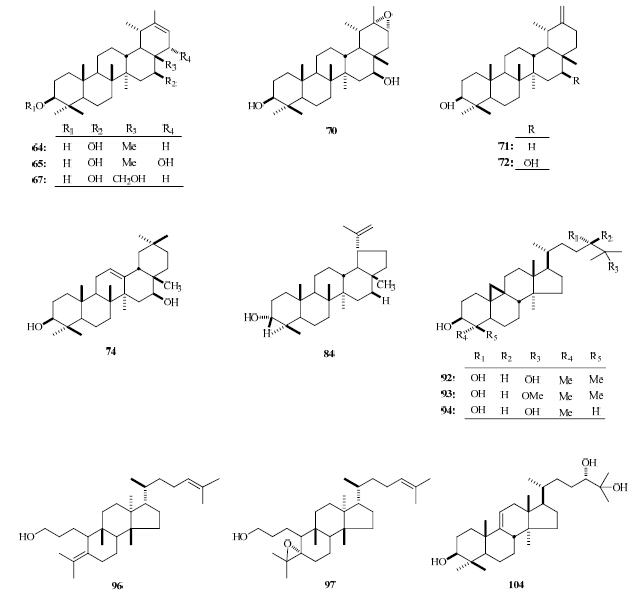 | 图 1 菊花中的萜类化合物Fig.1 Structures of triterpenes in C. morifoliuin |
蒲公英烷型化合物包括Ψ-蒲公英甾醇(63)[23]、款冬二醇(64)[23]、向日葵三醇C(65)[23]、22α-甲氧基款冬二醇(66)[23]、半日花三醇B0(67)[24]、棕榈酸16β,22α-二羟基假蒲公英甾醇酯(68)[20]、棕榈酸16β-羟基假蒲公英甾醇酯(69)[20]、款冬二醇α-环氧化物(70)[23]、蒲公英甾醇(71)[23]、阿里二醇(72)[23]。
齐墩果烷型化合物包括β-香树素(73)[23]、马尼拉二醇(74)[23]、高根二醇(75)[23]、龙吉苷元(76)[23]、齐墩果烯二醇(77)[23]、向日葵三醇A1(78)[24]。
乌苏烷型化合物包括α-香树精(79)[23]、熊果醇(80)[23]、榄香树脂醇(81)[23]、熊果酸(82)[18]。
羽扇烷型化合物包括羽扇豆醇(83)[23]、3-表羽扇豆醇(84)[23]、金盏菊二醇(85)[23]、向日葵三醇B2(86)[23]、棕榈酸16β,28-二羟基羽扇醇酯(87)[20]。
蒲公英赛烷(taraxerane)型三萜仅有蒲公英赛醇(88)[23]。
环木菠萝烷型化合物有环阿乔醇(89)[23]、24-亚甲基环木菠萝烷醇(90)[23]、24(R)-环菠萝烷-3β,24,25-三醇(91)[23]、24(S)-环菠萝烷-3β,24,25-三醇(92)[23]、24(S)-25-甲氧基环菠萝烷-3β,24-二醇(93)[23]、24(S)-29-去甲环菠萝烷-3β,24,25-三醇(94)[25]、24(S)-25-甲氧基环菠萝烷-3β,24,28-三醇(95)[25]。
大戟烷型化合物包括helianol(96)[23]、4,5α-epoxyhelianol(97)[23]、Δ7-甘遂醇(98)[23]。
达玛烷型型化合物包括达玛烷二烯醇(99)[23]、达玛烷二烯醇 Ⅱ(100)[25]、3-表南美楝属醇(101)[25]。
豆甾烷型化合物包括24(R)-海藻甾醇(102)[25]、24(S)-海藻甾醇(103)[25]。
从菊花里分得的羊毛烷型化合物有24(S)-lanost-9(11)-ene-3β,24,25-triol(104)[25]。部分新化合物的结构见图 1。
1.2.2 单萜类及倍半萜类除了三萜类化合物,菊花中还含有单萜及倍半萜类化合物。
单萜类化合物有1,8-桉叶素(105)[26]、莰酮(106)[26]、龙脑(107)[26]、α-侧柏酮(108)[26]、p-甲基异丙基苯(109)[26]、桃金娘烯醇(110)[26]、β-蒎烯(111)[26]等。
倍半萜类化合物包括cumambrin-A(112)[13]、野菊花内酯(113)[13]、7-(2-hydroxy-2-propyl)- 10-methyl-4-methyleneperhydro-naphthalene-3,5,6-triol(114)[13]、α-金合欢醇(115)[12]、金合欢烯(β-farnesene,116)[26]、野菊花四醇(chrysanthetetrol,117)[27]、野菊花三醇A(chrysantetriol A,118)[27]等。
1.3 有机酸类菊花所含的有机酸类化合物包括4,5-二-咖啡酰基奎宁酸(119)[5]、4-咖啡酰基-5-阿魏酰基奎宁酸(120)[5]、5-芥子酰基奎宁酸(121)[5]、绿原酸(122)[11]、咖啡酸(123)[5]、咖啡酸甲酯(124)[28]、咖啡酸乙酯(125)[21]、咖啡酸丁酯(126)[21]、macranthoin F(127)[11]、奎宁酸(128)[5]、4-O-咖啡酰基奎宁酸(129)[21]、1,3-O-二咖啡酰奎宁酸(130)[11]、3,4-O-二咖啡酰基奎宁酸(131)[21]、3,5-O-二咖啡酰奎宁酸(132)[11]、4-甲氧基桂皮酸(133)[28]等。
1.4 其他类除上述主要成分外,菊花中还含有少量蒽醌类、脂肪酸、脂肪醇类和微量元素等物质。
2 药理作用中医理论认为菊花具有清热解毒、疏散风热、平肝明目之功效。现代药理学研究主要集中在保护心血管、抗肿瘤、调血脂等方面,其对肝的保护作用[29]、镇痛作用是近年来的新发现。
2.1 对心血管系统的作用俞浩等[30]将滁菊总黄酮(总黄酮量为76.38%)配置成40、20、10 mg/(kg·d)高中低剂量连续喂饲Wista大鼠5 d后,接着对大鼠进行心肌缺血再灌注损伤(MIRI)处理。与模型组相比,高中低剂量组能显著减小MIRI大鼠心肌梗死范围(P<0.01),升高血清和心肌组织中超氧化物歧化酶(SOD)的活性(P<0.01),降低大鼠全血黏度,可下降血液中丙二醛(MDA)的量(P<0.01),降低血清中肌酸磷酸激酶(CK)、乳酸脱氢酶(LDH)的活性(P<0.01)。因此认为菊花总黄酮可对抗缺血再灌注引起的心肌损伤,能抑制MIRI引起的脂质过氧化损伤,有效防止血栓形成,从而促进MIRI的恢复。
汝海龙等[31]研究杭白菊总黄酮(TFCM)对离体血管环的收缩作用时发现,当TFCM在0.001~0.3 g/L时对1×10-5 mol/L苯肾上腺素和120 mmol/L KCl所引起的无内皮和有内皮血管环收缩均有抑制作用,与对照组相比差异显著(P<0.01),而且发现TFCM的抑制作用随浓度的增高而增强,各浓度之间对血管收缩的抑制作用有显著差异(P<0.01);相同浓度的TFCM对无内皮和有内皮血管组的收缩抑制作用也有显著差异(P<0.01)。杭白菊总黄酮具有一定的输张血管作用,这可能与其既对受体依赖性钙通道有明显抑制作用,又对电压依赖性钙通道有一定的抑制作用有关,这一机制需要更深入的研究。
2.2 抗肿瘤有研究发现菊花根中所含有的4-甲氧基桂皮酸、(1S,2S)-1,2,3-trihydroxy-1-(3,4-methylenedioxy- phenyl)-propane、咖啡酸甲酯和刺槐素均具有细胞毒活性,通过抑制肿瘤细胞的生长而发挥抗肿瘤作用[28]。研究人员分别在人肺癌A549细胞、皮肤黑色素瘤SK-MEL-2和小鼠黑色素瘤B16F细胞株的培养基中分别加入2.25~112.201 mg/mL的(1S,2S)-1,2,3-trihydroxy-1-(3,4-methylenedioxyphenyl)- propane、咖啡酸甲酯、刺槐素和4-甲氧基桂皮酸,对照组加入等量的培养基,在25 ℃条件下培养24 h,观察细胞生长情况。结果,与对照组比较(1S,2S)-1,2,3-trihydroxy-1-(3,4-methylenedioxyphenyl)- propane和咖啡酸甲酯具有抑制肿瘤生长的活性,活性浓度为2.25~65 µg/mL,当4-甲氧基桂皮酸和刺槐素的浓度低于40 µg/mL时对肿瘤细胞株无抑制作用。
林忠宁等[32]发现菊花倍半萜烯内酯类的活性成分parthenolide具有诱导人鼻咽癌细胞毒性和凋亡的作用。研究人员将10~100 µmol/L的parthenolide与鼻咽癌细胞系CNE1作用6~36 h后,再与阴性对照组比较,发现CNE1细胞LDH漏出率明显增加,细胞增殖抑制率升高(P<0.05);细胞出现凋亡特征形态学改变,癌细胞失贴壁率明显增高(P<0.05),证明菊花中的parthenolide对人鼻咽癌细胞的生长具有一定抑制作用,这与其破坏癌细胞膜的完整性、抑制细胞的增殖、介导细胞毒效应有关。
2.3 免疫调节马力[33]分离SD雄性大鼠肠道淋巴细胞,将细胞分成菊花多糖组、绿原酸组及对照组。分别在细胞培养液中加入0.5、1.0、2.0 mg/mL菊花多糖及等量的绿原酸,对照组加入等量的培养液。将淋巴细胞于培养箱孵育48 h后观察其生长情况,并将上清液取出进行肿瘤坏死因子-α(TNF-α)、γ-干扰素(INF-γ)的检测。与对照组比较,菊花多糖及绿原酸高中低剂量组均能提高淋巴细胞上清液中TNF-α、INF-γ的量,并且差异显著(P<0.01),高剂量组对淋巴细胞分泌TNF-α、INF-γ的促进作用最强。实验结果表明,菊花多糖及绿原酸可刺激肠道淋巴细胞分泌TNF-α、INF-γ,提高细胞免疫,从而发挥免疫调节作用。
2.4 抑菌菊花根的提取物通过抑制细菌的生长,改变细菌细胞的渗透压而达到广谱的杀菌活性[28]。将含有4-甲氧基桂皮酸40 mg的溶液分别加入到革兰阳性菌、革兰阴性菌的培养基中,对照组加入等量的培养基,在25 ℃培养72 h后观察细菌生长情况。与对照组相比,4-甲氧基桂皮酸能抑制革兰阳性菌、革兰阴性菌的生长,抑菌范围为9.4~12.6 mm。相同方法测试了菊花根中所含有的(1S,2S)-1,2,3-trihydroxy-1-(3,4-methylenedioxyphenyl)-propane和刺槐素对念珠菌的抑菌请况,结果与对照组相比此2种化合物对念珠菌属显示出了较强的抑制活性,其抑菌范围分别为9.5~13、9~12 mm。从实验结果中能得出菊花提取物可破坏细菌的细胞膜从而改变细菌内部的渗透压,破坏细菌的生长,从而达到抑菌的作用。
2.5 保护红细胞膜胡春等[34]以离体人红细胞膜为材料,借助1,6-二苯基-1,3,5-己三烯和8-苯胺基-1-萘磺酸铵荧光探针技术,发现菊花提取物对细胞膜流动性具有保护作用;试验中将菊花水提取液(以芦丁计的黄酮浓度9.1 mg/mL)3、9、12 µL加入到被超氧阴离子损伤的人红细胞膜体系中,通过计算膜流动性的恢复率,得出3种剂量的结果都呈显著的正相关;同时发现随着菊花提取物浓度的增加,红细胞膜的流动性增强。这与菊花提取物中黄酮等小分子能有效地进入红细胞膜区的内部,修复超氧阴离子损伤的细胞膜,从而改变膜的流动性有关,这一特性优于SOD等酶抑制剂,在对抗生物膜过氧化的应用中很有价值。
2.6 抗疲劳利用小鼠持续游泳实验,胡春等[35]将小鼠分成服用菊花提取物高、中、低(1.2、0.8、0.4 mL/kg)剂量组与0.5 mL蒸馏水空白组,ig给药10 d后进行持续游泳实验,记录各鼠的持续游泳时间。与对照组比较,发现菊花提取物高中剂量组可使小鼠的游泳时间增长(P<0.01或P<0.05),其中高剂量组小鼠游泳时间比空白组提高2.2倍,中剂量组小鼠游泳时间比空白组提高1.6倍。在相同的实验基础上又进行了小鼠常压耐缺氧实验,结果显示,菊花提取物高剂量组能延长小鼠生存时间,但中低剂量组均未见此结果。菊花提取物可提高实验小鼠抗疲劳的能力,服用菊花提取物一段时间后组织耗氧量下降,对非特异性因素的抵抗能力具有一定的提高。这主要可能与它消除超氧阴离子自由基、提高运动耐受性有关,其更详细的作用机制还需要更深入的研究。
2.7 调血脂胡春等[35]、于善凯等[36]在研究菊花降血脂作用的过程中发现,对高脂饲料喂养的大鼠给予菊花提取物后,发现大鼠血清总胆固醇恢复到基础值并能抑制三酰甘油升高;而对正常饲料喂养的大鼠,菊花提取物可以保持血清总胆固醇基本不变,提高有保护作用的高密度脂蛋白(HDL)、降低有危害作用的低密度脂蛋白(LDL)的浓度,提示菊花提取物对预防高血脂疾病具有重要意义。根据以上实验结果,可以将菊花用于日常生活中,作为预防和治疗高血脂疾病的辅助手段。
2.8 抑制高脂型脂肪肝形成崔艳[37]将雄性昆明种小鼠随机分成正常对照组、脂肪肝模型组、菊花提取物75、150、300 mg/kg组及阳性对照药非诺贝特胶囊40 mg/kg组,每组小鼠10只。除正常对照组外其余组小鼠连续6周ig高脂乳剂,同时除正常对照组和脂肪模型组灌服等量0.5%CMC-Na外其余各组小鼠灌服相应的药物溶液0.2 mL/10 g,连续6周。之后,将各组的10%肝组织匀浆液进行TC、TG及游离脂肪酸(FFA)测试。将测试结果与正常对照组比较,菊花提取物能降低高脂性脂肪肝模型组小鼠肝组织中TC和TG含量,尤其150、300 mg/kg组的作用更加明显(P<0.05);FFA没有显著性差异;与对照组相比,菊花提取物还能降低高脂性脂肪肝模型组小鼠血清中TC和TG水平,尤其是150、300 mg/kg组对TC水平有明显降低作用(P<0.05),但对FFA水平反而有升高作用。菊花提取物能降低肝组织中的TC和TG含量,可使小鼠肝组织脂肪变性的程度明显减轻,可抑制脂肪肝的形成。
2.9 镇痛张培培[38]采用小鼠扭体法来研究滁菊总黄酮的镇痛作用。将昆明种小鼠随机分成6组:生理盐水组、阳性对照药吗啡组(4 mg/kg)和阿司匹林组(40 mg/kg)、滁菊总黄酮剂量分别为50、100、200 mg/kg组,每组10只。除吗啡组为ip一次给药外,其他各组小鼠分别ig生理盐水或受试药1次/d,连续5 d。最后1次给药60 min后,给小鼠ip 0.6%冰醋酸0.2 mL,致使小鼠产生扭体反应。以15 min内发生小鼠扭体总数,作为疼痛指标,并对扭体反应的抑制率进行计算。结果,与对照组相比,滁菊总黄酮100、200 mg/kg可明显减少小鼠扭体反应数(P<0.01),最大抑制率达45.2%,可见将滁菊总黄酮全身给药具有一定的镇痛作用。接下来,研究人员在小鼠的脑侧室分别注射吗啡、滁菊总黄酮及阿司匹林,与对照组相比,5、10 mg/kg滁菊总黄酮可明显减少0.6%冰醋酸诱发的小鼠扭体反应,抑制率达52%,吗啡组达100%,阿司匹林组无明显影响。综合上述实验结果,可得出滁菊总黄酮有明显的镇痛作用,且镇痛作用至少有部分中枢机制参与,但其详细的作用机制还需更深入的研究。
2.10 其他作用Nishina等[39]研究发现菊花的绿原酸与金合欢素能微弱地刺激神经轴突的生长,此作用弱于对照组神经生长因子NGF,但是也具有重要意义。SB203580酶是P38丝裂素活化蛋白激酶通路(P38MAPK)的抑制剂,此酶在绿原酸与金合欢素的刺激下,作用于PC12细胞,能够强烈的促进神经轴突的增长。Wang等[40]研究菊花中的香叶木素能抑制黑色素的沉着,可能成为黑色素沉着症的潜在治疗药物。
3 结语迄今为止,国内外学者对菊属植物亳菊、滁菊、杭菊及贡菊等的研究已经取得了不少进展,并发现对菊花功效的认识传统中医与现代药理研究具有相同之处。传统中医认为菊花解热解毒,如今菊花用于抗菌、抗肿瘤及镇痛的较多,其清肝明目的药理作用与抑制高脂肪性脂肪肝相呼应。
不同品种的菊花,其功效各有侧重。有人总结文献显示,贡菊中总黄酮和绿原酸的含量都高于其他3种药用菊花[39]。学界认为绿原酸是抗菌有效成分[27],而黄酮类化合物具有保护心血管的作用[28]。贡菊在保护心血管、抗菌活性上可能优于其他3种药用菊花。通过GC-MS分析,杭菊挥发油成分较少,反映在感官品质上就是杭菊的气味较淡。贡菊中挥发油的总量虽然不高,但其组成成分中,莰酮的含量很高,这与贡菊的柔和、清凉、清新和淡雅的风味特征相印证。滁菊和毫菊中挥发油含量较高[41],而且含有较多的萜类物质,如1,8-桉叶素、樟脑、莰酮等,分析结果与这2种药菊强烈的中药气味特征相吻合。另外,贡菊还含有很多萜类及其含氧衍生物、烷烃类、烯烃类,这些物质的存在不仅增强了贡菊的药用价值,而且丰富了其感官品质。因此,从已有文献资料看,贡菊较其他3种菊花可能不仅更适合药用,同时适于作为饮料、功能和保健食品开发的原料。但是,现有的8种菊花商品的物质基础与功效关系,还需要进行深入研究。
菊花中的主要成分为黄酮、萜类以及有机酸,但药理作用的研究主要集中在黄酮类化合物,对其所含有的萜类等物质的研究鲜有报道。萜类等其他成分具有多种药理活性[40],因此对菊花中萜类等主要成分的研究可成为今后研究的重点,能扩大菊花这一传统中药的实用范围,并且为新药研发提供新的前体化合物。
另外,菊花的保肝及镇痛作用是近年来的新发现,如果对其作用机制进行更深入研究,不仅能推广其在临床上的应用,还有可能研制出新的功能性药物。
对菊属植物菊花主要研究的药用部位为干燥的花,对其秸秆、叶等其他部位的研究尚不多见。菊花秸秆、叶能否代替花入药,从而扩大菊属植物的使用范围及药用部位,提高现有药用植物资源的再生能力和内在质量,需要有进一步的化学、药理学以及分子生物学等多学科的交叉研究进行支持。
| [1] | 中国药典[S]. 一部. 2010. |
| [2] | 张晓媛, 段立华, 赵 丁. 菊花化学成分及药理作用的研究[J]. 时珍国医国药, 2008, 19(7): 1702-1704. |
| [3] | Miyazawa M, Hisama M. Antimutagenic activity of flavonoids from Chrysanthemum morifolium[J]. Biosci Biotechnol Biochem, 2003, 67(10): 2091-2099. |
| [4] | Schwinn K E, Markham K R, Giveno N K. Floral flavonoids and the potential for pelargonidin biosynthesis in commercial Chrysanthemum cultivars[J]. Phytochemistry, 1994, 35(1): 145-150. |
| [5] | Lin L Z, Harnly J M. Identification of the phenolic components of chrysanthemum flower (Chrysanthemum morifolium Ramat)[J]. Food Chem, 2010, 120(1): 319-326. |
| [6] | Zhang J, Ding A W. Two new flavonoid glycosides from Chrysanthemum morifolium[J]. Chin Chem Lett, 2006, 17(8): 1051-1053. |
| [7] | 沈一行, 陈建民. 北野菊黄酮类成分研究[J]. 药学学报, 1997, 32(6): 451-454. |
| [8] | 姜洪芳, 张 玖, 单承莺. 亳菊花中黄酮类化合物的分离鉴定[J]. 中国野生植物资源, 2008, 27(5): 50-52. |
| [9] | Xie Y Y, Yuan D, Yang J Y, et al. Cytotoxic activity of flavonoids from the flowers of Chrysanthemum morifolium on human colon cancer colon 205 cells[J]. J Asian Nat Prod Res, 2009, 11(9): 771-778. |
| [10] | 邹文韬, 张因皎, 俞菊红, 等. 杭白菊中黄酮类化合物的分离与鉴定[J]. 浙江理工大学学报, 2010, 27(1): 140-144. |
| [11] | Wang S, Hao L J, Zhu J J, et al. Study on the effects of sulfur fumigation on chemical constituents an antioxidant activity of Chrysanthemum morifolium cv. Hang-ju[J]. Phytomedicine, 2014, 21(5): 773-779. |
| [12] | Sun Q L, Hua S, Ye J H, et al. Flavonoids and volatiles in Chrysanthemum morifolium Ramat flower from Tongxiang County in China[J]. Afr J Biotechnol, 2010, 9(25): 3817-3821. |
| [13] | 张 聪, 秦民坚, 王 玉. 野菊花的化学成分[J]. 药学与临床研究, 2009, 17(1): 39-41. |
| [14] | 李青杰. 野菊花的化学成分研究[J]. 临床合理用药杂志, 2011, 4(17): 65-66. |
| [15] | Yun X J, Shu H M, Chen G Y, et al. Chemical constituents from barks of Lannea coromandelica [J]. Chin Herb Med, 2014, 6(1): 65-69. |
| [16] | 金海红. 酵母细胞壁多糖对抗白菊抗氧化活性和黄酮类物质合成积累的影响[D]. 杭州: 浙江工商大学, 2011, 1-61. |
| [17] | 顾瑶华, 秦民坚. 亳菊的化学成分研究[J]. 中草药, 2006, 37(12): 1784-1786. |
| [18] | 杨念云, 任爱农, 胡万春, 等. 菊花脑嫩茎叶的化学成分[J]. 中国药科大学学报, 2005, 36(5): 402-404. |
| [19] | Zang H J, Kang M Q, Zhang H Q, et al. Matrix solid phase dispersion extraction for determination of flavonoids in the flower of Chrysanthemum morifolium Ramat. by capillary zone electrophoresis[J]. Anal Methods, 2014, 6: 766-773. |
| [20] | 胡立宏, 陈仲良. 杭白菊的化学成分研究: 两个新三萜酯的结构测定[J]. 植物学报, 1997, 39(1): 85-90. |
| [21] | 胡立宏, 陈仲良. 杭白菊的化学成分研究: 正戊基果糖甙的结构测定[J]. 植物学报, 1997, 39(2): 181-184. |
| [22] | Nakayama M, Koshioka M, Shibata M, et al. Identification of cyanidin 3-O-(3″,6″-O-Dimalonyl-β- glucopyranoside) as a flower pigment of chrysanthemum (Dendranthema grandiflorum)[J]. Biosci Biotechnol Biochem, 1997, 61(9): 1607-1608. |
| [23] | Akihisa T, Franzblau S G, Ukiya M, et al. Antitubercular activity of triterpenoids from Asteraceae flowers[J]. Biol Pharm Bull, 2005, 28(1): 158-160. |
| [24] | Ukiya M, Akihisa T, Tokuda H, et al. Constituents of compositae plants: III. Anti-tumor promoting effects and cytotoxic activity against human cancer cell lines of triterpene diols and triols from edible chrysanthemum flowers[J]. Cancer Lett, 2002, 177(1): 7-12. |
| [25] | Ukiya M, Akihisa T, Yasukawa K, et al. Constituents of compositae plants 2. Triterpene diols, triols, and their 3-O-fatty acid esters from edible chrysanthemum flower extract and their anti-inflammatory effects[J]. J Agric Food Chem, 2001, 49(7): 3187-3197. |
| [26] | 芦金清, 李 竣. 神农香菊的挥发油化学成分[J]. 中国中药杂志, 2002, 27(8): 598-599. |
| [27] | 汪国鹏. 野菊花有效组分的鉴定特征研究[D]. 北京: 北京中医药大学, 2006. |
| [28] | Rahman M A A, Moon S S. Antimicrobial phenolic derivatives from Dendranthema zawadskii var. Latilobum kitamura (Asteraceae)[J]. Arch Pharmacal Res, 2007, 30(11): 1374-1379. |
| [29] | 李国栋, 陈园园, 王 盼, 等. 野菊花中萜类和黄酮类化合物保肝作用研究[J]. 中草药, 2013, 44(24): 3510-3514. |
| [30] | 俞 浩, 肖 新, 刘汉珍, 等. 滁菊总黄酮对大鼠心肌缺血再灌注损伤的影响[J]. 食品科学, 2012, 33(15): 283-286. |
| [31] | 汝海龙, 蒋惠娣, 林国华, 等. 杭白菊总黄酮输血管作用[J]. 杭州师范学院学报, 2005, 4(6): 411-414. |
| [32] | 林忠宁, 林育纯, Sheng-Han ming, 等. 菊花倍半萜烯内酯诱导人鼻咽癌细胞毒性和凋亡的研究[J]. 中草药, 2002, 32(10): 909-912. |
| [33] | 马 力, 唐凤敏, 曾天舒, 等. 菊花多糖和绿原酸免疫调节作用的研究[J]. 医药导报, 2008, 27(10): 1168-1170. |
| [34] | 胡 春, 丁霄霖. 菊花提取物对人红细胞膜的保护作用研究[J]. 食品科学, 1996, 17(2): 7-12. |
| [35] | 胡 春, 丁霄霖. 菊花提取物对实验动物抗疲劳和降血脂作用的研究[J]. 食品科学, 1996, 17(10): 58-62 |
| [36] | 于善凯, 张 英, 吴晓琴, 等. 杭白菊的营养成分及其生物活性[J]. 中国食物与营养, 2002, 2: 50. |
| [37] | 崔 艳. 菊花提取物抑制小鼠高脂性脂肪肝形成及其机制研究[D]. 苏州: 苏州大学, 2014: 1-9. |
| [38] | 张培培. 滁菊总黄酮的镇痛抗炎作用及部分机制研究[D]. 合肥: 安徽医科大学, 2013, 1-15. |
| [39] | Nishina A, Kimura H, Tsukagoshi H, et al. Neurite outgrowth in PC12 cells stimulated by components from Dendranthema grandiflorum cv. "Mottenohoka" is enhanced by suppressing phosphorylation of p38MAPK[J]. Evid-Based Compl Alt, 2013, DOI: 10. 1155/2013/ 403503. |
| [40] | Wang Y J, Yang X W, Guo Q S, et al. Optimization of the extraction conditions and simultaneous quantification of six flavonoid glycosides in Flos Chrysanthemum by RP-LC[J]. Chromatographia, 2009, 70: 109-16 |
| [41] | 段崇霞, 张正竹. 四大药用菊花功能成分的比较研究[J]. 安徽农业大学学报, 2008, 35(1): 99-105. |
| [42] | 谭世强, 谢敬宇, 郭 帅, 等. 三萜类物质的生理活性研究概括[J]. 中国农学通报, 2012, 28(36): 23-27. |
 2015, Vol. 38
2015, Vol. 38



