2. 太原理工大学校医院, 山西 太原 030024
2. College Hospital, Taiyuan University of Technology, Taiyuan 030024, China
柴芩清热胶囊由柴胡、连翘、诃子、黄芩、大黄、甘草等组成,具有解肌透邪、清热泻火的功效,适用于感冒热证。证见恶寒、发热、头痛、身痛、咽痛或鼻塞、流涕等。经过多年临床应用证实,其具有较好的临床疗效。为有效控制其质量,确保该制剂的临床疗效,本试验对组方主要药味建立了定性鉴别方法,对方中君药黄芩的有效成分黄芩苷建立了高效液相色谱(HPLC)定量测定方法。试验结果显示,所建方法简便易行、灵敏准确、专属性强,可用于柴芩清热胶囊的质量控制。
1 仪器和试药 1.1 仪器Agilent高效液相色谱仪;Agilent N1100化学工作站;DAD二级阵列紫外检测器;依立特ODS-BP(250 mm×4.6 mm,5 μm)色谱柱;KQ3200DB型数控超声波清洗器(昆山市超声仪器有限公司);BP211D型电子天平(德国赛多利斯)。
1.2 试药芩连清热胶囊(自制样品,共3批,批号20130301、20130302、20130303);黄芩苷对照品(批号110715-200514,质量分数91.7%)、柴胡皂苷a对照品(批号110777-201309,质量分数92.0%)、柴胡皂苷d对照品(批号110778-200506,质量分数96.0%)、柴胡对照药材(批号120992-201108)、连翘苷对照品(批号110821-200340,质量分数95.3%)、连翘对照药材(批号120908-200512)、没食子酸对照品(批号110831-200302,质量分数89.9%)、诃子对照药材(批号121015-200503)、大黄对照药材(批号121249-201003)均购于中国食品药品检定研究院;甲醇为色谱纯;去离子水。
2 方法与结果 2.1 薄层色谱(TLC)鉴别 2.1.1 柴胡取本品内容物3 g,加5%浓氨甲醇溶液20 mL,超声处理20 min,滤过,滤液蒸干,残渣加水20 mL使溶解,用乙醚振摇洗涤2次,每次20 mL,合并乙醚液,弃去,水层用水饱和的正丁醇提取3次,每次15 mL,合并正丁醇液,用氨试液洗涤3次,每次15 mL,弃去氨液,分取正丁醇液,用正丁醇饱和的水洗涤3次,每次15 mL,弃去水洗液,正丁醇液回收溶剂至干,残渣加甲醇2 mL使溶解,过中性氧化铝柱(100~200目,3 g,内径为1.2 cm),用70%乙醇洗脱,收集洗脱液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取柴胡对照药材1 g,同法制成对照药材溶液;再取柴胡皂苷a对照品、柴胡皂苷d对照品,加甲醇制成0.5 mg/mL的混合溶液,作为对照品溶液。按处方制备缺柴胡的阴性样品,按供试品溶液制备方法制备阴性样品溶液。照薄层色谱法(《中国药典》2010版一部附录VI B)试验,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(13:7:2)配制、并在10℃放置后的下层溶液为展开剂,展开,取出,晾干,喷以2%对二甲氨基苯甲醛的40%硫酸溶液,60℃加热至显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,分别显相同颜色的斑点,结果见图 1。
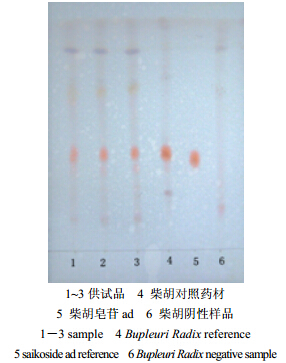 | 图 1 柴胡鉴别薄层色谱图Fig.1 TLC of Bupleuri Radix |
取本品内容物2 g,加水30 mL,加热回流20 min,趁热滤过,滤液用醋酸乙酯振摇提取3次,每次30 mL,合并醋酸乙酯液,蒸干,残渣加30%乙醇5 mL使溶解,加至已处理好的大孔树脂(D101,内径1.2 cm,高24 cm)上,用30%乙醇溶液30 mL洗脱,弃去洗脱液,再以50 mL 50%的乙醇溶液洗脱,收集洗脱液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液;另取连翘对照药材1 g,同法制成连翘对照药材溶液;再取连翘苷对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液;按处方制备缺连翘的阴性样品,按供试品溶液制备方法制备阴性样品溶液。照薄层色谱法(《中国药典》2010年版一部附录Ⅵ B)试验,吸取上述溶液各5 μL,以三氯甲烷-甲醇(5:1)为展开剂,展开,取出,晾干。喷以10%的硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点,结果见图 2。
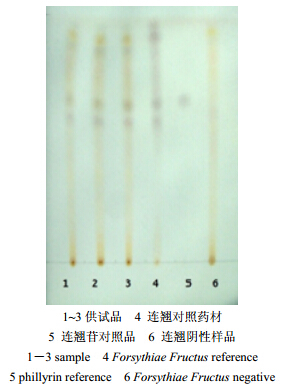 | 图 2 连翘鉴别的薄层色谱图Fig.2 TLC of Forsythiae Fructus |
取本品内容物0.5 g,加乙醇20 mL,超声处理15 min,滤过,滤液蒸干,残渣加水10 mL使溶解,用醋酸乙酯提取2次,每次10 mL,合并醋酸乙酯液,水浴蒸干,残渣加醋酸乙酯1 mL使溶解,作为供试品溶液。另取没食子酸对照品,加醋酸乙酯制成0.5 mg/mL的溶液,作为对照品溶液。按处方制备缺诃子的阴性样品,按供试品溶液制备方法制备阴性样品溶液。照薄层色谱法(《中国药典》2010年版一部附录VIB)试验,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-醋酸乙酯-甲酸(6:4:1)为展开剂,展开,取出,晾干,喷以1%三氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,结果见图 3。
 | 图 3 诃子鉴别薄层色谱图Fig.3 TLC of Chebulae Fructus |
取本品内容物3 g,加甲醇30 mL,超声处理30 min,滤过,滤液蒸干,残渣加水20 mL使溶解,再加盐酸2 mL,加热回流30 min,立即冷却,用乙醚振摇提取3次,每次10 mL,合并乙醚液,挥干,残渣加三氯甲烷1 mL使溶解,作为供试品溶液。另取大黄对照药材1 g,同法制成对照药材溶液。按处方制备缺大黄的阴性样品,按供试品溶液制备方法制备阴性样品溶液。照薄层色谱法(《中国药典》2010版一部附录VI B)试验,吸取供试品溶液及阴性样品溶液10 μL、对照药材溶液4 μL,分别点于同一硅胶G薄层板上,以石油醚(30~60℃)-甲酸乙酯-甲酸(15:5:1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同的橙黄色荧光斑点,见图 4。
 | 图 4 大黄鉴别薄层色谱图Fig.4 TLC of Rhei Radix et Rhizoma |
色谱柱为十八烷基硅烷键合硅胶柱(250 mm×4.6 mm),柱温25℃,流动相为甲醇-0.2%磷酸(49∶51),检测波长为280 nm,理论板数按黄芩苷峰计算应不低于2500。
2.2.2 对照品溶液的制备取黄芩苷对照品适量,精密称定,加甲醇制成40 μg/mL的溶液,即得。
2.2.3 供试品溶液的制备参照《中国药典》2010年版一部含黄芩的中药复方制剂项下含量测定方法试验。柴芩清热胶囊供试品提取方法选择超声处理,制得的供试品溶液25 mL,超声处理30 min,并对提取所用溶剂、超声时间进行考察。结果,确定提取溶剂为70%乙醇、超声时间为30 min。
2.2.4 专属性试验按处方工艺制备缺黄芩药材的阴性样品,按2.2.3项下供试品方法制备,即得阴性供试品溶液。吸取对照品溶液、供试品溶液及阴性溶液,进样,测定。结果阴性样品不干扰黄芩苷的测定。见图 5。
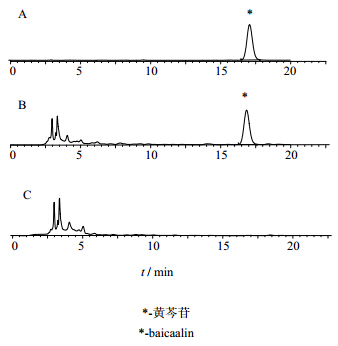 | 图 5 黄芩苷对照品(A)、供试品(B)及阴性样品(C)色谱图Fig.5 Chromatogram of baicaalin (A), sample (B),and negative sample (C) |
精密称取黄芩苷对照品,加甲醇制成47.6 μg/mL的溶液。分别精密吸取1、2、5、10、15 μL进样,依法测定,以黄芩苷质量为横坐标,峰面积积分值为纵坐标,计算得回归方程:Y=2 669.9X−2.980 6,r=1。表明黄芩苷在0.0436~0.654 μg与峰面积具有良好的线性关系。
2.2.6 精密度试验精密量取黄芩苷对照品溶液(43.6 μg/mL),按上述色谱条件连续进样6次,每次进样10 μL测定,计算黄芩苷峰面积积分值的RSD值为1.09%,表明仪器的精密度良好。
2.2.7 稳定性试验取同一批(批号20130303)中试样品,按供试品溶液的制备方法制备;每隔一定时间测定一次,进样6次;计算黄芩苷峰面积积分值的RSD值为2.15%,表明供试品在10 h内稳定性良好。
2.2.8 重复性试验取同一批(批号20130303)样品,研细,混匀;取约0.2g,精密称定,按供试品溶液制备方法制备,平行制备6份进行含量测定,每份测2次,取平均值。经计算供试品中黄芩苷平均含量为30.44 mg/g,RSD为1.38 %,重复性良好。
2.2.9 加样回收试验分别取已知含量的柴芩清热胶囊样品6份约0.1 g,精密称定,分别精密添加一定量的对照品,按供试品溶液制备方法制备,测定供试品中黄芩苷峰面积并计算加样回收率。结果表明,供试品中黄芩苷平均加样回收率为98.39%,RSD值为0.81%。
2.2.10 样品测定按供试品溶液的制备方法操作,对柴芩清热胶囊3批样品中黄芩苷进行含量测定,精密吸取供试品溶液10 μL,注入液相色谱仪,计算样品中黄芩苷的质量分数,结果见表 1。
| 表 1 批样品中黄芩苷的含量测定结果 Table 1 Determination of baicalin in three batches of samples |
复方中柴胡的薄层鉴别一直是个难点。柴胡主要含有皂苷和挥发油,此外还有黄酮类、多糖类、豆甾醇、木脂素、香豆素、色氨酸等[1]。曾参照《中国药典》2010年版一部中柴胡药材的鉴别方法[2]。结果在供试品色谱中,在对照药材相应的位置上斑点不清晰,而且底色较重。鉴别效果不理想。通过不断分析原因,多次试验,同时参考文献方法[3, 4, 5]。主要是本处方中药味较多,杂质影响鉴别。柴胡皂苷易溶于水、稀醇,特别是热水和热醇,在丁醇和戊醇中溶解度最大,难溶或不溶于苯,氯仿等试剂。所以根据柴胡皂苷的性质进行了多步纯化。最后经过反复试验研究,采用三氯甲烷-甲醇-水(13:7:2)配制,并在10℃以下放置分层的下层溶液为展开剂,用2%对二甲氨基苯甲醛的40%硫酸溶液为显色剂,采用柴胡对照药材作对照,供试品样品中柴胡皂苷类成分斑点清晰,特征性强,阴性无干扰,该方法成熟,重复性好。
| [1] | 杨 柳, 王雪莹, 刘 畅, 等. 北柴胡化学成分与药理作用的研究进展[J]. 中医药信息, 2012, 29(3): 143-145. |
| [2] | 中国药典[S]. 一部. 2010. |
| [3] | 薛吉利, 丁 红, 杜 艳, 等.小柴胡片中柴胡和党参的薄层鉴别[J].中国药物与临床, 2012, 12(11): 1445- 1446. |
| [4] | 刘琳娜, 戚志华, 郭志伟, 等.小柴胡汤滴丸质量标准研究[J]. 实用药物与临床, 2012, 15(11): 742-744. |
| [5] | 张明子, 玄龙洙, 刘 汇.复方熊胆乙肝胶囊中柴胡鉴别的探讨[J]. 药物鉴定, 2011, 20(20): 33-34. |
 2014, Vol. 37
2014, Vol. 37

