辅酶是生物体内广泛存在的脂溶性醌类化合物,在人体呼吸链中质子移位及电子传递中起重要作用,可作为细胞代谢和细胞呼吸激活剂,并是重要的抗氧化剂和非特异性免疫增强剂,具有抗心肌缺血、抗心衰、抗心律失常、提高人体免疫力、增强抗氧化、延缓衰老和增强人体活力等功能。在欧美国家,辅酶Q10广泛应用在非处方药和保健食品中。在《美国药典》(USP)中辅酶Q10被收录为膳食补充剂类产品。辅酶Q10作为常规品种,分别被《欧洲药典》(EP)、《日本药典》(JP)、《英国药典》(BP)、《中国药典》2010年版(ChP2010)等多国药典收录。除《日本药典》外,《美国药典》、《欧洲药典》、《英国药典》、《中国药典》2010年版都收载了辅酶Q10异构体检测项目。《美国药典》检测项目为有关物质项下测试2,癸稀醌(2Z)-异构体和相关杂质;《欧洲药典》和《英国药典》测试项目为有关物质项下,杂质F测试;《中国药典》2010年版测试项目为检查项下,异构体测试。各药典的关于异构体测试的色谱条件见表 1;样品处理方法各药典要求基本一致,即样品加正己烷溶解配置成约1.0 mg/mL的溶液,要求避光操作。各国药典均未提及样品溶液临用新配;关于辅酶Q10异构体检测过程溶液降解有关的文献报道也较少,本文通过一系列试验证实了异构体检测溶液在存放过程会发生降解,从而导致检测结果的偏差。
| 表 1 各药典关于异构体测试的色谱条件 Table 1 CoQ10 isomer test conditions from different pharmacopoeia |
辅酶Q10(杭州华东医药集团康润制药有限公司,生产批号COQ-140367、COQ-140369;神舟生物科技有限公司,生产批号SZFQ140201、SZFQ140202;新昌制药有限公司,生产批号0908105);正己烷(色谱纯,默克公司);醋酸乙酯(色谱纯,默克公司);
Agilent 1200高效液相色谱仪(四元泵,紫外检测器,自动进样器,柱温箱);Agilent 1260高效液相色谱仪(四元泵,紫外检测器,自动进样器,柱温箱);100 mL棕色量瓶,100 mL透明量瓶。 1.2 方法 1.2.1 供试品溶液的制备
精密称定辅酶Q10产品每批各100 mg分别置于棕色量瓶和透明量瓶中,加正己烷约50 mL震摇溶解,全溶后加正己烷定容至刻度。
用注射器分别抽取各批号新配好的棕色瓶和透明瓶溶液各1.5 mL左右注入棕色进样小瓶中,记录为0 h供试品溶液。
将剩余的供试品溶液配制好的样品置于室温条件,日光灯下放置3 h,用注射器分别抽取各批号新配好的棕色瓶和透明瓶溶液各1.5 mL左右注入棕色进样小瓶中,记录为3 h供试品溶液。
剩余供试品溶液继续放置至5 h,用注射器分别抽取各批号新配好的棕色瓶和透明瓶溶液各1.5 mL左右注入棕色进样小瓶中,记录为5 h供试品溶液。
1.2.2 色谱条件参照《中国药典》2010年版辅酶Q10产品项下异构体检测条件要求,色谱柱为汉邦LichrospherTM Si硅胶柱(4.6 mm×250 mm,5 μm),流动相为正己烷-醋酸乙酯(97:3),体积流量2.0 mL/min,检测波长275 nm,进样量为20 μL,记录色谱图至主成分峰保留时间的约4倍(40 min)。辅酶Q10异构体检测的HPLC色谱图见图 1。
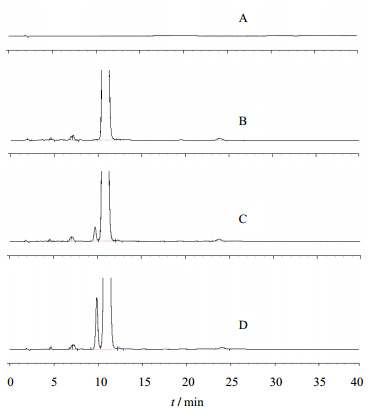 | 图 1 空白溶剂和供试品溶液(0、3、5 h)色谱图Fig. 1 Chromatogram of blank and test solution(0, 3, 5 h) |
根据表 2统计结果,3种不同来源的辅酶Q10产品相对保留时间(RRT)小于1.0的几个杂质均存在,其主要差异在于RRT大于1.0处的几个杂质。根据《中国药典》2010年版有关内容描述,辅酶Q10保留时间约为10 min,异构体峰相对保留时间约为0.9,3种不同来源的辅酶Q10产品中均存在RRT=0.90杂质,即3种不同来源的辅酶Q10产品中均存在辅酶Q10异构体。
| 表 2 不同来源辅酶Q10产品异构体杂质 Table 2 Isomer impurities in CoQ10 products from different sources |
不同存放条件,不同存放时间辅酶Q10正己烷溶液典型的HPLC图谱见图 1。
2.3 辅酶Q10正己烷溶液中异构体变化情况不同来源的几批产品配制的异构体检测溶液分别存放于棕色量瓶和透明量瓶,0、3、5 h异构体峰面积归一化百分比变化情况见表 3。
| 表 3 辅酶Q10的正己烷溶液不同时间和条件的HPLC峰面积归一化结果 Table 3 HPLC area percentage of CoQ10 in n-hexane from different time and conditionse |
不同来源的几批产品配制的异构体检测溶液分别存放于棕色容量瓶和透明容量瓶,0、3、5 h主峰变化情况见图 2。
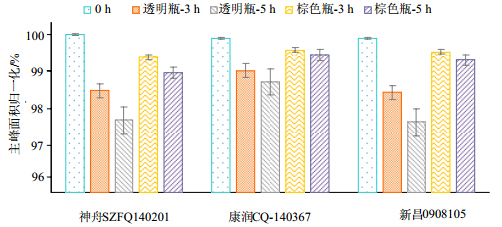 | 图 2 不同来源辅酶Q10主峰面积归一化百分比变化情况Fig. 2 Changes of HPLC main peak area percentage of CoQ10 from different sources |
按上述1.2供试品制备方法分别用棕色量瓶和透明量瓶取制备1批(CQ-140367)供试品溶液,并装在黑色塑料袋中,置于室温条件下密闭的瓦楞纸箱中,分别在0、5 h和放置过夜时间点取样,按照1.2.2色谱条件HPLC检测。不同时间点HPLC图谱显示主峰面积归一化百分比和异构体峰面积归一化百分比未发生明显变化。
3 分析与讨论综合上表 3和图 2统计结果,RRT=0.90杂质峰面积归一化百分比变化明显,除RRT=0.90杂质峰和主峰面积归一化百分比变化较大外,其他杂质
峰面积归一化百分比几乎未发生变化。在正己烷溶液中辅酶Q10主要降解产物是辅酶Q10异构体。辅酶Q10的正己烷溶液在棕色量瓶中转换为异构体的速度远低于在透明量瓶中的转换速度。辅酶Q10在正己烷溶液中转换为异构体的过程中,棕色量瓶和透明量瓶的透光效果不同,光线能加速了辅酶Q10转换为异构体,因此,《中国药典》中明确指出了异构体检测过程要避光操作。另外,无论是棕色量瓶还是透明量瓶中不避光长时间的放置都会造成异构体峰面积和归一化百分比的增加,从而影响检测结果的准确性。
辅酶Q10异构体检测过程中,样品的配置应在避光环境中进行,应使用棕色容量瓶配制溶液,配制好的溶液应尽快进样分析,样品溶液的制备应坚持临用新配原则,应避免长时间的放置造成辅酶Q10降解为异构体,从而影响了检测结果的准确性。
| [1] | 中国药典2010 年版[S].二部.2010: 882-883. |
| [2] | 美国药典32 版[S].USP32-NF27: 1079-1080. |
| [3] | 欧洲药典6.0 版[S].EP 6.0: P3163-3164. |
| [4] | 张劲松, 王 丹, 黄琴伟, 等.国产辅酶Q10 有关物质的评价研究[J].西北药学杂志2009, 24(6): 440-442. |
| [5] | 王 艳.保健食品中辅酶Q10 含量的测定[J].公共卫生与防御医学, 2012, 23(4): 103-104. |
| [6] | 张 楠, 曹玉成.辅酶Q10 制备方法研究进展[J].榆林学院学报, 2006, 16(6): 12-14. |
| [7] | 王 辛, 乔海鸥, 穆敏杰.保健食品中辅酶Q10 含量的测定及其提取条件的研究[J].中国卫生检验杂志, 2008, 18(7): 1321-1323. |
| [8] | Fir M M, Smidovnik A, Milivojevic L, et al.Studies ofCoQ10 and cyclodextrin complexes: solubility, thermo-and photo-stability[J].J Incl Phenom MacrocyclChem, 2009, 64(3/4): 225-232. |
 2014, Vol. 37
2014, Vol. 37

