2. 天津泛博生物科技有限公司, 天津 300384
2. Tianjin Fineample Biotechnology Company Co., Ltd., Tianjin 300384, China
慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)是因形态成熟的淋巴细胞不能够正常凋亡,反而在淋巴组织中克隆性增殖而引发的一种慢性血液系统恶性肿瘤[1]。CLL有一定的家族遗传性,属于B细胞非霍奇金淋巴瘤(non-Hodgkin’s lymphoma,NHL)中较常见的一种。套细胞淋巴瘤(mantle cell lymphoma,MCL)是一种罕见的B细胞NHL,约占全部NHL的5%~10%,兼具恶性淋巴瘤的难治愈性及侵袭性[2]。MCL不易诊断,约85%的患者确诊时已处于Ⅲ~Ⅳ期;且易复发,是远期生存率最低的亚型淋巴瘤。临床上常表现为高热乏力、脾脏和淋巴结肿大、胃肠道累及和对神经系统的浸润[3]。
目前CLL的一线治疗方案是FCR方案,即氟达拉滨(F)、环磷酰胺(C)和利妥昔单抗(R)三者联合治疗的方案,该方案有一定疗效,但无疾病进展生存率为38%,3或4级不良反应时有发生[4]。MCL常选用蒽环类或含大剂量阿糖胞苷的药物,然
而对常规化疗药大多不敏感,虽然已有较多药物用于治疗,但患者的总生存期并没有明显延长[5];尽管也采用药物与单抗联合化疗的方案治疗MCL,但毒性较大,感染发生率约为14%,3~4级不良反应发生率高达87%[6]。因此,可行的治疗方案和高效安全的药物有待推出。由Pharmacyclics公司和杨森制药(Jassen)共同研制的依鲁替尼(Ibrutinib,商品名Imbruvica)作为口服的布鲁顿酪氨酸激酶(BTK)抑制剂类首创新药,于2013年2月被FDA授予突破性治疗药物资格,并分别于2013年11月13日和2014年2月12日批准为MCL和CLL的治疗药物[7,8]。 1 药物基本信息[8,9]
通用名:Ibrutinib
别名:CRA-032765、PCI-32765
化学名:1-[(3R)-3-[4-氨基-3-(4-苯氧基苯基)-1H-吡唑并[3,4-d]嘧啶-1-基]-1-哌啶基]-2-丙烯-1-酮
CAS号:936563-96-1
分子式:C25H24N6O2
相对分子质量:440.50,结构见图 1。
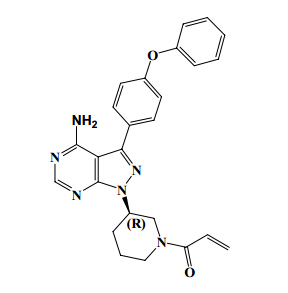 | 图 1 依鲁替尼结构Fig. 1 Structure of Ibrutinib |
本品为白色或类白色固体,易溶于二甲基亚砜,可溶于甲醇,不溶于水;分配系数(lgP)为3.97(pH=7);解离常数(pKa)为74;熔点为149~158 ℃。
制剂处方包括依鲁替尼、甲基纤维素钠、硬脂酸镁、微晶纤维素、十二烷基硫酸钠。
适应症:慢性淋巴细胞白血病、套细胞淋巴瘤。
剂型:胶囊
规格:140 mg/粒
用法用量:口服,1 次/d,3 粒/次治疗慢性淋巴细胞白血病;口服,1 次/d,4 粒/次治疗套细胞淋巴瘤。 2 合成方法
美国Pharmacyclics公司的专利技术[10],以1H-吡唑并[3,4-d]嘧啶-4-胺(1)为起始原料,DMF为溶剂,在加热条件下,与N-碘代琥珀酰亚胺反应制备得到3-碘-1H-吡唑并[3,4-d]嘧啶-4-胺(2);K2CO3和二烷为反应溶剂,在微波和180 ℃条件下,化合物2与适当取代的苯基硼酸进行钯介导的交叉偶联反应,形成中间体1;在偶氮二甲酸二异丙酯和树脂结合的pph3条件下,中间体1通过Mitsunobu反应与N-Boc-3-羟基哌啶偶合,得到Boc(叔丁氧羰基)保护的中间体2;中间体2用盐酸去保护后,再与丙烯酰氯偶合,得到目标化合物,合成路线见图 2。 3 作用机制
B细胞抗原受体(BCR)的信号通路是众多肿瘤生长和播散的关键驱动者[2]。BTK作为BCR信号肽不可或缺的参与者,对B淋巴细胞的形成、分化、信息传递和生存至关重要。BTK是BCR通道
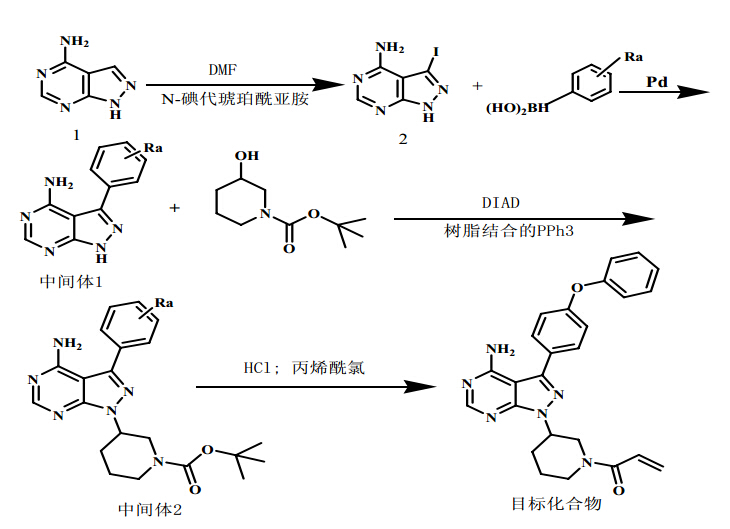 | 图 2 依鲁替尼的合成Fig. 2 Synthesis of Ibrutinib |
可识别的信号肽分子,当该信号肽分子穿过B淋巴细胞表面受体时,B淋巴细胞实现转运、趋化性和黏附作用的必需通道被激活,这为B细胞恶性肿瘤的形成提供了便利[8]。
依鲁替尼是一种小分子的BTK抑制剂,可与BTK活性位点上的半胱氨酸残基(Cys-481)选择性地共价结合,不可逆地抑制BTK的活性,进而抑制BCR信号通路的激活,有效阻止肿瘤从B细胞迁移至适宜肿瘤生长的淋巴组织,减少B细胞恶性增殖并诱导细胞的凋亡,从而发挥治疗CLL和MCL的作用[11]。非临床研究表明依鲁替尼能够抑制恶性B淋巴细胞在体内的增殖和存活[12]。 4 药效学
Ponader 等[13]的一项试验中,给4对淋巴瘤模型犬每日口服依鲁替尼胶囊2.5~20 mg/kg,共7 d,然后镜检被标记的单核细胞,结果发现依鲁替尼能够与外周血液及肿瘤组织中的BTK结合,肿瘤斑块都有不同程度的减少。
Ⅰ期临床试验结果表明,对于容易复发且不易治愈的NHL患者,依鲁替尼可与BTK形成不可逆结合,在服药后的4 h内不可逆结合率高达95%以上,该结合对周围血细胞无显著影响[14]。一项对48位CLL患者每日po依鲁替尼420 mg,治疗时间为15.6个月的试验结果显示总体应答率为58.3%,应答响应时间从5.6~24.2个月[8]。在Ⅱ期临床试验中,111名MCL患者每日po依鲁替尼560 mg,治疗时间为8.3个月,结果显示总体应答率高达68%,完全应答率达到21%,另有47%的患者为部分应答,应答响应时间的中值为17.5个月[15]。 5 药动学 5.1 吸收
依鲁替尼口服后吸收迅速,1~2 h可达最大血药浓度,其暴露量将增加至840 mg[8]。在稳定状态下,从服药560 mg/d的患者体内检测到药-时曲线下面积(AUC)为(953±750)ng∙h/mL;从服药420 mg的患者体内检测到AUC为(680±517)ng∙h/mL。与禁食1夜后用药相比,非空腹服用依鲁替尼会使其暴露量增加近2倍。 5.2 分布
在体外试验中,依鲁替尼与人体血浆蛋白的可逆性结合率为97.3%,在50~1 000 ng/mL没有剂量相关[16]。在稳定状态下,依鲁替尼的表观分布容积(Vd,ss/F)约为10 000 L。 5.3 代谢
依鲁替尼主要通过细胞色素P450(CYP3A和少部分的CYP2D6)代谢,代谢后产生多种代谢产物。其中,有效代谢产物PCI-45227是一种对BTK具有抑制活性的二氢二醇物质。与依鲁替尼相比,这种代谢物对BTK的抑制作用更强,约是依鲁替尼的15倍。在稳定状态下,PCI-45227的平均代谢率为1~2.8。 5.4 消除
依鲁替尼的表观清除率(CL/F)约为1 000 L/h,半衰期(t1/2)为4~6 h[8]。依鲁替尼在体内主要以代谢产物的形式存在,随粪便排出体外。通过给健康受试者口服放射性14C标记的依鲁替尼,发现近90%的放射物在168 h内消除,其中大多(约80%)随粪便排出,近10%随尿液排出,约1%以原形随粪便排出。
依鲁替尼的消除不会随年龄(37~84岁)和性别而产生变化,但在中度肝损伤患者体内其系统性暴露量较健康受试者高6倍。 6 药物相互作用
依鲁替尼主要通过CYP3A代谢,因而在与CYP3A抑制剂或诱导剂同时服用时,其暴露量将会受到影响。酮康唑是CYP3A强抑制剂,能使依鲁替尼的最大血药浓度(Cmax)和AUC分别增加29、24倍;中度CYP3A抑制剂能使依鲁替尼的Cmax和AUC分别增加6、9倍[8]。
利福平是强CYP3A诱导剂,能使依鲁替尼的暴露量降低为原来的1/10;中度CYP3A诱导剂也能使依鲁替尼的暴露量降低为原来的1/3[9]。这种暴露量的改变并不是希望的结果。因此,应避免依鲁替尼与中度或强CYP3A抑制剂及诱导剂同时服用,这种强抑制剂还包括伊曲康唑、伏立康唑、泊沙康唑、克拉霉素和泰利霉素,强诱导剂还包括卡马西平、利福平和苯妥英等。 7 不良反应
在Ⅱ期临床研究中,51名CLL患者每日口服依鲁替尼420 mg,治疗时间为21个月,出现的不良反应大多数属于1或2级,约20%的患者出现了腹泻、上呼吸道感染、乏力、咳嗽、关节痛、药疹、发热或轻微水肿等,出现3或3级以上血液病不良反应较少,包括血小板减少(10%),嗜中性白细胞减少(15%)[17];111名MCL患者每日口服依鲁替尼560 mg,治疗时间为8.3个月,出现的不良反应也大多属于1或2级,近20%的患者出现了腹泻、乏力、恶心、轻微水肿、呼吸障碍、便秘、呕吐或食欲减退等,出现3或3级以上血液病不良反应同样较少,包括嗜中性粒细胞减少(16%),血小板减少(11%)和贫血(10%)[8]。 8 结语
分子靶向抗肿瘤药物以选择性高、毒性低、活性强的特点引领目前肿瘤治疗的发展方向。依鲁替尼是口服的BTK抑制剂类首创新药,是作用于BTK的新型分子靶向抗肿瘤药物,对B细胞淋巴瘤作用明显,现已批准作为MCL和CLL的治疗药物。但是,依鲁替尼潜在的药物相互作用尚未得到充分的认识,因此需要更进一步的研究。
另有研究表明,依鲁替尼对其他B细胞淋巴瘤(包括小淋巴细胞淋巴瘤、滤泡性淋巴瘤和弥漫大B细胞淋巴瘤)也有一定的作用[17,18,19]。因此,进行相关的药效、临床与药动学研究后,依鲁替尼具有良好的开发前景。搞清楚与其他药物的相互作用、增加新的适应症也将是未来研究的重点。
| [1] | 李 菲, 易树华, 于 珍, 等. 利妥昔单抗联合氟达拉滨和环磷酸酰胺治疗慢性淋巴细胞白血病的疗效和安全性 [J]. 中华血液学杂志, 2013, 34(5): 384. |
| [2] | Novero A, Ravella P M, Dous G, et al. Ibrutinib for B cell malignancies [J]. Exp Hematol Oncol, 2014, 3(1): 4. |
| [3] | 刘雪花, 龚玉萍. 套细胞淋巴瘤的研究进展 [J]. 中华临床医师杂志, 2013, 7(20): 9300-9303. |
| [4] | 夏 奕, 徐 卫, 李建勇. 第54届美国血液学年会研究热点报道——慢性淋巴细胞白血病 [J]. 中华血液杂志, 2013, 34(2): 182-183. |
| [5] | Chandran R, Gardiner S K, Simon M, et al. Survival trends in mantle cell lymphoma in the United States over 16 years 1992-2007 [J]. Leuk Lymphoma, 2012, 53(8): 1488-1493. |
| [6] | 朱 军, 应志涛. 套细胞淋巴瘤诊治新进展 [J]. 中国肿瘤临床杂志, 2011, 38(18): 1067-1069. |
| [7] | 张 翼. FDA批准套细胞淋巴癌治疗新药依鲁替尼 [J]. 药品评价杂志, 2013, 10(22): 27-28. |
| [8] | FDA. Full prescribing information [EB/OL].(2014-02-13)[2014-03-21]. http://www.accessdata.fda. |
| [9] | FDA. Clinical pharmacology and biopharmaceutics review(s) [EB/OL]. (2013-11-25)[2014-01-12]. http:// www.acce-ssdata.fda.gov/drugsatfda_docs/nda/2013/205552Orig1s000ClinPharmR.pdf. |
| [10] | Pharmacyclics Inc., Sunnyvale, CA(US). Inhibitors of Bruton’s tyrosine kinase [P]. US: 007514444B2, 2009-04-07. |
| [11] | Burger J A, Hacken E. Molecular pathways: targeting the microenvironment in chronic lymphocytic leukemia-focus on the B cell receptor [J]. Clin Cancer Res, 2014, 20(3): 548-556. |
| [12] | Honigberg L A, Smith A M, Sirisawad M, et al. The Bruton tyrosine kinase inhibitor PCI-32765 blocks B-cell activation and is efficacious in models of autoimmune disease and B-cell malignancy [J]. Proc Nat Acad Sci USA, 2010, 107(29): 13075-13080. |
| [13] | Ponader S, Chen S S, Buggy J J, et al. Bruton’s tyrosine kinase inhibitor PCI-32765 thwarts chronic lymphocytic leukemia cell survival and tissue homing in vitro and in vivo [J]. Blood, 2012, 119(5): 1182-1189. |
| [14] | Advani R H, Buggy J J, Sharman J P, et al. Bruton tyrosine kinase inhibitor Ibrutinib (PCI-32765) has significant activity in patients with relapsed/refractory B-cell malignancies [J]. Clin Oncol, 2013, 31(1): 88-94. |
| [15] | Wang M L, Rule S, Martin P, et al. Targeting BTK with Ibrutinib in relapsed or refractory mantle-cell lymphoma [J]. N Eng1 J Med, 2013, 369(6): 507-516. |
| [16] | Byrd J C, Furman R R, Coutre S E, et al. Targeting BTK with ibrutinib in relapsed chronic lymphocytic leukemia [J]. New Eng J Med, 2013, 369(1): 32-42. |
| [17] | Cameron F, Sanford M. Ibrutinib: first global approval [J]. Drugs, 2014, 74(2): 263-271. |
| [18] | O’Brien S, Furman R R, Coutre S E, et al. Ibrutinib as initial therapy for elderly patients with chronic lymphocytic leukaemia or small lymphocytic lymphoma: an open-label, multicentre, phase 1b/2 trial [J]. Lancet Oncol, 2014, 15(1): 48-58. |
| [19] | Mathews Griner L A, Guha R, Shinn P, et al. High-throughput combinatorial screening identifies drugs that cooperate with ibrutinib to kill activated B-cell-like diffuse large B-cell lymphoma cells [J]. Proc Nat Acad Sci USA, 2014, 111(6): 2349-2354. |
 2014, Vol. 37
2014, Vol. 37


