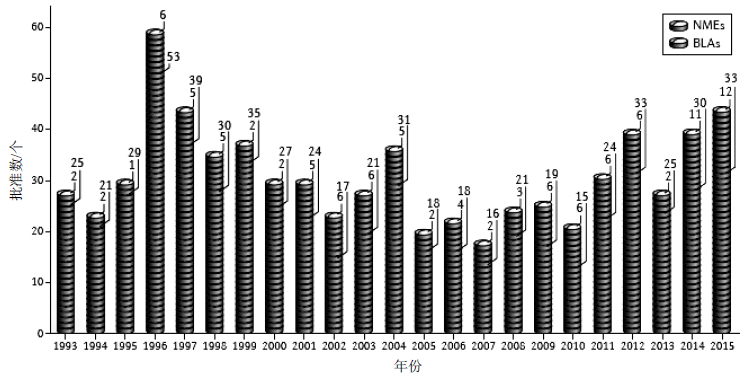
无论对产业界还是美国食品药品监督管理局 (FDA)自身来说,2015 年都是标志性的年份,其 药品评价和研究中心(CDER)共批准了45 个小分 子及抗体类新药,这是过去19 年中批准数最多的年 份,超过了先前创纪录的2014 年的41 个,见图 1。 这个数字也是2005—2009 年平均批准数的1 倍。 FDA 的生物药品评价和研究中心(CBER)还批准 了疫苗等13 个生物制品。
|
图 1 1993 年以来CDER 历年批准的新药 Fig.1 NMEs and BLAs approved by CDER since 1993 |
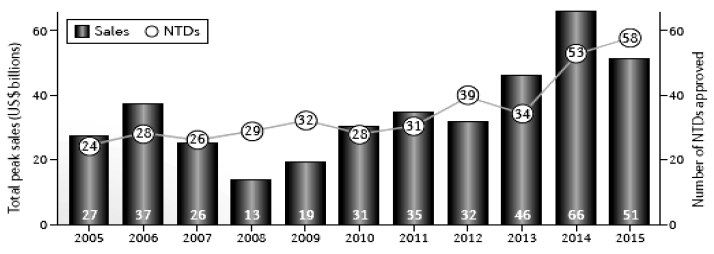
据波士顿咨询公司(BCG)的年度分析报告披露, 这些药品均有非常可观的潜在商业价值。如图 2 所示, 这些新批准品种的平均年销售峰值预计可达9 亿美 元。虽然低于2014 年的年均销售峰值的14 亿美元, 但比2009 年批准品种的平均销售峰值高50%。2014 年的高平均销售峰值主要是由于吉列德科学公司创 销售纪录的丙肝复方新药ledipasvir/sofosbuvir,以及2 个肿瘤免疫疗法的新药。
|
图 2 2005 年以来历年批准新品的合计销售峰值 Fig.2 Aggregated peak drug sales since 2005 |
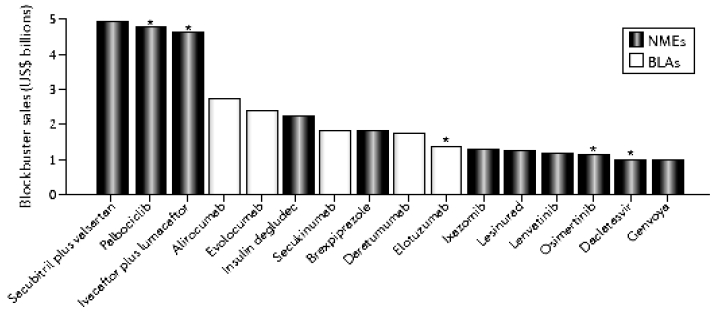
BCG 的高级合伙人Michael Ringel 认为,无论 从批准数量,还是预计的销售峰值,2015 年都是制 药界的丰收年,新药数量及商业价值已经从2009 年下行轨道急速进入上升轨道了。CDER 新批准的 品种中约有16 个(36%)可能达到重磅炸弹级,见 图 3。
|
图 3 2015 年批准可能的重磅炸弹品种及销售峰值 Fig.3 Anticipated blockbusters approved in 2015 and estimated sales for 2020 |
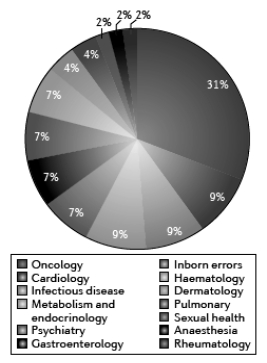
从治疗领域来看,抗肿瘤药物仍然占多数,见 图 4,2015 年FDA 共批准了14 个抗肿瘤药物,占 总数的31%。过去4 年中有3 年抗肿瘤药物的占比 都超过30%,只有2014 年占比为20%。多样性骨 髓瘤又是其中的热点,2015 年共有4 个新药,包括 首次2 个单抗类药物被批准用于本适应症。另外, Amgen 公司的talimogene laherparepvec,作为第1 个溶瘤病毒制剂也将很快获批。
|
图 4 2015 年新批品种的领域分布 Fig.4 Approvals by therapeutic area |
据BCG 的年度分析报告,2015 年批准的抗肿 瘤药物的商业价值可能小于前几年批准的抗肿瘤药 物。其中最有商业价值的是辉瑞首创的CDK4/ CDK6 抑制剂palbociclib,预计年销售峰值可达到 48 亿美元。2015 年CDER 新批的品种见表 1,部分 即将获批的品种见表 2。
| 表 1 2015 年CDER 新批的品种 Table 1 New CDER approvals for 2015 |
| 表 2 部分即将获批的品种 Table 2 Selected new drugs to watch |
另外3 个畅销药物来自全科医生的意见,这是 很不寻常的,因为这些领域已经很久没有新药了。1 个是诺华的治疗慢性心衰的药物entrsto(LCZ-696), 预计全球年销售峰值可达50 亿美元,还可能成为以 效果来定价的1 个案例。另外两个是通过快速审批 的PCSK9 抑制剂,用于降低低密度脂蛋白,分别 是赛诺非的alirocumab 和Amgen 的evolocumab。
以治疗罕见病开发的孤儿药的批准数量在2015 年达到最高峰,共有21 个获批,占比达47%,远超 2014 年的17 个(41%)和2013 年的9 个(33%)。 2014 年批准的孤儿药中超过一半是抗肿瘤药,这也反 映出肿瘤适应症的分类越来越细。重大突破性药物的 审批政策执行以来,这类药物的批准数量基本稳定, 2015 年共批准10 个,占比22%,2014 年是9 个,占 比也是22%。这些药物中有5 个(50%)预计可达到 重磅炸弹级,而2014 年的比例则为66%(6 个)。
相比于高批准率,2015 年的拒批率是很低的。
CDER 只签发了2 封完成拒绝批准的回复信,而 2009 年是22 封。这可不是FDA 降低了新药批准的标 准,而是归功于他们与申报者建立了更密切的交流, 更好地平衡风险/效益比,提高申报的成功率。
2016 年仍将是新药批准的丰产年。FDA在2015 年共收到40 个新药申请(包括NME 和BLA),2014 年是41 个。这些申请的大多数都将在2016 年评审 并获批。本年度的新药中包括治疗唐氏肌无力的首 个外显子跳读的寡核苷酸药物,首个B 细胞淋巴瘤-2 抑制剂,首个抗PDL-1 单抗药物等全新机制的新药。
欧盟(EMA)在2015 年共批准各类药品39 个, 包括小分子药物、血液制品、抗体及疫苗。EMA 批 准的品种大部分与FDA 的品种重叠,治疗领域上也 与FDA 相似,抗肿瘤药和孤儿药占多数。EMA 批准 的品种中有3 个还没有获得FDA的批准,分别是UCB 公司治疗癫痫的布瓦西坦,Grupo Ferrer 公司治疗嗜 睡症的替罗利特,以及Birken 公司治疗伤口愈合的富 含白桦木质醇的桦树皮提取物。
 2016, Vol. 31
2016, Vol. 31

