2. 天津药物研究院, 天津 300193
2. Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China
通用名:finerenone
别名:BAY-94-8862
化学名:4-(4-氰基-2-甲氧苯基)-5-乙氧基-2,8-二甲基-1,4-二氢-1,6-萘啶-3-甲酰胺
英文名:4-(4-cyano-2-methoxyphenyl)-5-ethoxy- 2,8-dimethyl-1,4-dihydro-1,6-naphthyridine-3-formamide
CAS:1050477-31-0
分子式:C21H22N4O3
相对分子质量:378.6
研究和开发公司:德国拜耳公司
结构见图 1
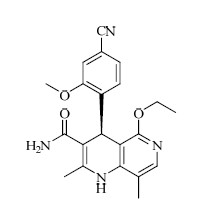 | 图 1 finerenone 的结构式 Fig.1 Structure of finerenone |
药理分类:非甾体类盐皮质激素受体拮抗剂
适应症:慢性心脏衰竭、慢性肾脏病
目前阶段:Ⅲ期临床
2 相关背景finerenone是新一代口服非甾体类盐皮质激素受体拮抗剂,由德国制药巨头拜耳公司开发,并研究其治疗慢性心脏衰竭和糖尿病性肾病的疗效和安全性[1]。finerenone能够阻断醛甾酮导致的盐皮质激素受体过度激活产生的有害影响,盐皮质激素受体的过度激活可在心脏和肾脏中导致病理性改变,这可通过有效的阻断加以预防。当前应用甾体类药物已被证明能够有效降低伴有低射血分数的心脏衰竭患者的心血管死亡率,但严重的副作用(如高钾血症、肾功能不全、抗雄激素/孕激素)限制了这类药物的使用。近年来,慢性心脏衰竭仍是一种致命性疾病,5年生存率与晚期癌症类似。该研究的领导者Bärfacker博士指出[2]:对于目前糖尿病或其他原因引起的慢性肾脏病患者,finerenone是一个比螺内酯受体选择性更大、受体亲和力比依普利酮更好的药物,可用于严重肾功能损害的患者。
3 合成路线finerenone的合成方法主要有两条路线:第1条路线[3]是将2-甲氧基-4-氰基苯甲醛和乙酰乙酸乙酯溶于二氯甲烷,回流24 h缩合得到化合物1。化合物1中加入3-甲基-4-氨基-2-氧代吡啶,在异丙醇中回流36 h环合得到化合物2。化合物2在烷基三氟甲基磺酸酯、硼氢化钠、DMF、溴乙烷存在下,130 ℃下反应约1 h,得化合物3。化合物3与三苯基溴化磷、醋酸乙酯、氨水在100 ℃下反应约10 h合成finerenone,合成路线见图 2。该路线由于步骤较多,合成过程中生成杂质多,并且杂质难以从最终产物中除去,这种副产物的生成影响了finerenone的纯度和收率。
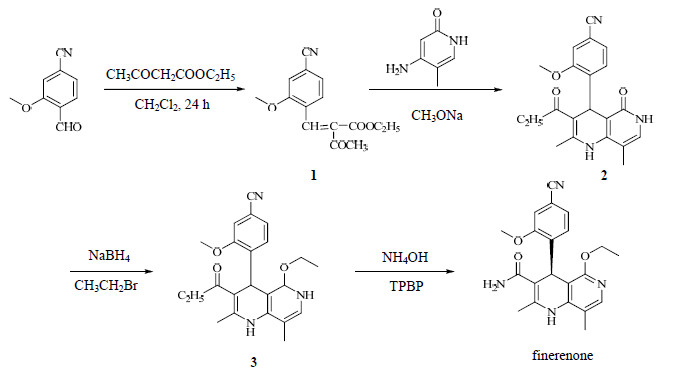 | 图 2 finerenone 的合成路线一 Fig.2 No. 1 synthesis route of finerenone |
第2条合成路线[4]是先将各个中间体制备好,参照二氢吡啶环合方法,将2-甲氧基-4-氰基苯甲醛和氨基丁烯酸甲酰胺、3-甲基-4,5-二氯-6-乙氧基吡啶采用一锅法制备finerenone,操作简单,收率高,适合工业生产,合成路线见图 3。
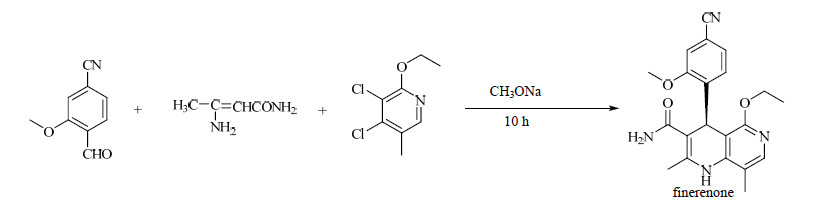 | 图 3 finerenone 合成路线 二 Fig.3 No. 2 synthesis route of finerenone |
醛甾酮通过在远端肾单位的上皮细胞中促进钠潴留和钾分泌,而在保持流体和电解质内环境稳定方面起到关键作用,因此有助于保持细胞外体积恒定和有助于调节血压。除此之外,醛甾酮在心血管系统的结构和功能上显示出直接效应,但是其所基于的机制尚未得到充分解释。醛甾酮是形成于肾上腺皮质中的甾类激素,它的产生极大地取决于肾血流量而被间接地调节。肾血流量的任何减少都导致肾中的酶肾素释放入循环血液。这进而激活血管紧张素Ⅱ的形成,一方面对动脉血管具有收缩作用,但另一方面也剌激肾上腺皮质中醛甾酮的形成。因此,肾作为血液循环中的血压传感器,也间接用作体积传感器,且经肾素-血管紧张素-醛甾酮体系抵消体积的严重损失,这一方面是通过增加血液压力(血管紧张素Ⅱ效果),另一方面通过增加肾中钠和水的再吸收来重新平衡血管系统的填充状态来实现。该控制系统可能以各种方式发病。如肾血流量的慢性减少导致过量的释放醛甾酮,进而血容量的膨胀和由此通过增多地供应血容量使心脏虚弱。另外,过量的醛甾酮效果导致血液和细胞外液中钾浓度减少,在之前已经以其他方式受损的心肌中,如果存在低于临界最小值水平可能诱发具有致命结果的心律不齐。这很可能是患有心力衰竭的患者中经常出现的心源性猝死的主要起因之一[5]。
由于其作用机制,finerenone适用于预防处于心源性猝死的增加风险中的心源性猝死,特别为患有如下病症患者:原发性和继发性高血压、有或没有充血性心力衰竭的高血压心脏病、抵抗疗法的高血压、急性和慢性心力衰竭、冠心病、稳定性和不稳定性心绞痛、心肌缺血、心肌梗死、扩张型心肌病、先天的原发性心肌病。该化合物可以预防和/或治疗浮肿形成,如肺水肿、肾原性水肿或心力衰竭相关的浮肿。
4.2 药理作用为研究finerenone治疗心衰的效果,分别在大鼠、兔和狒狒中进行动物模型试验[6]。清醒大鼠慢性充血性心力衰竭模型,雄性Wistar大鼠(体质量280~300 g),用5%异氟烷在麻醉笼里麻醉,连接到通气泵(50下/min,7 mL),并且通入2%异氟烷,体温通过加热垫维持在37~38 ℃。给予5 mg/kg finerenone,用药8周,在第3和第4根肋骨之间横向地打开胸部,露出心脏,分离腹主动脉和左肾动脉,应用超声心动图动态监测左室舒张末期内径、舒张末期室间隔厚度和左室后壁厚度。并制作病理切片,经染色后置光镜下观察心肌组织形态和纤维化程度,给药8周后,基本恢复造模前的症状。在兔和狒狒模型中,分别给予finerenone 5 mg/kg,结果显示均对醛固酮增多症和心衰发展具有显著的保护作用。给药10周后,finerenone呈剂量相关性地降低血压、蛋白尿、心脏和肾脏质量,并且改善收缩压和舒张压功能,呈剂量相关地抑制肥大和纤维化。药动学研究发现,finerenone在大鼠、狗、猴的动物试验中,表现出良好的生物利用度(35%~50%)。
盐皮质激素受体拮抗剂改善慢性心力衰竭的终末器官损害,新的非甾体类盐皮质激素受体拮抗剂finerenone具有独特的药效和选择性。大鼠疾病模型显示finerenone均匀的分配到大鼠心、肾组织[7]。finerenone减少心肌肥厚,减少血浆脑钠肽前体蛋白量。在大鼠慢性心力衰竭发展冠状动脉结扎后,finerenone可以提供器官保护,降低电解质紊乱的风险,具有独特的双重作用模式,能增加心脏输出,并使血管扩张,在改善心脏泵功能时并不增加心率,能有效缓解症状。其也能使静脉、动脉和脑血管扩张,降低前负荷和后负荷,改善冠状血流。
5 临床研究 5.1 Ⅰ期临床选择健康受试者服用finerenone,发现盐皮质激素受体拮抗剂体内吸收良好。一项随机开放性研究中,60例健康受试者分成6组,每日口服finerenone 2.5、5、7.5、10、15、25 mg/次,对其药动学研究发现,每日服用5、10 mg/次组,血浆中finerenone的血药浓度达到5~20 ng/mL就会产生作用,口服生物利用度达到40%左右,半衰期为15 h,平均在口服后1~3 h后血药浓度达到峰值。另一项40名糖尿病引起充血性心力衰竭患者(平均年龄56岁)的研究中,服用finerenone 10 mg/d,血浆中finerenone的含量达到10~20 ng/mL,口服生物利用度达到40%~50%,半衰期为15 h,平均在口服后3 h血药浓度达到峰值[8],血流动力学应激标志物是有效的,在所有的临床研究中都显示出良好的耐受性,副作用是胃肠道反应,如恶心、呕吐和腹泻。
5.2 Ⅱ期临床这个多中心、随机、双盲、平行、安慰剂对照的Ⅱ期临床研究题目为糖尿病肾病的盐皮质激素受体拮抗剂的研究研究。参加试验的纳入标准为:2型糖尿病,蛋白尿≥30 mg/g,血钾水平≤4.8 mmol/L。821例患者随机分为治疗组和对照组,治疗组的患者服用剂量为10 mg/d的finerenone,对照组服用相对应量的安慰剂,疗程为60 d,764例患者完成了该试验。结果显示两组在不良事件上无显著差异。主要有效性的测量终点为发病率,以及安全治疗后48 h内发生严重不良事件的情况[9]。由此可以看出,finerenone是安全有效的口服抗慢性心力衰竭药物。在2015年欧洲心脏病学会报告上,Ⅱ期临床研究显示finerenone对2型糖尿病和/或慢性肾脏疾病患者的心衰有一定程度的改善。
在另一组Ⅱ期临床研究中[10],将508例充血性心力衰竭患者随机分为2个双盲剂量组,finerenone 10 mg/d,螺内酯40 mg/d对照组,通过心电图、X线检查、超声心动图等临床观察,finerenone组有效率为92%,螺内酯组有效率为88%,出现轻微的恶心、呕吐、腹泻等消化道不良反应。哈佛大学的Robert教授评价近年来糖尿病肾病引起的心力衰竭发病速度快速增长,目前还缺乏有效药物,如果有一种新药能有效治疗,那将意义非凡。因此有必要对finerenone进行一个长期研究以观察其对肾小球滤过率和白蛋白尿的影响。
5.3 Ⅲ 期临床finerenone是第3代盐皮质激素受体拮抗剂,在临床前、I期、II期临床研究中已展现出较好的疗效和安全性。正在进行的Ⅲ期临床研究是一项双盲、对照、国际多中心的临床试验,主要是为了判定finerenone的安全性和有效性[11]。试验以被诊断为心脏衰竭、呼吸衰竭等疾病之一的患者为研究对象,随机分成两组,其中一组为finerenone 10 mg/d,另一组是依普利酮40 mg/d,两组均治疗60 d,这项研究预计招收3 600例受试者,来自23个国家,比较口服finerenone(1次/d)和依普利酮(1次/d)在治疗心衰恶化、2型糖尿病和/或慢性肾病患者时的安全有效性。在1 300例心力衰竭并具有相关症状的患者中评价了其疗效,finerenone给药后一般在20~30 min起效。参与者的平均年龄为64.2岁,78%为男性。在基线时,36.7%患者有很高的蛋白尿(≥300 mg/g)和40%患者肾小球滤过率为60 mL/ (min∙1.73 m2)或更低[12]。结果表明finerenone给药后尿白蛋白与肌酐比值的剂量相关性降低。finerenone组个体次要终点较依普利酮组有所降低。结果表明糖尿病肾病患者中,大多数接受血管紧张素转换酶抑制剂或血管紧张素受体拮抗剂的加入,finerenone与安慰剂相比导致尿白蛋白与肌酐比值的改善,需要进一步的试验来比较finerenone与其他活性药物,且受体亲和力优于依普利酮,可以改善肾功能标志物,与其他非甾体激素受体拮抗剂相比,finerenone出现高钾血症的概率低很多。结果显示,finerenone安全有效,能改善患者的预后,并能保持良好的血流动力学作用。
6 安全性将健康受试者分成5组,分别口服单剂量的finerenone 2.5、5、10、20、40 mg/d,结果没有受试者退出或出现严重的不良事件,并且随着剂量的增加,药时曲线下面积的增加不呈正比(剂量增加,清除率下降)。研究表明,finerenone具有很好的安全性。对药物之间相互作用的临床研究中,将健康的受试者分为两组,一组接受finerenone 10 mg/d,另一组服用依普利酮40 mg/d,持续28 d。结果发现,finerenone耐受性良好,没有严重不良事件的报告,并且发现finerenone也没有产生相互作用[13]。临床研究发现finerenone的主要不良反应是大剂量服用时会出现恶心、腹泻等消化道症状。
7 结 语近年来糖尿病肾病引起慢性心衰的发病速度快速增长,目前还缺乏有效药物,药物的研究重点是有一种新药能有效、更安全、更具针对性的治疗。随机试验发现,糖尿病肾病患者在肾素-血管紧张素系统的阻断剂药物中加用finerenone后,可以改善肾功能标志物,与其他非甾体类激素受体拮抗剂相比,finerenone出现高钾血症的概率很低。而finerenone是一个比螺内酯的受体选择性更大、受体亲和力比依普利酮更好的盐皮质激素受体拮抗剂,这将成为全球超过3千万患者的福音。当然,finerenone仍处于研究阶段,真正对某种疾病的疗效还需更多的循证医学依据。通过诸多的研究成果及数据监测,相信现在的抗慢性心衰治疗水平将发生重大变革。
| [1] | Amazit L, Le Billan F, Kolkhof P, et al. Finerenone impedes aldosterone-dependent nuclear import of the mineralocorticoid receptor and prevents genomic recruitment of steroid receptor coactivator-1[J]. J Biol Chem, 2015, 290(36): 21876-21889. |
| [2] | Bärfacker L, Kuhl A, Hillisch A, et al. Discovery of BAY 94-8862: a nonsteroidal antagonist of the mineralocorticoid receptor for the treatment of cardiorenal diseases[J]. Chem Med Chem, 2012, 7(8): 1385-1403. |
| [3] | Searls T, McLaughlin L W. Preparation of 4-aryl-1,4- dihydro-1,6-naphthyridine amides[J].Tetrahedron, 1999, 55(6): 11985-11996. |
| [4] | Lars B, Peter K, Karl-heinz S, et al. Substituted 4-aryl-1,4-dihydro-1,6-naphthyridinamides and use thereof [P]. WO: 2008104306, 2008-09-04. |
| [5] | Pitt B, Anker S D, Böhm M, et al. Rationale and design of MinerAlocorticoid Receptor antagonist Tolerability Study-Heart Failure (ARTS-HF): a randomized study of finerenone vs. eplerenone in patients who have worsening chronic heart failure with diabetes and/or chronic kidney disease[J]. Eur J Heart Fail, 2015, 17(3): 224-232. |
| [6] | Kolkhof P, Delbeck M, Kretschmer A, et al. Finerenone, a novel selective nonsteroidal mineralocorticoid receptor antagonist protects from rat cardiorenal injury[J]. J Cardiovasc Pharmacol, 2014, 64(1): 69-78. |
| [7] | Bramlage P, Swift S, Thoenes M, et al. Non-steroidal mineralocorticoid receptor antagonism for the treatment of cardiovascular and renal disease[J]. Eur J Heart Fail, 2015, doi: 10.1002/ejhf.444. |
| [8] | Ruilope L M, Agarwal R, Chan J C, et al. Rationale, design, and baseline characteristics of ARTS-DN: a randomized study to assess the safety and efficacy of finerenone in patients with type 2 diabetes mellitus and a clinical diagnosis of diabetic nephropathy[J]. Am J Nephrol, 2014, 40(6): 572-581. |
| [9] | Pitt B, Kober L, Ponikowski P, et al. Safety and tolerability of the novel non-steroidal mineralocorticoid receptor antagonist BAY 94-8862 in patients with chronic heart failure and mild or moderate chronic kidney disease: a randomized, double-blind trial[J]. Eur Heart J, 2013, 34(31): 2453-2463. |
| [10] | Pitt B, Anker S D, Böhm M, et al. Rationale and design of MinerAlocorticoid Receptor antagonist Tolerability Study- Heart Failure (ARTS-HF): a randomized study of finerenone vs. eplerenone in patients who have worsening chronic heart failure with diabetes and/or chronic kidney disease[J]. Eur J Heart Fail, 2014, 16(2): 224-232. |
| [11] | Pitt B, Filippatos G, Gheorghiade M, et al. Rationale and design of ARTS: a randomized, double-blind study of BAY 94-8862 in patients with chronic heart failure and mild or moderate chronic kidney disease[J]. Eur J Heart Fail, 2012, 14(6): 668-675. |
| [12] | Bakris G L, Agarwal R, Chan J C, et al. Effect of finerenone on albuminuria in patients with diabetic nephropathy: a randomized clinical trial[J]. JAMA, 2015, 314(9): 884-894. |
| [13] | Bauersachs J. The ARTS of third-generation mineralocorticoid receptor antagonists: achieving cardiovascular benefit with minimized renal side effects?[J]. Eur Heart J, 2013, 34(31): 2426-2428. |
 2016, Vol. 31
2016, Vol. 31

