达格列净是由百时美施贵宝公司和阿斯利康公司开发的钠依赖性葡萄糖转运蛋白(SGLT)抑制剂,化学名为2-氯-5-(β-D-吡喃葡萄糖-1-基)-4′-乙氧基二苯甲烷。2012年12月在欧盟上市,2014年1月在美国上市,商品名为Farxiga。研究显示,SGLT (主要是SGLT2)可调节血糖在肾小球的滤过重吸收过程,因此达格列净通过对SGLT2的抑制作用,阻止葡萄糖在肾脏的重吸收,增加葡萄糖在尿液中的排泄从而起到降低血糖的作用,是非常有效的SGLT2抑制剂[1,2,3]。根据文献报道的达格列净的合成工艺[4,5,6,7],分析其可能存在的微量杂质包括:合成中间体,如5-溴-2-氯-4′-乙氧基二苯甲酮(Z1)、5-溴-2-氯-4′-乙氧基二苯甲烷(Z2);副反应产物,如2-溴-5-(β-D-吡喃葡萄糖-1-基)-4′-乙氧基二苯甲烷(F1)、2-氯-4′-乙氧基二苯甲烷二聚物(F2)、2-氯-5-(β-D-吡喃葡萄糖-1-基)-2′-乙氧基二苯甲烷(F3)。本实验建立了达格列净原料药中有关物质的检测方法,结果表明该方法灵敏度高、重复性好、专属性强,可以作为达格列净原料药中有关物质的控制方法。
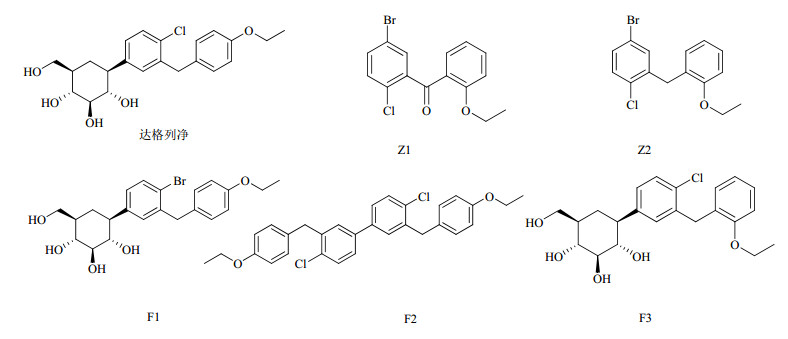 | 图 1 达格列净及有关物质的化学结构Fig.1 Chemical structures of dapagliflozin and its related substances |
Agilent 1290高效液相色谱仪;XS205DU型电子分析天平(梅特勒-托利多公司)。
达格列净(批号140504,质量分数为99.8%)、Z1(批号140402,质量分数为99.0%)、Z2(批号140402,质量分数为99.2%)、F1(批号140602,质量分数为99.1%)、F2(批号140702,质量分数为98.0%)、F3(批号140715,质量分数为98.3%)对照品均由深圳振强生物技术公司提供;达格列净原料药(批号分别为140909粗品、140909、140910、140911,规格20 kg/桶)均为自制。甲醇、四氢呋喃为色谱纯,水为纯化水,其他试剂均为分析纯。
2 方法与结果 2.1 色谱条件Diamonsil C18色谱柱(250 mm×4.6 mm,5 μm);以0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)为流动相;体积流量1.0 mL/min;检测波长220 nm;柱温35℃;进样量为10 μL。
2.2 溶液的制备 2.2.1 对照品溶液储备液的制备称取达格列净、杂质Z1、Z2、F1、F2、F3对照品各约10 mg,精密称定,置25 mL量瓶,加甲醇溶解并稀释至刻度,摇匀,即得。
2.2.2 供试品溶液的制备取达格列净原料药约10 mg,精密称定,置25 mL量瓶,加0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)溶解并稀释至刻度,摇匀,即得。精密量取1.0 mL,置1 000 mL量瓶,加0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)稀释至刻度,摇匀,即得0.1%自身对照溶液。
2.3 系统适用性试验取达格列净原料药约10 mg,精密称定,置25 mL量瓶,加入杂质对照品储备液0.1 mL,再加0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)溶解并稀释至刻度,摇匀。精密量取10 μL,连续进样6次,记录色谱图。结果各杂质峰分离度均大于1.5,主峰拖尾因子在0.9~1.1,主成分与杂质峰面积的RSD值均在1.5%以下,符合系统适用性要求。已知杂质以外标法计算,未知杂质以主成分1%自身对照法计算。限度:单个杂质的峰面积不得大于1%对照溶液的主峰峰面积的1/10,总杂质峰面积之和不得大于1%对照溶液主峰峰面积的1/2。
2.4 专属性试验取达格列净、杂质对照品溶液储备液,移取0.1 mL置25 mL量瓶中,加甲醇溶解并稀释至刻度。精密量取10 μL,进样,记录色谱图,杂质Z1、Z2、F1、F2、F3与达格列净的分离度都大于1.5,各个杂质之间的分离度都大于1.5。
取3份达格列净原料药粗品(批号为140909粗品)约10 mg,分别加1 mol/L盐酸溶液0.5 mL、1 mol/L氢氧化钠溶液0.5 mL,30%过氧化氢溶液1 mL,置60℃水浴加热30min,取出冷却,调至中性,即得酸、碱、氧化降解样品;另取达格列净原料药粗品适量,分别置于80℃烘箱及5 000 lx光照试验箱中放置7 d,即得高温、强光照降解样品。分别取各样品,制备供试品溶液,进样测定,色谱图见图2。结果表明,降解产物与达格列净能完全分离。达格列净原料药在酸、碱和氧化条件下不稳定,产生较多的降解杂质。因此在储存运输过程中,应避免接触酸、碱,且应密闭保存。
 | 图 2 达格列净加已知杂质(A)、酸降解样品(B)、碱降解样品(C)、氧化降解样品(D)、高温降解样品(E)、强光照降解样品(F)、粗品(G)和系统适应性溶液(H)的HPLC图谱Fig.2 HPLC chromatograms of dapagliflozin spiked with known impurities (A), acid degradation sample (B), alkaline degradation sample (C), oxidative degradation sample (D), high-temperature degradation sample (E), light degradation sample (F), crude sample(G),and system adaptive solution(H) |
取达格列净、杂质对照品溶液储备液,用0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)逐渐稀释至信噪比(S/N)约为3,所得溶液即为检出限试验供试品溶液。用0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)逐渐稀释至信噪比(S/N)约为10,所得溶液即为定量限试验供试品溶液。结果表明:达格列净及杂质Z1、Z2、F1、F2、F3的检测限分别为1.63、1.34、1.54、1.42、1.71、2.11 ng,达格列净及杂质Z1、Z2、F1、F2、F3的定量限分别为4.11、3.22、3.83、3.65、4.33、4.92 ng。
2.6 线性关系考察取达格列净及杂质对照品溶液储备液,加0.02 mol/L磷酸二氢钠水溶液-甲醇-四氢呋喃(60:35:5)稀释制成0.40、1.0、2.0、2.5、4.0 μg/mL溶液。精密量取10 μL,进样分析,记录色谱图。以峰面积为纵坐标,质量浓度为横坐标,进行线性回归,得回归方程,见表1。
| 表 1 达格列净及已知杂质的线性关系结果 Table 1 Linearity of dapagliflozin and its impurity |
取2.5 mg/mL达格列净原料药(批号140909)供试品溶液,放置0、1、2、4、8、10 h后分别进样测定,考察达格列净及杂质Z1、Z2、F1、F2、F3、其他最大单杂和总杂的变化。结果表明,最大单杂F1的质量分数分别为0.08%、0.08%、0.07%、0.08%、0.08%、0.06%,无明显变化,表明溶液在10 h内稳定。
2.8 精密度试验平行制备6份2.5 mg/mL达格列净原料药(批号140909)供试品溶液和1%自身对照溶液,分别进样测定,结果未知最大杂质、F1的RSD值分别为1.3%、1.4%。
2.9 回收率试验取达格列净原料药约10 mg,精密称定,置25 mL量瓶,分别加入达格列净及杂质对照品溶液储备液0.015、0.020、0.025、0.030、0.035 mL,制备供试品溶液,每个质量浓度制备3份供试品溶液,进样测定,计算回收率,结果杂质Z1、Z2、F1、F2、F3的平均回收率分别为98.9%、97.6%、103.2%、102.4%、102.8%,RSD值分别为1.8%、1.3%、1.5%、0.7%、1.7%。
2.10 样品测定取批号140909、140910、140911达格列净原料药适量,制备供试品溶液,进样测定。已知杂质以外标法计算,未知杂质以主成分1%自身对照法计算。结果见表2。结果表明,3批样品中有关物质的检测结果在合格范围之内,单个杂质与总的杂质都小于限度。
| 表 2 达格列净原料药中有关物质的测定结果 Table 2 Determination of related substances in dapagliflozin active pharmaceutical ingredient |
实验筛选了多种填料的色谱柱,包括Waters XBridge苯基色谱柱、Waters Spherisorb氨基柱、Waters Xselect C18色谱柱、Agilent SB-C18色谱柱、Diamonsil C18色谱柱。其中Waters XBridge苯基色谱柱、Waters Spherisorb氨基柱对于杂质的分离都不是很理想。C18柱色谱柱比较适用于杂质的分离,其中Diamonsil C18色谱柱主峰与杂质的分离度良好且峰形对称。
3.2 流动相的选择流动相的选择和优化是整个色谱条件摸索过程中的难点,需要从不同的角度进行筛选。其中有机溶剂的种类和配比,以及缓冲盐的种类、浓度和pH值等对保留时间、峰形和分离度都有一定的影响[8]。实验分别考察了有机相的种类、缓冲盐的种类、缓冲盐浓度、流动相比例。特别是在考察有机相的种类时,首先考察了常用的甲醇和乙腈,最后考察了四氢呋喃体系,虽然该体系平衡过程比较长,但是相对于常用的甲醇和乙腈系统,主成分与杂质都得到了有效的分离。在考察缓冲盐浓度时,分别考察了0.01、0.02、0.04 mol/L磷酸二氢钠水溶液为缓冲盐溶液对供试品溶液出峰情况及含量的影响,随着缓冲盐浓度的增加,主峰的峰面积也随着增加,同时峰形也会发生变化,最终确定0.02 mol/L为最佳缓冲盐溶液浓度。
| [1] | Cole P, Vicente M, Castaner R. Dapagliflozin. SGLT2 inhibitor, Antidiabetic agent [J]. Drugs Future, 2008, 33(9):745-751. |
| [2] | Meng W, Ellsworth B A, Nirschl A A, et al. Discovery of dapagliflozin: a potent, selective renal sodium-dependent glucose cotransporter 2 (SGLT2) inhibitor for the treatment of type 2 diabetes [J]. J Med Chem, 2008, 51(5): 1145- 1149. |
| [3] | 石卫峰, 李晓宇, 刘皋林. 治疗2型糖尿病新药达格列净 [J]. 中国新药杂志, 2013, 22(16): 1861-1863. |
| [4] | 禹艳坤, 冀亚飞. 达格列净的合成 [J]. 中国医药工业杂志, 2011, 42(2): 84-87. |
| [5] | 张帅阳, 徐 斌, 王德才. 达格列净合成路线图解 [J]. 中国医药工业杂志, 2014, 45(12): 1192-1195. |
| [6] | 张玲钰. SGLT2抑制剂达格列净脱氧衍生物的研究 [D]. 济南: 山东大学, 2014. |
| [7] | 任建国, 吴沙沙, 刘 爽, 等. 达格列净的合成工艺改进 [J]. 中国药物化学杂志, 2014, 24(5): 375-379. |
| [8] | 全红娜, 金松子, 雷勇胜, 等. 反相高效液相色谱中流动相选择与优化的研究进展 [J]. 现代药物与临床, 2015, 29(10): 1190-1194 |
 2015, Vol. 30
2015, Vol. 30

