1 药物概况
通用名:缬沙坦/sacubitril三钠水合物
别名:LCZ696、缬沙坦/AHU377
化学名:N-(1-戊酰基)-N-[4-[2-(1H-四氮唑-5-基)苯基]苄基]-L-缬氨酸/4-(((2S,4R)-1-([1,1'-联苯]-4-基)-5-乙氧基-4-甲基-5-氧代戊烷-2-基)氨基)-4-氧代丁酸
CAS:936623-90-4
分子式:(C24H29N5O3)·(C24H29NO5)Na3·2.5(H2O)
相对分子质量:961.03
结构见图 1
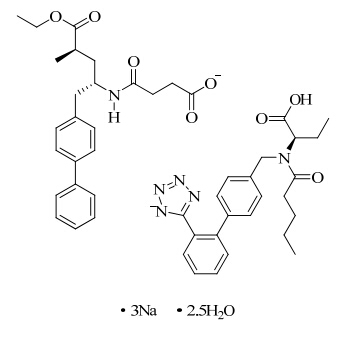 | 图 1 LCZ696的结构式Fig. 1 Structure of LCZ696 |
原研公司:诺华
适应症:心力衰竭
目前阶段:Ш期临床
给药途径:口服
2 相关背景心力衰竭是由于心脏不能泵出足够的血液供应全身,由此引发呼吸困难、疲劳等一系列症状的致命性疾病,严重影响患者的生活质量。肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone,RAAS)是射血分数降低心力衰竭(heart failure and a reduced ejecion fraction,HFrEF)患者的有效治疗靶点,尽管使用血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体拮抗剂、β受体阻滞剂能改善生存,但是仍有50%的患者在确诊后5年内死亡。对于射血分数正常心力衰竭(heart failure with preserved ejection fraction,HFpEF)患者来说,目前还没有降低发病率和死亡率的治疗方法。脑啡肽酶属于一种中性肽链内切酶,其受到抑制可以提高利钠肽、缓激肽和P物质的生物活性,引起利尿、血管舒张和抗细胞增殖,进而产生明显的减轻心脏负荷和降低血压作用[1]。由于脑啡肽酶具有潜在的水解血管紧张素Ⅱ和内皮素的作用,脑啡肽酶抑制剂单独应用不能改善心力衰竭伴高血压患者的血压情况。因此,将脑啡肽酶抑制剂和RAAS抑制剂联合应用成为心力衰竭药物开发的一个重要方向[2, 3]。奥马曲拉是由
BMS公司开发的脑啡肽酶和ACEI双重抑制剂,尽管被证实能够改善患者的发病率和死亡率,但是因严重增加血管性水肿的风险而导致退市[4, 5]。造成上述不良反应增加的原因是由于该药物同时抑制了脑啡肽酶、ACEI和氨肽酶P,而使缓激肽和P物质在体内的蓄积(特别是黑色人种)[6]。诺华公司开发的LCZ696(缬沙坦/AHU377)是第一个血管紧张素Ⅱ受体-脑啡肽酶双重抑制剂,它为心力衰竭的药物治疗提供了一个新的途径[7]。
3 合成路线缬沙坦为已上市多年的经典ACEI类药物,其合成方法繁多,并无新颖性,在此不进行详细描述。
sacubitril的合成路线[8]:Boc保护的手性氨基醇在四甲基哌啶氧化物(TEMPO)的催化下使用次氯酸钠进行氧化,得到对应的脂肪醛(1);化合物1与Wittig试剂反应,得到α, β-不饱和酸酯(2),化合物2在乙醇中使用LiOH进行水解,获得对应的α, β-不饱和酸(3);化合物3在不对称催化剂的催化下室温加压下加氢,将其中的碳碳双键还原,得到α-手性的羧酸(4);化合物4在乙醇中使用SOCl2与乙醇反应,并在原位产生的HCl催化下酯化,得到对应的羧酸乙酯,同时分子中NH2上的Boc保护基被脱除,得到脱保护的羧酸乙酯(5);化合物5中游离的NH2与琥珀酸酐反应得到终产物sacubitril,见图 2。
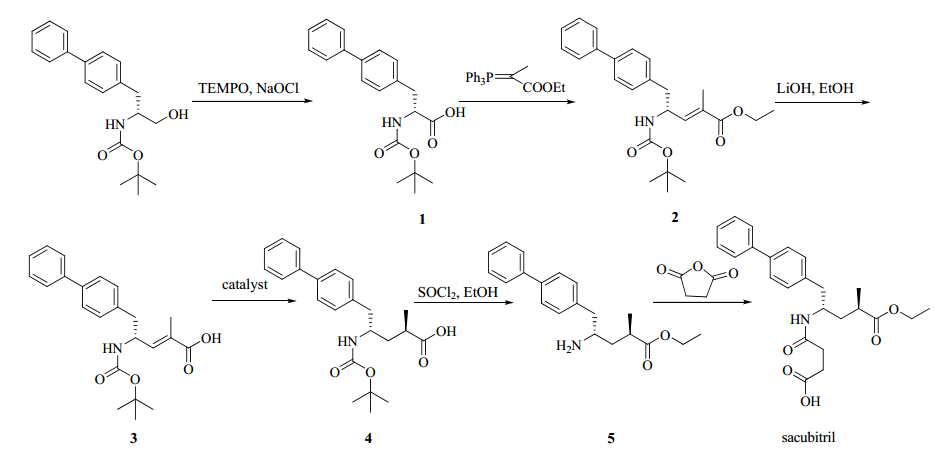 | 图 2 sacubitril的合成路线Fig. 2 Synthetic route of sacubitril |
LCZ696的制备方法[9]:1 mol sacubitril的游离酸和1 mol缬沙坦的游离酸溶于一定体积的丙酮中,搅拌;在另一容器中将3 mol NaOH溶于一定体积的水。将两溶液混合,并在室温下搅拌1 h,获得澄清的溶液。该溶液在35 ℃下蒸干,获得一个玻璃状的固体,在其中加入一定体积的丙酮,超声波超声,直到获得沉淀。抽滤收集沉淀,并在空气中室温下干燥2 d,直到恒定质量,即可得到三钠盐水合物。各种表征方法确定了LCZ696的结构组成,且肯定其不是简单的sacubitril钠盐和缬沙坦二钠盐的物理混合。
4 作用机制和药理作用利钠肽是维持体内水钠平衡的一个重要的神经内分泌激素家族,它们可以抑制RAAS、减少交感神经运动、降低血压和抗细胞增殖[10]。该家族包括3个成员:心钠肽(atrial NP,ANP)、脑钠肽(brain NP,BNP)和C型钠肽(C-type NP,CNP),前二者主要由左心室在心室壁压力增强的情况下释放,排钠利尿和舒张血管;C型钠肽主要存在于中枢神经系统、肾脏和血管内皮细胞,但具体作用机制不清楚[11, 12]。脑啡肽酶(即中性肽链内切酶24.11)为锌依赖的基质金属蛋白酶,可以催化降解包括ANP、BNP、缓激肽以及血管紧张素Ⅱ在内的多种肽类[13]。神经内分泌激活是心力衰竭发生发展的主要机制,抑制脑啡肽酶提高利钠肽水平是治疗心力衰竭的一个途径,阻断RAAS则是另一种方法,二者联合可以更好的发挥协同作用[14]。与奥马曲拉比较,LCZ696无直接抑制ACEI和氨肽酶P的作用,并且降低了血管性水肿的风险[15]。在作用机制上,该药物可以通过舒张血管、排钠利尿、抑制交感神经运动和RAAS、防止心肌细胞肥大和纤维化、降低前后负荷,使心力衰竭患者的心脏和肾功能均受益[16]。
LCZ696口服片剂由缬沙坦(已知的血管紧张素受体拮抗剂)和AHU377(前药,可以迅速代谢为活性产物LBQ657)按物质的量1∶1共结晶形成。在一项临床前研究中[17],比格犬单剂量分别经口给予LCZ696片(300 mg,354 μmol/kg)、缬沙坦(160 mg,367 μmol/kg)+AHU377(100 mg,232 μmol/kg)片后,缬沙坦的达峰时间(tmax)分别为1.3、4 h,给药后,前者中缬沙坦的药时曲线下面积(AUC)和峰浓度(Cmax)系统暴露量约为后者的3倍;而AHU377活性产物LBQ657的系统暴露量在两组之间相似,表明LCZ696片的成药形式促进了缬沙坦的吸收,而对LB Q657的药动学无明显影响。此外,LCZ696(2~60 mg/kg)可以剂量相关地降低肾素- 血管紧张素原高表达转基因高血压大鼠(dTGR)的平均动脉压,以及提高SD大鼠血浆中心钠肽的免疫活性[17]。
5 临床研究 5.1 Ⅰ期临床在一项Ⅰ期临床研究中[17],健康受试者单剂量分别口服LCZ696片(200~1 200 mg)后,缬沙坦、AHU377及活性产物LBQ657的tmax分别为1.7~2.2、0.5~1.1、1.9~3.5 h;平均半衰期(t1/2)分别为8.9~16.6、1.1~3.6、9.9~11.1 h;多剂量口服LCZ696片(50~900 mg,1次/d),14 d后,缬沙坦、AHU377及LBQ657的tmax分别为1.6~4.9、0.6~0.9、1.8~2.7 h,比较首次给药和末次给药后AUC和Cmax的暴露量,三者并无蓄积现象;单剂量口服LCZ696片(400 mg)和缬沙坦片(320 mg)后,缬沙坦于二者的平均tmax分别为2、4 h;平均t1/2相近,约为18 h;AUC和Cmax也比较相近。按等剂量系统暴露的分析比较,LCZ696片的暴露量约为缬沙坦片的1.4倍。在健康受试者的剂量探索试验中[17],与安慰剂比较,LCZ696(200 ~900 mg/kg)中AHU377活性产物LBQ657可以使受试者心钠肽和环磷酸鸟苷(cGMP)升高,其中,服药4 h后平均cGMP水平最大提高40%,24 h后恢复到基线值;同样,缬沙坦也可以显著提高肾素的浓度(93%~6 34%)、血浆肾素活性(280%~1 768%),以及AngⅡ(241%~1 188%)的水平。
上述结果提示,LCZ-696具有抑制脑啡肽酶和阻断血管紧张素受体Ⅰ的双重作用,缬沙坦和LBQ657具有相似的药动学特性,二者升高血浆中cGMP和RAAS标志物达最大浓度的时间也相近(4 h),可以更好的协同发挥药效作用。
5.2 Ⅱ期临床一项随机、平行、双盲、多中心的为Ⅱ期试验[18],共纳入301例纽约心脏病协会(NYHA)Ⅱ~Ⅲ级心衰、左室射血分数为≥45%、NT-pro BNP>400 pg/mL的患者。患者随机分成两组,即LCZ696滴注(200 mg,2次/d)或缬沙坦滴注(160 mg,2次/d),治疗36周。主要终点为基线至12周的左室壁应力标志物NT-proBNP的变化。结果显示:LCZ696组和缬沙坦组分别有134、132例患者达到了主要终点。治疗12周时,与缬沙坦组相比,LCZ696组的NT-proBNP水平显著降低。LCZ696组的不良反应发生率与缬沙坦组相近。其中,LCZ696组有22例(15%)患者,缬沙坦组有30例(20%)患者发生一个以上严重不良反应事件。研究表明,与缬沙坦比较,LCZ696可将射血分数正常心衰患者的NT-proBNP降低更多,治疗12周后患者的耐受性良好。
5.3 Ⅲ期临床2014年11月,关于LCZ696最大规模的Ш期临床试验——PARADI ARADI GM-HF研究公布[19]:该研究纳入8 000多例NYHA心功能Ⅱ~Ⅳ级的典型HFrEF患者,对比了LCZ696(200 mg,2次/d)和依那普利(10 mg,2次/d)两个治疗方案。研究于2014年3月初停止,结果显示,针对院外治疗患者,LCZ696组比依那普利组生存期更长。2014年8月,该研究的最新数据显示,与依 那普利相比,LCZ696使猝死率降低了20%,心衰住院风险降低了21%,全因死亡率降低了16%。同时,还使重症监护治疗的需求降低了16%,使因急症恶化而必须急诊治疗的需求降低了30%。
当入院治疗时,LCZ-696和依那普利组患者住院时间一样,但LCZ696组需要重症监护的时间缩短了18%,同时需要静脉注射药物帮助其心脏泵血的需求减少了31%。根据疾病的严重程度和恢复程度,医生和患者对LCZ696的评价都比依那普利好;同时,与依那普利相比,LCZ696能够使与心脏负荷和心脏损伤相关的心脏生物标志物(NTpro-BNP和肌钙蛋白)水平始终较低。结果表明,LCZ696有望改善HFrEF患者的疾病进程。
6 安全性和耐受性在PARADI ARADI GM-HF研究中,与依那普利组相比,LCZ696组并未增加严重血管性水肿的发生率;LCZ696组出现较频繁的症状性低血压发作(P<0.001),但未导致比依那普利组更多的停药;LCZ696组肾损伤、高钾血症和咳嗽的发生率较低,对基础心率和血清肌酐水平也无明显影响[19]。截至目前,LCZ696所报道的临床安全性和耐受性良好。
7 其他糖尿病和慢性肾病是心力衰竭患者的常见并发症。PARAMOUNT试验研究显示[20],与缬沙坦比较,LCZ696治疗36周后,可以降低HFpEF患者血清肌酐水平(P<0.05),并提高估算的肾小球滤过率(P<0.05)。此外,一项Meta分析研究表明[21],与RAAS抑制剂单独应用比较,LCZ696对心力衰竭患者肾功能具有积极的作用,该作用可能与脑啡肽酶抑制剂舒张肾小球入球小动脉,增加肾髓质血流量,促进利尿利钠有关。
8 结语过去25年内,将ACEI、血管紧张素受体拮抗剂、β受体阻滞剂、利尿剂、醛固酮受体拮抗剂、脑啡肽酶抑制剂中的几种联合应用一直是心力衰竭药物治疗的基础方案和研究热点。LCZ696在药物设计上吸取了奥马曲拉失败的教训,降低了血管性水肿的风险,使缬沙坦和LBQ657在作用机制上互补重叠,并通过共结晶的成药形式优化二者的药动学特征,也提高了患者的顺应性。它不仅能够降低死亡或住院风险,还能够降低或减缓心脏功能衰竭速度,潜在改变疾病进展,为HFrEF的治疗提供了希望,此外,针对HFpEF和高血压适应症的临床试验也正在进行[22]。LCZ696无疑是心衰治疗领域的一个伟大突破,它的成功将促进血管紧张素受体-脑啡肽酶抑制剂的进一步发展,因此,该类药物将具有非常广阔的临床应用前景和社会价值。
| [1] | Kuhn M. Molecular physiology of natriuretic peptide signaling [J]. Basic Res Cardiol, 2004, 99(2): 76-82. |
| [2] | Maric C, Zheng W, Walther T. Interactions between angiotensin ll and atrial natriuretic peptide in renomedullary interstitial cells: the role of neutral endopeptidase [J]. Nephron Physiol, 2006, 103(3): 149-156. |
| [3] | McMurray J J. Neprilysin inhibition to treat heart failure: a tale of science, serendipity, and second chances [J]. Eur J Heart Fall, 2015, 17(3): 242-247. |
| [4] | Packer M, Califf R M, Konstam M A, et al. Comparison of omapatrilat and enalapril in patients with chronic heart failure: the omapatrilat versus enalapril randomized trial of utility in reducing events (OVERTURE) [J]. Circulation, 2002, 106(8): 920-926. |
| [5] | Messerli F H, Nussberger J. Vasopeptidase inhibition and angio-oedema [J]. Lancet, 2000, 356(9230): 608-609. |
| [6] | Cruden N L, Fox K A, Ludlam C A, et al. Neutral endopeptidase inhibition augments vascular actions of bradykinin in patients treated with angiotensin-converting enzyme inhibition [J]. Hypertension, 2004, 44(6): 913-918. |
| [7] | Hegde L G, Yu C, Renner T, et al. Concomitant angiotensin AT1 receptor antagonism and neprilysin inhibition produces omapatrilat-like antihypertensive effects without promoting tracheal plasma extravasation in the rat [J]. J Cardiovasc Pharmacol, 2011, 57(4): 495-504. |
| [8] | David H, Bernhard W, Matthias L, et al. Process for preparing biaryl substituted 4-amino-butryric acid or derivertives thereof and their use in the production of NEP inhibitors [P]. WO: 2008031567, 2007-09-11. |
| [9] | Li F, Erik G S, Allen S P, et al. Compounds containing S-N-valeryl-N-valine and (2R,4S)-5-biphenyl-4-yl-4-(3-carboxy-propionyl-amino)-2-methyl-pentanoic acid ethyl ester moieties and cations [P]. US: 20150057322, 2014-06-23. |
| [10] | Gardner D G, Chen S, Glenn D J, et al. Molecular biology of the natriuretic peptide system: implications for physiology and hypertension [J]. Hypertension, 2007, 49(3): 419-426. |
| [11] | Vardeny O, Miller R, Solomon S D. Combined neprilysin and renin-angiotensin system inhibition for the treatment of heart failure [J]. JACC Heart Fail, 2014, 2(6): 663-670. |
| [12] | Scotland R S, Cohen M, Foster P, et al. C-type natriuretic peptide inhibits leukocyte recruitment and platelet-leukocyte interactions via suppression of P-selectin expression [J]. Proc Natl Acad Sci USA, 2005, 102(40): 14452-14457. |
| [13] | Daniels L B, Maisel A S. Natriuretic peptides [J]. J Am Coll Cardiol, 2007, 50(25): 2357-2368. |
| [14] | Reed B N, Street S E, Jensen B C. Time and technology will tell: the pathophysiologic basis of neurohormonal modulation in heart failure [J]. Heart Fail Clin, 2014, 10(4): 543-557. |
| [15] | Makani H, Messerli F H, Romero J, et al. Meta-analysis of randomized trials of angioedema as an adverse event of renin-angiotensin system inhibitors [J]. Am J Cardiol, 2012, 110(3): 383-391. |
| [16] | Segura J, Ruilope L M. Dual-acting angiotensin receptor-neprilysin inhibition [J]. Curr Hypertens Rep, 2011, 13(1): 74-78. |
| [17] | Gu J, Noe A, Chandra P, et al. Pharmacokinetics and pharmacodynamics of LCZ696, a novel dual-acting angiotensin receptor-neprilysin inhibitor (ARNi) [J]. J Clin Pharmacol, 2010, 50(4): 401-414. |
| [18] | Solomon S D, Zile M, Pieske B, et al. The angiotensin receptor neprilysin inhibitor LCZ696 in heart failure with preserved ejection fraction: a phase 2 double-blind randomised controlled trial [J]. Lancet, 2012, 380(9851): 1387-1395. |
| [19] | McMurray J J, Packer M, Desai A S, et al. Angiotensin-neprilysin inhibition versus enalapril in heart failure [J]. N Engl J Med, 2014, 371(11): 993-1004. |
| [20] | Voors A A, Gori M, Liu L C, et al. Renal effects of the angiotensin receptor neprilysin inhibitor LCZ696 in patients with heart failure and preserved ejection fraction [J]. Eur J Heart Fail, 2015, 17(5): 510-517. |
| [21] | Bodey F, Hopper I, Krum H. Neprilysin inhibitors preserve renal function in heart failure [J]. Int J Cardiol, 2015, 179: 329-330. |
| [22] | Gradman A H. LCZ696: The next step in improving RAS inhibition [J]. Curr Hypertens Rep, 2015, 17(5): 37. |
 2015, Vol. 30
2015, Vol. 30


