2. 哈尔滨莱博通药业有限公司, 黑龙江 哈尔滨 150025
2. Harbin Laiboten Pharmaceutical Co., Ltd, Harbin 150025, China
依维莫司是免疫抑制剂西罗莫司C42位丙酸酯类衍生物,结构式见图 1。由诺华公司研发,临床上主要用于预防心脏移植和肾移植手术后的排异反应[1]。依维莫司也是一种mTOR激酶抑制剂,可阻断细胞周期从G1期到S期进程,导致癌细胞死亡,2009年FDA批准其用于治疗使用舒尼替尼或索拉非尼无效的晚期肾癌[2]。另外依维莫司还具有抑制血管内皮细胞增殖的作用,用作药物支架的涂层药物可防止冠状动脉支架植入后血管再狭窄[3]。本实验建立反相高效液相色谱法测定依维莫司原料药中依维莫司,该方法操作简便,专属性强,为依维莫司原料药的质量控制提供了准确可行的分析方法。
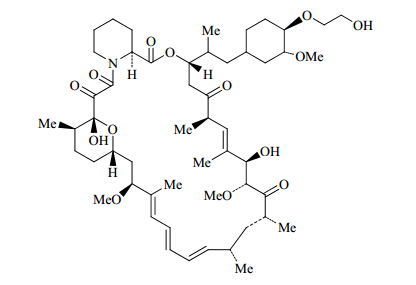 | 图 1 依维莫司的结构式Fig. 1 Structure of everolimus |
Agilent 1260高效液相色谱仪,Agilent色谱工作站;CPA225D型电子天平(北京赛多利斯仪器有限公司)。
1.2 药品与试剂依维莫司原料药(武汉贝尔卡生物医药有限公司),依维莫司对照品(质量分数99%,Aladdin),甲醇(色谱纯,Fisher公司)、乙腈(色谱纯,Fisher公司),其他试剂均为分析纯,水为纯化水。
2 方法与结果 2.1 色谱条件Hypersil-ODS C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(70∶30);检测波长:276 nm;柱温:50 ℃;体积流量:0.8 mL/min;进样量:10 μL。
2.2 溶液的配制取依维莫司原料10 mg,精密称定,置于10 mL量瓶中,用流动相乙腈-水(70∶30)溶解并加至刻度,摇匀,作为供试品溶液。取依维莫司对照品10 mg,精密称定,置于10 mL量瓶中,用流动相乙腈-水(70∶30)溶解并稀释至刻度,摇匀,即得对照品溶液。
2.3 专属性试验取供试品溶液适量,分别经2 mol/mL硫酸溶液(室温放置1 h)、2 mol/L氢氧钠溶液(室温放置1 h)、10%过氧化氢溶液(室温放置1 h)、80 ℃高温1 h进行破坏。精密量取上述溶液分别注入色谱仪,记录色谱图。结果表明,依维莫司经酸、碱、氧化、高温破坏,所产生的降解产物与主成分均能完全分离,不干扰依维莫司的测定。色谱图见图 2。
 | *-依维莫司 *-everolimus图 2 酸破坏试验(A)、碱破坏试验(B)、氧化破坏试验(C)和高温破坏试验(D)的HPLC图谱Fig. 2 HPLC chromatograms of destroyed by acid (A), destroyed by alkali (B), destroyed by oxidation (C), and destroyed by heating (D) |
称取依维莫司对照品10 mg,精密称定,置于10 mL量瓶中,用流动相溶解并稀释至刻度,摇匀后作为标准贮备液。分别精密量取储备液0.5、1.0、1.5、2.0、2.5、5.0 mL,置10 mL量瓶中,并用流动相稀释至刻度。进样测定,记录色谱图。以质量浓度为横坐标,峰面积为纵坐标,进行线性拟合,得回归方程为Y=32.123 X+183.27,r=0.999 7,结果表明,依维莫司在63~1 008 μg/mL线性关系良好。
2.5 精密度试验取批号140528依维莫司样品,制备供试品溶液,精密量取20 μL,重复进样6次,结果依维莫司峰面积的RSD值为0.7%。
2.6 稳定性试验取批号140528依维莫司样品适量,制备供试品溶液,于室温(20~25 ℃)下放置,分别于0、2、4、6、8、10 h分别进样测定,记录主峰面积,结果依维莫司峰面积的RSD值为0.52%,说明供试品溶液在10 h内稳定性良好。
2.7 重复性试验取批号140528依维莫司样品6份,制备供试品溶液,分别进样测定,记录峰面积,计算依维莫司的质量分数,结果其RSD值为0.58%。
2.8 回收率试验精密称取批号140528依维莫司样品40 mg,置于100 mL量瓶中,共9份,分别加入依维莫司对照品32.03、39.95、45.77 mg,制备供试品溶液,进样测定,计算回收率,结果平均回收率为100.45%,RSD值为0.64%(n=9)。
2.9 样品测定取依维莫司原料药约10 mg,精密称定,置于10 mL量瓶中,加流动相溶解,并稀释至刻度,摇匀。再精密量取2 mL,置于10 mL量瓶中,加流动相稀释至刻度,摇匀。取上述溶液10 μL进行测定;另精密称取105 ℃干燥至恒定质量的依维莫司对照品适量,同法测定作为对照,按外标法计算依维莫司的质量分数,结果见表 1。
| 表 1 依维莫司原料药中依维莫司的测定结果(n=3)Table 1 Determination of everolimus in everolimus active pharmaceutical ingredient (n=3) |
取依维莫司适量,加流动相稀释至适宜浓度,以流动相为空白样品,在190~400 nm波长进行扫描。结果依维莫司在276 nm处有最大吸收,而空白样品无吸收,故选择276 nm作为检测波长。
3.2 流动相的选择参考同类化合物的检测方法[4],对流动相进行筛选。根据试验结果,确定用乙腈和水为流动相,所得依维莫司峰形较好,且主峰保留时间适宜。
综上所述,本实验建立了利用高效液相色谱法测定依维莫司的方法,方法学研究表明利用该方法测定依维莫司保留时间稳定,方法精密度高,结果准确,是一种较理想的测定方法,为依维莫司质量控制标准的建立提供参考。
| [1] | Motzerr J, Bacik J, Schwartz L H, et al. Prognostic factors for survival in previously treated patients with metastatic renal cell carcinoma [J]. J Clin Oncol, 2004, 22(3): 454-463. |
| [2] | 张 茹, 刘素娟, 秦莉伟. 雷帕霉素靶蛋白抑制剂——依维莫司 [J]. 现代中西医结合杂志, 2010, 9(26): 3399-3401. |
| [3] | 李红杰, 胡 好, 睢大员. 第二代药物涂层支架的研究进展 [J]. 武警医学, 2011, 22(11): 1001-1004. |
| [4] | 仲伟潭, 魏增辉, 常 亮, 等. 发酵液中西罗莫司含量的测定 [J]. 河北化工, 2009, 32(3): 68-70. |
 2015, Vol. 30
2015, Vol. 30

