盐酸伪麻黄碱、马来酸氯苯那敏和氢溴酸右美沙芬均被收录入我国第一批非处方药目录中。盐酸伪麻黄碱为α受体激动剂,可以减轻鼻塞,能够缓解普通感冒和流感引起的鼻部症状,临床资料表明其缓解普通感冒鼻部症状的疗效优于安慰剂。马来酸氯苯那敏为H1受体阻滞剂,能够缓解因抗原抗体反应引起组织胺释放导致的临床症状,如过敏或感冒引起的流涕、眼痒、流泪、打喷嚏等。氢溴酸右美沙芬是一种镇咳药,能直接作用于延髓咳嗽中枢,缓解干咳。由这3种成分组成的美尔伪麻复方制剂主要用于缓解由感冒或过敏引起的上呼吸道症状,如鼻塞、流涕、打喷嚏及咳嗽。目前,国家食品药品监督管理总局已批准美尔伪麻溶液和美敏伪麻咀嚼片上市销售,它们的活性成分均为盐酸伪麻黄碱、马来酸氯苯那敏和氢溴酸右美沙芬,且均为普通释放制剂。美敏伪麻缓释胶囊为含有速释小丸和能在一定时间内发挥作用的缓释小丸,故其有效浓度可维持12 h,减少了服药次数,提高了用药安全性。伪麻黄碱、氯苯那敏和右美沙芬各自单体或与其他药物组成的复方在健康人体内的药动学研究均有报道[1, 2, 3, 4, 5]。本实验研究了美敏伪麻缓释胶囊在健康人群单、多次给药的药动学特征,希望为美敏伪麻缓释胶囊上市以及临床用药提供支持。
1 材料 1.1 仪器LC-MS/MS系统由日本岛津LC-20A液相系统及美国AB公司配备电喷雾离子源的API 4000三重串联四极杆质谱组成。Milli Q纯水机(Millipore,Bedford,MSA),Corning 320 pH计,Mettler AX150型分析天平。
1.2 药品与试剂美敏伪麻缓释胶囊由中美天津史克制药有限公司提供,每粒含盐酸伪麻黄碱90 mg、马来酸氯苯那敏4 mg、氢溴酸右美沙芬30 mg,批号PCM050301。盐酸伪麻黄碱(质量分数为99.8%)、马来酸氯苯那敏(质量分数为99.7%)、氢溴酸右美沙芬(质量分数为95.0%)、酒石酸右啡烷(质量分数>99%)对照品均由中美天津史克制药有限公司提供。内标苯丙醇胺购自Sigma公司。甲醇、乙腈均为HPLC级,由Fisher提供,醋酸乙酯为分析纯,购自北京化学试剂公司,乙酸铵、氢氧化钠购自北京益利精细化学品有限公司,去离子水由Milli Q纯化系统制备。空白血浆由受试者捐献。
2 方法与结果 2.1 试验对象21名健康男性受试者顺利完成本研究,其中年龄为(32.3±2.57)岁,体质量为(59.9±4.90)kg,身高为(1.66±0.05)m,体质量指数为(21.9±1.50)。所有受试者经生命体征、心电图及各项实验室检查无异常或不具有临床意义的异常,无中枢神经系统、心血管系统、肾脏、肝脏、消化道、呼吸系统、代谢及骨骼肌肉系统的明确病史。AIDS和肝炎病毒感染者、药物滥用者、最近3个月内献血或作为受试者被采样者,以及嗜烟、嗜酒者和试验前两周内曾服用过各种药物者均在筛选中排除。本研究通过北京协和医院伦理委员会的批准,试验前受试者均先签署知情同意书。
2.2 给药方法与样本采集22例受试者在第1天单次服用美敏伪麻缓释胶囊1粒,于第1天的服药前(0 h)和服药后0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5、8、8.5、9、9.5、10、10.5、12、13.5、16、24、28、30、34、36、37.5、48、52、58、60、61.5、62、72 h从前臂静脉采血3 mL,用于获取受试者单次给药的药动学信息。在第4~8天口服美敏伪麻缓释胶囊,1粒/次,2次/d,分别于给药前从受试者前臂静脉采血3 mL。在第9天早晨口服1粒美敏伪麻缓释胶囊,于第9天给药前(0 h)和给药后0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5、8、8.5、9、9.5、10、10.5、11、12、13.5、16、24、28、30、34、36 h从前臂静脉采血3 mL,用于获取受试者多次给药达稳时的药动学信息。所有血样在取样30 min内,在4 ℃,4 000 r/min条件下离心分离15 min,离心后的血浆在−20 ℃条件下保存,待测。
受试者于每个周期试验前1天晚上入住I期病房,需禁食10 h以上,试验第1天早上按照试验方案口服美敏伪麻缓释胶囊,200 mL温开水送服,不能咀嚼或碾碎。服药后医生或护士将检查受试者口腔以确保药物咽下。除服药用的温开水外,服药前及服药后2 h内禁止饮水,服药后4、10 h进食标准早餐、午餐和晚餐(统一的低脂清淡饮食)。单次给药时禁食4 h,多次给药时禁食2 h。在试验开始前3 d内和整个试验期间,受试者禁止饮酒。在试验开始前24 h和整个试验期间,受试者禁止饮用含咖啡因的饮料,如咖啡、茶、巧克力、可乐。
2.3 安全性评价整个试验过程由临床医师进行监护,最大限度的保护受试者的安全和权益,并考察试验药物的安全性。在筛选期和试验结束后的随访期抽血血液常规和生化检查,并在给药期间密切注意观察和询问受试者的各种反应,及时记录不良事件的性质、发生频率、处置及转归,并进行相关性分析,同时对试验前后实验室检查结果进行分析。
2.4 血浆中伪麻黄碱、氯苯那敏、右美沙芬及游离右啡烷的检测 2.4.1 色谱条件Waters Symmetry色谱柱(100 mm×4.6 mm,3.5 μm);流动相为乙腈-10 mmol/L乙酸铵(pH 5.5)(80∶20);体积流量1 mL/min;柱温为室温;每个样品分析用时3 min。
2.4.2 质谱条件离子源采用电喷雾离子源(ESI),源喷射电压为4 000 V;离子源气体1(N2)压力为50 Unit;离子源气体2(N2)压力为80 Unit;气帘气体(N2)压力为12 Unit;源温度:450 ℃;正离子多反应监测(MRM)模式检测。伪麻黄碱:监测离子m/z 166.3→133.2,去簇电压为35 V,碰撞能量为30 eV;氯苯那敏:监测离子m/z 275.2→230.2,去簇电压为45 V,碰撞能量为23 eV;右美沙芬:监测离子m/z 272.2→230.2,去簇电压为85 V,碰撞能量为50 eV;右啡烷:监测离子m/z 258.2→157.1,去簇电压为106 V,碰撞能量为54 eV。内标苯丙醇胺:监测离子m/z 152.2→134.1,去簇电压为40 V,碰撞能量为15 eV。
2.4.3 样品处理取0.3 mL血浆样品,与内标(100 ng/mL苯丙醇胺)50 μL和1 mol/L NaOH 50 μL先后混匀,加入醋酸乙酯0.9 mL,混匀后13 000 r/min离心10 min,取上清液约0.8 mL在40 ℃使用N2吹干,使用500 μL流动相乙腈-10 mmol/L乙酸铵(pH 5.5)(80∶20)复溶,备用。
2.4.4 特异性试验在上述检测条件下,伪麻黄碱、氯苯那敏、右美沙芬、右啡烷和内标的保留时间分别约为1.6、1.4、1.6、2.0、1.3 min,空白血浆、空白血浆加入内标和最低定量限的血浆样本的色谱图见图 1。可见4个化合物峰形良好,不受内源性干扰,并且检测灵敏度满足分析要求。
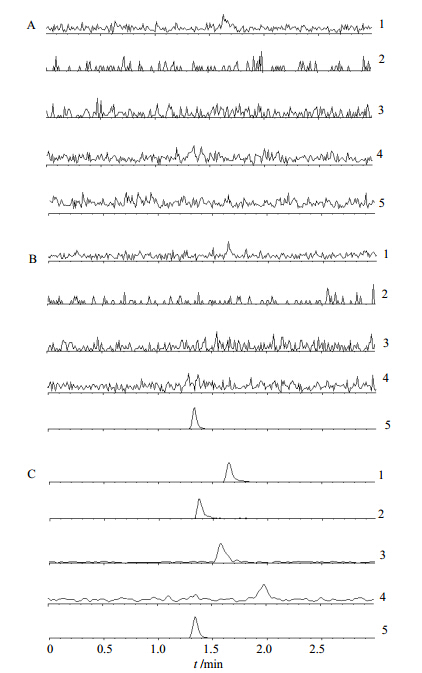 |
1-伪麻黄碱 2-氯苯那敏 3-右美沙芬 4-右啡烷 5-内标苯丙醇胺 1-pseudoephedrine 2-chlorpheniramine 3-dextrorphan 4-dextromethorphan 5-internal standard phenylpropanolamine图 1 各成分在人空白血浆(A)、加入内标(100 ng/mL)的人空白血浆(B)以及在LLOQ水平的人血浆样品(C)的色谱图Fig. 1 MRM chromatography of components in human blank plasma (A), human blank plasma added with 100 ng/mL internal standard (B), and human plasma at LLOQ level (C) |
以伪麻黄碱、氯苯那敏、右美沙芬、右啡烷与内标的峰面积之比为纵坐标,质量浓度为横坐标,进行曲线拟合,得回归方程。结果表明伪麻黄碱、氯苯那敏、右美沙芬、右啡烷分别在5.0~1 000、0.25~50、0.025~5、0.025~5 µg/L血浆浓度范围内线性关系良好。
2.4.6 LLOQ、日内、日间精密度和准确度从低至高3种不同质量浓度的质控样品,分别处理并测定5个,连续3批(在不同天分别制备与测定),计算日内精密度、日间精密度和准确度。同时制备一批LLOQ样本(重复5个)。由表 1可知,4个化合物的日内、日间精密度均小于15%,日内、日间准确度均在±15%以内,LLOQ的日内精密度均小于20%,日内准确度在20%以内,证明本法的LLOQ及日内、日间精密度和准确度符合要求。
| 表 1 精密度试验和准确度试验结果Table 1 Results of intra-and inter-day precision and accuracy test |
考察了样本反复冻融3次以及−20 ℃下储备液储存5个月、处理液进样器(室温)内放置24 h、样本室温放置12 h条件下的稳定性,考察3个质量浓度水平,每个浓度水平在不同实验中重复5次,结果见表 2。可知在上述各种条件下,样品稳定性良好。
| 表 2 稳定性试验结果Table 2 Results of stability test |
在3个质量浓度水平(每个质量浓度水平重复5次)上考察了伪麻黄碱、氯苯那敏、右美沙芬、右啡烷经本法制备后的回收率,见表 3。结果显示4个化合物的回收率在3个质量浓度水平间一致。
| 表 3 回收率试验结果Table 3 Results of recovery test |
22例受试者中有21例按照方案要求完成了全部试验样品采集及随访观察,另有1例受试者中途发生轻度腹泻,医生进行诊治后恢复,经医生判断与药物无关,并退出试验。另有1例受试者报告轻度转氨酶升高,为一过性,经医生判断可能与药物相关,未采取医学措施。无严重不良事件报告。
2.6 药时曲线及药动学参数使用Excel软件(2013)绘制血浆中伪麻黄碱、氯苯那敏、右美沙芬、右啡烷质量浓度随时间变化的曲线(图 4)。连续给药4 d、2次/d后,伪麻黄碱、氯苯那敏、右美沙芬、右啡烷在第7、8、9天的谷浓度无明显改变趋势,说明均达到稳态。
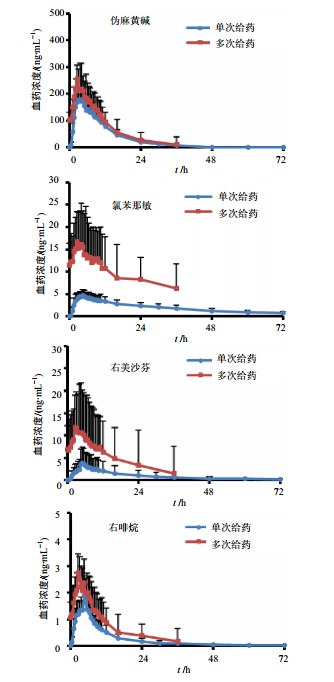 | 图 4 美敏伪麻缓释胶囊单、多次给药后平均药时曲线Fig. 4 Average concentration - time curves of Controlled-release Capsule Dextromethorphan Chlorpheniramine Pseudoephedrine after single and multiple doses |
使用WinNonlin软件NCA模块计算所得的单次、多次给药后伪麻黄碱、氯苯那敏、右美沙芬、右啡烷的平均药动学参数,见表 4。
| 表 4 单次和多次给药后伪麻黄碱、氯苯那敏、右美沙芬和右啡烷的药动学参数Table 4 Pharmacokinetic parameters of pseudoephedrine, chlorpheniramine, dextrorphan, and dextromethorphan in healthy subjects of Controlled-release Capsule Dextromethorphan Chlorpheniramine Pseudoephedrine after single and multiple doses |
美敏伪麻缓释胶囊单次给药后,伪麻黄碱、氯苯那敏、右美沙芬、右啡烷的AUClast与AUCinf比较接近,说明基本采样到消除相,与消除相相关的药动学参数可靠。缓释制剂给药后,4个化合物达峰时间平均值均在2 h以上,证明具有缓释效果。多剂量给药后,以AUC0-12 h计算的蓄积因子显示,伪麻黄碱、氯苯那敏、右美沙芬、右啡烷均有一定蓄积。通过比较单次给药后的AUCinf和稳态时的AUCtau, ss可知化合物的清除是否呈现时间依赖。伪麻黄碱、氯苯那敏和右啡烷的这两个参数都比较接近,右美沙芬的均值虽有升高,但其变异太大,因此经过t检验后也无明显差异,提示4个化合物的清除率均无时间相关性。
3 讨论本实验采用LC-MS/MS法测定血浆中伪麻黄碱、氯苯那敏、右美沙芬和右啡烷的药物浓度,该方法方便、灵敏、快速,便于大规模的生物样本分析,适用于人体药动学的研究。
从安全性结果来看,只有1例受试者出现与药物相关的不良事件,并且为轻度和一过性,无需进行治疗,结果显示美敏伪麻缓释胶囊单、多次给药后安全性良好。
文献报道盐酸伪麻黄碱半衰期为6~8 h[5],与本实验结果一致。非索伪麻缓释片(含120 mg伪麻黄碱)中伪麻黄碱的tmax、AUC、Cmax单、多次给药后分别为5.62~6.00 h、2 722~3 056 μg·h/L、186~194 ng/mL[5],与本实验结果一致。马来酸氯苯那敏平均半衰期为18~20 h[2],与本实验结果一致。混悬液口服后,氯苯那敏的tmax在1.4~2.2 h[3],与美敏伪麻缓释胶囊相比较短,提示美敏伪麻缓释胶囊具有缓释效果。
氢溴酸右美沙芬口服后吸收迅速,但在组织代谢前,经肝广泛代谢,血中的原形药浓度很低[6]。氢溴酸右美沙芬经O-脱甲基化成为其主要代谢产物右啡烷,其浓度较高,并且也有镇咳作用[6],因此本研究也同时检测了右啡烷。速释氢溴酸右美沙芬口服后,氢溴酸右美沙芬血药浓度达峰时间约为2~3 h[6],半衰期为3~4 h[7, 8],右啡烷血药浓度达峰时间为1~2 h,半衰期为2~4 h[6, 7, 8],与本实验结果一致。氢溴酸右美沙芬的代谢在肝脏受细胞色素P450酶、P4502D6的催化。这种酶存在基因多态性,相对于大多数人(被称为广泛代谢型),有7%~10%的白人(被称为缺乏代谢型)此酶功能缺陷[9]。文献报道,有0.95%的东方人在右美沙芬的代谢方面表现为缺乏代谢型(n=420),这与整个代谢基因多态性的发生几率是一致的(1.00%,n=3 003)。同时,这个发生率表明,缺乏代谢基因型在东方人中是罕见的[10]。本研究纳入的受试者中无缺乏代谢型报道。
综上所述,美敏伪麻缓释胶囊单、多次给药后伪麻黄碱、氯苯那敏、右美沙芬和右啡烷的吸收具有缓释特征。
| [1] | 刘 丹, 陈笑艳, 张逸凡, 等. 人血浆中O-去甲右美沙芬的测定及药代动力学研究 [J]. 药学学报, 2004, 39(6): 449-452. |
| [2] | 汤文艳, 郑 恒, 代宗顺, 等. 氨麻美敏分散片的人体相对生物利用度和生物等效性 [J]. 中国医院药学杂志, 2008, 28(17): 1469-1473. |
| [3] | 宋 敏, 谭鸿毅, 谭志荣, 等. 单剂量和多剂量口服布洛伪麻那敏干混悬剂在健康人体的药代动力学 [J]. 中国临床药理学杂志, 2010, 26(1): 28-32. |
| [4] | 卢俊钢, 吴春艳, 孙慧婧, 等. 健康受试者口服酚麻美敏片后氢溴酸右美沙芬及其代谢物的人体药动学研究 [J]. 药物分析杂志, 2011, 31(9): 1619-1625. |
| [5] | 邱 枫, 何晓静, 孙亚欣, 等. 非索伪麻缓释片在健康人体中的药代动力学 [J]. 中国临床药理学杂志, 2013, 29(2): 129-132. |
| [6] | Gorski J C, Jones D R, Wrighton S A, et al. Characterization of dextromethorphan N-demethylation by human liver microsomes. Contribution of the cytochrome P450 3A (CYP3A) subfamily [J]. Biochem Pharmacol, 1994, 48(1): 173-182. |
| [7] | Silvasti M, Karttunen P, Tukiainen H, et al. Pharmacokinetics of dextromethorphan and dextrorphan: a single dose comparison of three preparations in human volunteers [J]. Int J Clin Pharmacol Ther Toxicol, 1987, 25(9): 493-497. |
| [8] | Silvasti M, Karttunen P, Happonen P, et al. Pharmacokinetic comparison of a dextromethorphan-salbutamol combination tablet and a plain dextromethorphan tablet [J]. Int J Clin Pharmacol Ther Toxicol, 1990, 28(6): 268-272. |
| [9] | Kroemer H K, Eichelbaum M. "It's the genes, stupid". Molecular bases and clinical consequences of genetic cytochrome P450 2D6 polymorphism [J]. Life Sci, 1995, 56(26): 2285-2298. |
| [10] | Vogel F, Motulsky A G. Human Genetics. Problem and Approaches [M]. 2nd Ed. Berlin: Springer-Verlag, 1979. |
 2015, Vol. 30
2015, Vol. 30


