2. 江西中医药大学 科技学院, 江西 南昌 330025
2. College of Science and Technology, Jiangxi University of Traditional Chinese Medicine, Nanchang 330025, China
阿糖胞苷是作用于细胞S增殖期的嘧啶类抗代谢药物,通过抑制细胞DNA的合成,干扰细胞的增殖,临床上主要用于急性白血病的治疗[1, 2, 3]。阿糖胞苷在体内极易被胞苷脱氨酶脱氨,转化成无活性的阿糖尿苷[4, 5]。研究阿糖尿苷的药动学能够很好地理解阿糖胞苷在体内的代谢情况,为开发更好的阿糖胞苷剂型提供依据。本实验建立了LC-MS/MS法测定血浆中的阿糖尿苷,并将其应用于大鼠尾静脉注射阿糖胞苷后阿糖尿苷的药动学研究。
1 仪器与材料Waters ACQUITY TQD system超高效液相串联质谱仪(美国Waters公司)。
SD大鼠,雄性,体质量(250±20)g,购自沈阳药科大学实验动物中心,合格证号SCXK(辽)2014-0002。
阿糖尿苷对照品(质量分数99.5%,河南省新乡医药化工有限公司,批号2012106X),异烟肼对照品(质量分数大于99.5%,中国食品药品检定研究院,批号100578-200902)。注射用盐酸阿糖胞苷(规格100 mg,海正辉瑞制药有限公司,批号20130116),甲醇、乙腈(色谱级,美国Fisher公司),甲酸(色谱纯,天津康科德科技有限公司)。四氢尿苷(美国Calbiochem公司)。
2 方法和结果 2.1溶液的配制 2.1.1对照品溶液的配制精密称定阿糖尿苷10.0 mg,置100 mL量瓶中,加水溶解并稀释至刻度,摇匀,即得100.0 μg/mL储备液。精密量取储备液适量,分别用水逐级稀释成1.0、2.0、5.0、10.0、50.0、100.0、500.0、1 000.0 ng/mL阿糖尿苷溶液,置于冰箱−20 ℃保存。
2.1.2 内标溶液的配制精密称定异烟肼10 mg,置100 mL量瓶中,加水溶解并稀释至刻度,作为内标储备液。精密量取该储备液0.4 mL,置100 mL量瓶中,加水溶解并稀释至刻度,即得400.0 ng/mL内标溶液,置于冰箱−20 ℃保存。
2.2 血浆样品的处理方法取血浆30 μL,加入400.0 ng/mL内标异烟肼溶液30 μL和蒸馏水30 μL,然后加入乙腈200 μL,涡流混合2 min,15 000 r/min离心10 min,取上清液,即得。
2.3 测定条件 2.3.1 液相条件ACQUITY UPLC BEH C18色谱柱(50 mm×2.1 mm,1.7 μm);流动相:水(A)-乙腈(B),梯度洗脱:0 min(90% A),1.5 min(90% A),3.0 min(70% A),3.5 min(100% A),5.0 min(100% A);体积流量:0.2 mL/min;柱温:40 ℃;进样量:5 μL。
2.3.2 质谱条件离子源:ESI源;扫描方式:多反应监测(MRM)方式,扫描时间为0.1 s;毛细管电压:2.5 kV;锥孔电压:26 V;离子源温度:110 ℃;去溶剂气(N2)温度:350 ℃;去溶剂气(N2)流量:500 L/h;锥孔气流量:50 L/h。
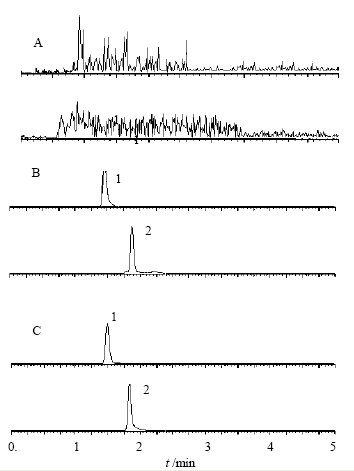
2.4 专属性试验分别取6只大鼠的空白血浆30 μL,除不加内标外(补加60 μL水),其余按照“血浆样品的处理方法”操作,进行LC-MS/MS分析,得空白血浆色谱图。将1.0 ng/mL阿糖尿苷和内标加入空白血浆中,按照“血浆样品的处理方法”操作,得色谱图。取大鼠给药后3 h的血浆30 μL,按照“血浆样品的处理方法”操作,得色谱图。由图 1可知,空白血浆中内源性物质不干扰阿糖尿苷和内标的测定。
|
1-阿糖尿苷 2-异烟肼 1-uridine 2-isoniazid 图 1 空白大鼠血浆(A)、加阿糖尿苷和内标异烟肼的大鼠血浆(B)以及大鼠给药射用盐酸阿糖胞苷血浆样品(C)的MRM图 Fig. 1 MRM chromatograms of blank rat plasma(A),blank plasma spiked with uridine and internal standard isoniazid (B),and rat plasma sample administered with Cytarabine Hydrochloride for injection (C) |
2.5 标准曲线的制备
精密量取空白大鼠血浆30 μL,共8份,分别置5.0 mL具塞玻璃管中,分别加入阿糖尿苷系列对照品溶液(相应血浆药物质量浓度1.0、2.0、5.0、10.0、50.0、100.0、500.0、1 000.0 ng/mL)30 μL,按照“血浆样品的处理方法”操作,每1个浓度进行双样本分析,记录色谱图,连续记录3 d。以待测物浓度为横坐标,待测物与内标物的峰面积比值为纵坐标,采用加权最小二乘法进行回归运算。得回归方程Y=0.503 X+8.045,r=0.990 8,线性范围为1.0~1 000 ng/mL。标准曲线的下限即阿糖尿苷的最低定量限(lower limit of quantification,LLOQ),是1.0 ng/mL。
2.6 精密度和准确度试验取空白血浆30 μL,将30 μL水换成相应体积的样品,其余按照“血浆样品的处理方法”操作,6个样品平行分析,每天测定1次,连续测定3 d,并与标准曲线的回归方程同时进行,测定样品的浓度。用计算RSD值。以测得值与真实值的比值计算准确度,结果见表 1。精密度试验的RSD值在−15%~15%,准确度试验的RSD值在±15%,符合测定的要求。
| 表 1 精密度和准确度试验结果 Table 1 Results of precision and accuracy test |
2.7 提取回收率试验
取空白血浆30 μL,将30 μL水换成相应体积的样品,其余按照“血浆样品的处理方法”操作,制备低、高浓度(2.0、800 ng/mL)的血浆样品,测得峰面积为A1;另取空白血浆30 μL,按照“血浆样品的处理方法”操作,残留物用含阿糖尿苷的样品溶液溶解,制成阿糖尿苷浓度分别是2.0、800.0 ng/mL样品溶液,进样分析,测得峰面积为A2。以每个浓度正常提取样品所得的峰面积(A1)与未提取样品峰面积(A2)均值的比值计算提取回收率。内标按照同样的方法测定回收率。阿糖尿苷和内标的提取回收率分别是95.2%、91.0%,86.4%。
2.8 基质效应试验分别取含阿糖尿苷低、高浓度(2、800 ng/mL)的血浆样品,进样分析,记录峰面积A3。取空白血浆30 μL,按照“血浆样品的处理方法”操作,残留物用含阿糖尿苷的样品溶液溶解,制成阿糖尿苷质量浓度分别是2.0、800.0 ng/mL的样品溶液,进样分析,测得峰面积为(A2)。以同一质量浓度血浆基质样品的峰面积(A2)与无基质样品的峰面积(A3)的比值计算基质效应。结果阿糖尿苷的平均基质效应是97.3%。
2.9 稳定性试验分别考察处理后的血浆样品4 ℃放置24 h的稳定性,血浆样品在3个冻融循环(−40~22 ℃),以及长期稳定性(−40 ℃放置30 d)和室温(23 ℃)放置2 h的稳定性,结果见表 2。表明,样品在上述条件下是稳定的。
| 表 2大鼠血浆中阿糖尿苷在不同条件下的稳定性 Table 2 Stability data of uridine in rat plasma under different conditions |
2.10 药动学参数的测定
取SD大鼠6只,实验前禁食过夜,尾iv注射用盐酸阿糖胞苷,剂量以阿糖胞苷计为3 mg/kg,于给药前和给药后5、15、30、45 min以及1、1.5、2、3、4、6、8、12、24 h经眼眶采血200 μL,同时加入胞苷脱氨酶抑制剂四氢尿苷溶液10 μL(在血液中浓度约为0.1 mmol/L),放置在涂有肝素的离心管中,4 000 r/min离心10 min,取血浆,置−40 ℃冰箱中待测。
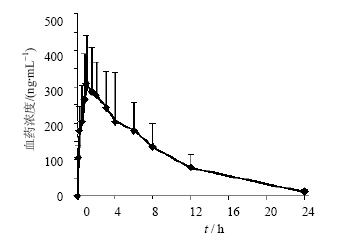
按照“血浆样品的处理方法”同时制备阿糖尿苷低、中、高3个质量浓度的样品,每个质量浓度进行双样本分析。以当日的标准曲线回归方程计算样品及各时间点样品中阿糖尿苷的质量浓度,样品测定结果的准确度在±15%。血药质量浓度-时间曲线见图 2。
|
图 2 大鼠给药射用盐酸阿糖胞苷后阿糖尿苷的血药浓度-时间曲线 Fig. 2 Mean plasma concentration - time curve of cytarabine inrats administered with Cytarabine Hydrochloride for injection |
可以看出,注射用盐酸阿糖胞苷尾静脉注射后,在体内很快的产生阿糖尿苷,5 min就能测到阿糖尿苷的存在,因此,临床上开发的剂型要避免阿糖胞苷在体内的快速代谢。从阿糖尿苷的趋势可以看出,阿糖尿苷的浓度随着阿糖胞苷的注射,逐渐升高,1 h后达到峰值。
大鼠体内的阿糖尿苷最大血药浓度(Cmax)和达峰时间(tmax)直接由实测值读出。由血药浓度-时间曲线末四点做半对数图,以lgC-t按最小二乘法进行线性回归,所得斜率的绝对值即为消除速率常数(ke);消除半衰期(t1/2)为ln2/ke。药时曲线下面积(AUC0-∞)由梯形法求得。药动学参数如下:tmax为1.0 h,Cmax为134.2 ng/mL,AUC0-t为2 316.0 ng·h/mL,t1/2为4.3 h。
3 讨论阿糖胞苷是治疗急性白血病的主要药物,临床上主要以鞘内注射的方式给药,但是阿糖胞苷在体内极易被胞苷脱氨酶脱氨,转化为无活性的阿糖尿苷。在实际的临床治疗中,对于使用阿糖胞苷常规剂量治疗的患者,如果出现诱导失败或复发的情况,会采用高剂量的阿糖胞苷来治疗,这种治疗方案的原理是高剂量的阿糖胞苷会在体内产生高浓度的阿糖尿苷,高浓度的阿糖尿苷会延长细胞的S周期和提高脱氧胞苷激酶的活性,进而提高阿糖胞苷的细胞活性[6]。因此,测定阿糖尿苷的浓度可以为临床上设计合理的阿糖胞苷给药方案提供依据。另外,通过代谢产物阿糖尿苷浓度趋势的了解,可以为开发阿糖胞苷的长效制剂提供指导。
| [1] | 吕冬梅, 王涛, 邱述玲, 等. RP-HPLC法测定小鼠各组织中阿糖胞苷及阿糖尿苷浓度 [J]. 中国药房, 2010, 10(29): 2720-2722. |
| [2] | 周敏, 汤静燕, 薛惠良, 等. 阿糖胞苷血浆浓度监测对小儿白血病化疗反应和预后的影响 [J]. 中国小儿血液和肿瘤杂志, 2008, 13(6): 258-260. |
| [3] | Scott-Moncrieff J C R, Chan T C K, Samuels M L, et al. Plasma and cerebrospinal fluid pharmacokinetics of cytosine arabinoside in dogs [J]. Cancer Chem Pharmacol, 1991, 29(1): 13-18. |
| [4] | Phuphanich S, Maria B, Braeckman R, et al. A pharmacokinetic study of intra-CSF administered encapsulated cytarabine (DepoCyt) for the treatment of neoplastic meningitis in patients with leukemia, lymphoma, or solid tumors as part of a phase III study [J]. J Neurooncol, 2007, 81(1): 201-208. |
| [5] | Zimmerman C L. The disposition of cytosine arabinoside and its metabolite after single doses to rabbits [J]. Biopharm Drug Dispos, 1990, 11(1): 121-129. |
| [6] | Wan S H, Huffman D H, Azarnoff D L, et al. Pharmacokinetics of 1-β-D-arabinofuranosylcytosine in human [J]. Cancer Res, 1974, 34(2): 392-397. |
 2014, Vol. 29
2014, Vol. 29

