2. 延边大学 药学院, 吉林 延吉 133002;
3. 沈阳药科大学 中药学院 基于靶点的药物设计与研究教育部重点实验室, 辽宁 沈阳 110016
2. College of Pharmacy, Yanbian University, Yanji 133002, China;
3. Key Laboratory of Structure-Based Drug Design & Discovery, Ministry of Education, School of Traditional Chinese Materia Medica, Shenyang Pharmaceutical University, Shenyang 110016, China
杭白菊为菊科植物菊Chrysanthemum morifolium Ramat.的干燥头状花序,亦名小汤黄、小白菊,与毫菊、滁菊、贡菊并称为中国驰名的四大名菊。第一次在其花朵尚未完全张开时收摘所得为胎菊,亦名甘菊[1];在其花朵盛开后采摘所得为市售杭白菊。杭白菊性微寒,味苦、甘,归肺、肝经,具有散风清热、平肝明目、清热解毒之功效,用于风热感冒、头痛眩晕、目赤肿痛、眼目昏花、疮痈肿毒[1]。《神农本草经》中记载,杭白菊茶能“主诸风头眩、肿痛、目欲脱、皮肤死肌、恶风湿痹,久服利气,轻身耐劳延年”。杭白菊主产于浙江桐乡,是卫生部首批批准的药食同源的道地药材之一,也是浙江省传统中药材“浙八味”之一,对其化学成分及药理活性的研究具有重要的价值,本文对近年来国内外报道的杭白菊的化学成分和药理活性进行总结归纳。
1 化学成分研究发现杭白菊的化学成分主要包括黄酮类、挥发油、三萜类、甾体类、酚类、多糖及微量元素等,药效物质基础主要为黄酮类、挥发油类成分。
1.1 黄酮类杭白菊中富含黄酮类化合物,其干品含总黄酮高达4.50%,其提取物中含总黄酮高达78.46%。杭白菊中黄酮类化合物的结构母核主要包括黄酮类(A)、黄酮醇类(B)、二氢黄酮类(C),是其主要的活性组分之一。杭白菊中分离鉴定的黄酮类化合物(1~46)见图 1和表 1。
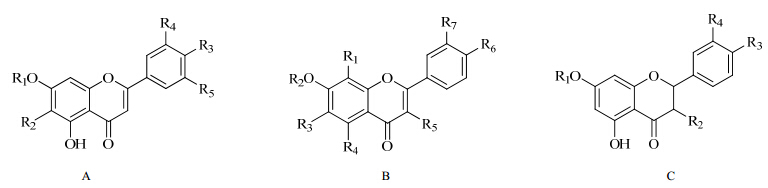 | 图 1 杭白菊中黄酮类化合物的结构Fig. 1 Structures of flavonoid compounds in Chrysanthemi Flos |
| 表 1 杭白菊中的黄酮类化合物 Table 1 Flavonoid compounds in Chrysanthemi Flos |
杭白菊挥发油具有特殊浓郁的芳香气味,研究者采用水蒸气蒸馏法从杭白菊中提取挥发油,利用GC/MS技术对杭白菊挥发油进行了分离、分析与鉴定,从中检出125个峰,目前鉴定出59种化合物,主要为单萜、倍半萜及其含氧衍生物,占挥发油总量的61.74%[23]。从分析结果来看,质量分数较高的成分有α-姜黄烯(8.99%)、石竹烯(7.86%)、β-马榄烯(4.59%)、香木兰烯(4.14%)、2-甲基-1-戊烯(3.36%)、龙脑(1.54%)、樟脑(1.40%)、乙酸龙脑酯(1.21%)等[23, 24]。
1.3 三萜及甾体类目前从杭白菊中分离得到的三萜及甾体类化合物共6个,分别为棕榈酸16β,28-二羟基羽扇醇酯(47)、棕榈酸16β-羟基假蒲公英甾醇酯(48)、棕榈酸16β,22α-二羟基假蒲公英甾醇酯(49)、假蒲公英甾醇(50)、蒲公英甾醇(51)、β-谷甾醇(52)[7]。杭白菊中三萜及甾体类化合物的结构式见图 2。
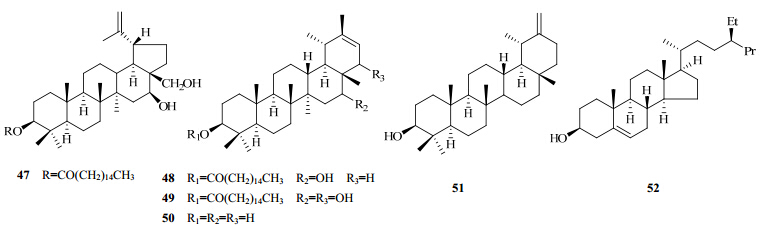 | 图 2 杭白菊中三萜及甾体类化合物的结构Fig. 2 Structures of triterpenes and sterols inChrysanthemi Flos |
杭白菊中广泛存在酚酸类成分,其中主要为C6-C3结构的苯丙酸类[5-6, 25-27],主要有灰毡毛忍冬素F(53)、绿原酸(54)、4-O-咖啡酰奎尼酸(55)、3,4-O-二咖啡酰奎尼酸(56)、4,5-O-二咖啡酰奎尼酸(57)、3,5-O-二咖啡酰奎尼酸(58)、1,3-O-二咖啡酰奎尼酸(59)、咖啡酸(60)、阿魏酸(61)、3,4-二羟基苯基丙酮(62),主要结构见图 3。
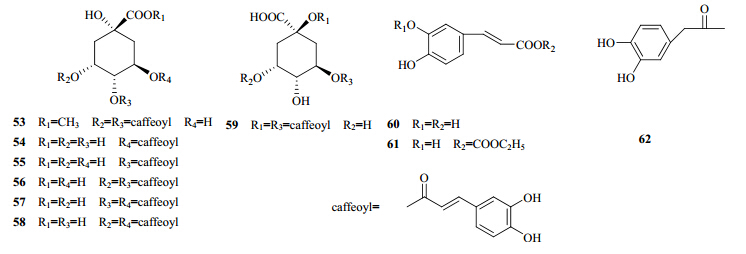 | 图 3 杭白菊中酚类化合物的结构Fig. 3 Structures of phenols in Chrysanthemi Flos |
杭白菊中还含有多糖成分与微量元素。胡立宏等[22]首次杭白菊中分离得到正戊基呋喃果糖苷,Liang等[28]从杭白菊中得到纯多糖P2;近年来对杭白菊微量元素的研究主要集中在微量元素的种类、含量、测定等方面,揭新明等[29]、沈颖旎等[30]报道杭白菊中富含Fe、Zn、Mn、Se、Cu,尤其是Zn、Mn、Se的量很高,也含有As、Cr、V、Sc、Co、Ni、Pb、Sr、Ba等。除上述成分外,杭白菊中还含有鞣质类化合物[31]、脂肪酸[32]、氨基酸[33]、叶黄素[34]、无机元素[34]等。鞣质类化合物有鞣花酸;脂肪酸主要有棕搁酸、亚油酸、亚麻酸。
2 药理作用按杭州本地的传统习惯,杭白菊有“黄菊入药,白菊入茶”之说,其具有疏散风热、平肝明目、清热解毒之功效。关于杭白菊的现代药理学实验主要集中于心血管保护、降血脂、抗氧化等方面的研究,其肝保护、神经保护作用是近年来的新发现。
2.1 心血管保护作用研究发现,杭白菊提取物具有显著的舒血管作用,并呈浓度相关性增加,其机制既与NO介导的途径有关,也与抑制电压依从性钙通道和受体操纵性钙通道以及激活ATP敏感钾通道有关[35, 36, 37, 38, 39, 40]。张玮等[38]和蒋惠娣等[41]报道,杭白菊提取物具有降低大鼠心室易颤性、抗心率失常的作用,能显著抵抗乌头碱和氯仿诱发的大鼠心率失常及氯仿诱发的小鼠心率失常。此外,杭白菊提取物对离体心脏和单个心肌细胞均显示出正性肌力作用,它对整体动物心脏是否也有正性肌力作用的研究正在进行中[42, 43],这种作用可能与杭白菊中含有的酚类成分有关。
2.2 降血脂、降血压、降血糖作用方雪玲等[44]报道,杭白菊提取物在大鼠高脂膳食情况下具有抑制血胆固醇和三酰甘油升高的作用,在大鼠正常的基础饲食情况下对血清胆固醇的升高有明显改善作用,这对预防和治疗高血脂疾病是有益的。有学者[45]通过对大鼠静脉注射杭白菊总黄酮,结果发现在给药后40~80 min时血压明显下降,说明其降压作用的有效成分为总黄酮类物质。陈少华等[46]实验研究发现杭白菊具有降糖功效,研制出了以杭白菊为主要成分的治疗糖尿病的药物“降糖康”,用药后糖尿病患者空腹及餐后血糖、糖化血红蛋白显著好转,血液黏度和血三酰甘油也随之降低,认为这种降血糖作用与其中含有的微量元素Cr有关,Wang等[19]认为杭白菊的这种降血糖作用与其含有的黄酮苷、咖啡酰奎尼酸有关。
2.3 抗氧化作用Lii等[47]研究发现,杭白菊提取物能提高体外培养小牛血管平滑肌细胞(VSMC)上清液中超氧化物歧化酶(SOD)活力、减少丙二醛(MDA)的生成,具有较强的抗氧化能力,且呈浓度相关性。秦卫东[48]研究发现,黄酮类与酚类是杭白菊的主要抗氧化成分,并且其抗氧化活性强弱与提取溶剂有关,其中,杭白菊的乙醇提取物抗氧化活性最强,另外,酵母细胞壁多糖处理可以提高杭白菊的抗氧化活性[20]。
2.4 抗癌作用有研究报道杭白菊提取物中木樨草素[49]与香叶木素[5]对人结肠癌细胞有显著的细胞毒性。另外,杭白菊挥发油部分的β-榄香烯具有显著的抗癌活性,“榄香烯乳注射液”是我国自主研发成功的二类抗肿瘤新药,目前已用于癌症病人的临床治疗[23]。
2.5 神经保护作用Kim等[50]和林琳等[51]报道了杭白菊的神经保护作用,实验结果显示,杭白菊提取物能通过抑制MPP+诱导的细胞毒性、氧化损伤、PARP蛋白水解与Bcl-2、Bax的表达,改善神经母细胞瘤系SH-SY5Y的细胞活力,这种较强的神经保护作用可能与杭白菊中含有的木樨草素、芹菜素、二咖啡酰奎尼酸、三萜类化合物有关,可作为治疗退行性神经疾病的潜在药物。
2.6 肝保护作用杭白菊的保肝作用是近年来的一个新发现。康文艺等[53]报道,杭白菊乙醇提取物和多糖部分对CCl4诱导的小鼠肝损伤有一定的保护作用,其通过对抗自由基与抑制脂质过氧化特异性地降低血清丙氨酸氨基转移酶(ALT)、门冬氨酸氨基转移酶(AST)的量,提高肝组织SOD活性。Wang等[54]研究证实杭白菊提取物能诱导大鼠肝微粒体中CYP1A1、CYP1A2和CYP2B1的活性表达,具有保肝功能。
2.7 其他李英霞等[54]报道,杭白菊中的挥发油成分在体外对金黄色葡萄球菌、白色葡萄球菌、变形杆菌、乙型溶血性链球菌、肺炎双球菌均有一定程度的抑制作用。其中,对金黄色葡萄球菌的抑制效果最为明显。Hu等[55]、张璐等[56]发现杭白菊中的金合欢素-7-O-β-D半乳糖苷是抗病毒的新活性成分,且毒性很低。另外,有报道杭白菊挥发油对新西兰兔体温升高有显著的降低作用且呈剂量相关性[57]。Lee等[12]最新研究发现,杭白菊中的香叶木素能抑制SCF/UVB诱导的色素沉着和c-Kit信号通路磷酸化,可能成为黑色素沉着症的潜在治疗药物。
3 结语杭白菊是我国传统的中药材,富含多种生物活性物质,具有较高的药食两用价值。目前,对杭白菊的研究主要集中在黄酮类、挥发油等成分的提取和分析,其他成分只局限在量的测定上,虽然近年来对其药用的研究逐渐增多,但对其中含有的单体活性成分的药理作用的研究还不是很明确。黄酮类化合物是杭白菊主要活性成分之一[58],在预防和治疗冠心病、糖尿病及抗癌方面具有重要地位,因此,有望从该类植物中找到抑制癌症的黄酮类先导化合物,这对于研发抗癌新药意义重大。另外杭白菊的保肝作用和神经保护作用是近年来的新发现,如对其药理活性、作用机制等进行深入研究,不仅可以研制出新的生理功能性食品,还对其应用于临床具有重要的价值。加强上述有关方面的研究,将为更好的开发利用这一资源奠定良好的基础。
| [1] | 中国药典[S]. 一部. 2010: 292. |
| [2] | 邹文韬. 杭白菊中黄酮类化合物的研究[D]. 杭州: 浙江理工大学, 2009: 1-54. |
| [3] | 邹文韬, 张因皎, 俞菊红, 等. 杭白菊中黄酮类化合物的分离与鉴定[J]. 浙江理工大学学报, 2010, 27(1): 140-144. |
| [4] | Wang S, Hao L J, Zhu J J, et al. Study on the effects of sulfur fumigation on chemical constituents an antioxidant activity of Chrysanthemum morifolium cv. Hang-ju[J]. Phytomedicine, 2014, 21(5): 773-779. |
| [5] | Xie Y Y, Yuan D, Yang J Y, et al. Cytotoxic activity of flavonoids from the flowers of Chrysanthemum morifolium on human colon cancer Colon 205 cells[J]. J Asian Nat Prod Res, 2009, 11(9): 771-778. |
| [6] | Lin L Z, Harnly J M. Identication of the phenolic components of chrysanthemum ower (Chrysanthemum morifolium Ramat)[J]. Food Chem, 2010, 120: 319-326. |
| [7] | 胡立宏, 陈仲良. 杭白菊的化学成分研究: 两个新三萜酯的结构测定[J]. 植物学报, 1997, 39(1): 85-90. |
| [8] | 胡碧波, 吴祖帅, 蔡君, 等. 杭白菊中主要黄酮苷的测定及影响因素考察[J]. 中国中药杂志, 2006, 31(21): 1772-1775. |
| [9] | 彭钰芳, 邹文韬, 许传莲. 杭白菊中黄酮类化合物及其抑制人源肿瘤细胞增殖活性的研究[J]. 中国药学杂志, 2010, 45(19): 1454-1459. |
| [10] | 蒋惠娣. 中药杭白菊心血管系统作用及活性成分研究[D]. 杭州: 浙江大学, 2004: 1-131. |
| [11] | Lee S J, Jung T H, Kim H, et al. Inhibition of c-Kit signaling by diosmetin isolated from Chrysanthemum morifolium[J]. Arch Pharm Res, 2014, 37(2): 175-185. |
| [12] | Wang Y J, Yang X W, Guo Q S, et al. Optimization of the extraction conditions and simultaneous quantification of six flavonoid glycosides in Flos Chrysanthemi by RP-LC[J]. Chromatographia, 2009, 70: 109-116. |
| [13] | Chen Z, Tu M, Sun S, et a1. The exposure of luteolin is much lower than that of apigen in in oral administration of Flos Chrysanthemi extract to rats[J]. Drug Metab Pharmacokinet, 2012, 27(1): 162-168. |
| [14] | Lee J S, Kim H J, Lee Y S, et a1. A new anti-HIV flavonoid glucuronide from Chrysanthemum morifolium[J]. Planta Med, 2003, 69(9): 859-861. |
| [15] | Zhang H J, Kang M Q, Zhang H Q, et al. Matrix solid phase dispersion extraction for determination of flavonoids in the flower of Chrysanthemum morifolium Ramat. by capillary zone electrophoresis[J]. Anal Methods, 2014, 6: 766-773. |
| [16] | Niu Y, Yin L, Luo S, et a1. Identification of the anti-oxidants in Flos Chrysanthemi by HPLC-DAD-ESI/MS(n) and HPLC coupled with a post-column derivatisation system[J]. Phytochem Anal, 2013, 24(1): 59-68. |
| [17] | Cheng W M, Cheng X Q, Zeng Y C, et al. One new flavonoid glycoside from Chrysanthemum morifolium[J]. Asian J Chem, 2013, 25(4): 2335-2336. |
| [18] | 胡碧波, 吴祖帅, 蔡君, 等. 杭白菊中主要黄酮苷的测定及影响因素考察[J]. 中国中药杂志, 2006, 31(21): 1772-1775. |
| [19] | Wang T, Guo Q S, Mao P F. Flavonoid accumulation during florescence in three Chrysanthemum morifolium Ramat cv. ‘Hangju' genotypes[J]. Biochem Syst Ecol, 2014, 55(1): 79-83. |
| [20] | 金海红. 酵母细胞壁多糖对杭白菊抗氧化活性和黄酮类物质合成积累的影响[D]. 杭州: 浙江工商大学, 2011: 1-61. |
| [21] | 张晓媛, 段立华, 赵丁. 菊花化学成分及药理作用的研究[J]. 时珍国医国药, 2008, 19(7): 1702-1704. |
| [22] | 胡立宏, 陈仲良. 杭白菊的化学成分研究: 正戊基果糖甙的结构测定[J]. 植物学报, 1997, 39(2): 181-184. |
| [23] | 孙桂菊, 张菲菲, 马永健, 等. 杭白菊挥发油成分分析及β-榄香烯含量的测定[J]. 食品科学, 2008, 29(9): 506-510. |
| [24] | 鲍忠定, 秦志荣, 许荣飞, 等. 杭白菊挥发油化学成分的气相色谱-质谱联用技术分析[J]. 分析检验, 2003, 24(6): 120-121. |
| [25] | Chen J, Cao J, Gao W, et a1. Environmentally friendly ionic liquid-in-water microemulsions for extraction of hydrophilic and lipophilic components from Flos Chrysanthemi[J]. Analyst, 2013, 138(20): 5933-5941. |
| [26] | Kil B S, Lee Youb S. Allelopathic effects of Chrysanthemum morifolium on germination and growth of several herbaceous plants[J]. J Chem Ecol, 1987, 13(2): 299-308. |
| [27] | Chang C F, Kamya Y, Nagasawa H, et al. Occurence of two catechol derivatives in Chrysanthemum morifolium[J]. Agr Biol Chem, 1975, 39(2): 573-574. |
| [28] | Liang F, Hu C, He Z, et a1. An arabinogalactan from flowers of Chrysanthemum morifolium: structural and bioactivity studies[J]. Carbohydr Res, 2014, 387: 37-41. |
| [29] | 揭新明, 候霞. 菊花微量及宏量元素分析[J]. 广东微量元素学, 1997, 4(6): 62-64. |
| [30] | 沈颖旎, 冯恺, 黄海龙. 杭白菊中微量元素的研究进展[J]. 微量元素与健康研究, 2011, 28(5): 56-58. |
| [31] | Terashima S, Shimizu M, Horie S, et al. Studies on aldose reductase inhibitors from natural products. IV. Constituents and aldose reductase inhibitory effect of Chrysanthemum morifolium, Bxia orellana and Ipomoea batatas[J]. Chem Pharm Bull, 1991, 39(12): 3346-3347. |
| [32] | 李金玉. 杭白菊中脂肪酸组成的GC-MS分析[J]. 中国食物与营养, 2008, 3: 48-49. |
| [33] | Shahat A A, APers S, Pieters L, et al. Isolation and complete NMR assignment of the numbing principle from Chrysanthemum morifolium[J]. Fitoterapia, 2001, 72(l): 89-91. |
| [34] | 金建忠, 闻鸣, 申屠超. 杭白菊化学成分最新研究进展[J]. 食品工业科技, 2014, 3: 1-7. |
| [35] | He D, Ru X, Wen L, et al. Total flavonoids of Flos Chrysanthemi protect arterial endothelial cells against oxidative stress[J]. J Ethnopharmacol, 2012, 139(1): 68-73. |
| [36] | 汝海龙, 蒋惠娣, 林国华. 杭白菊总黄酮的舒血管作用[J]. 杭州师范学院学报: 自然科学版, 2005, 4(6): 411-414. |
| [37] | Jiang H, Xia Q, Xu W, et al. Chrysanthemum morifolium attenuated the reduction of contraction of isolated rat heart and cardiomyocytes induced by ischemia/reperfusion[J]. Pharmazie, 2004, 59(7): 565-567. |
| [38] | 张玮, 叶治国, 崔洁, 等. 杭白菊乙酸乙酯提取物对大鼠实验性心律失常的影响及其机制[J]. 浙江大学学报: 医学版, 2013, 38(4): 377-382. |
| [39] | Ma X, Li Y F, Gao Q, et a1. Direct vasorelaxation and vasoprotective properties of total flavonoids of Flos Chrysanthemi and its main bioactive components in rat resistance artery[J]. FASEB J, 2007, 21: 740. |
| [40] | Jiang H D, Cai J, Xu J H, et a1. Endothelium-dependent and direct relaxation induced by ethyl acetate extract from Flos Chrysanthemi in rat thoracic aorta[J]. J Ethnopharmacol, 2005, 101(1): 221-226. |
| [41] | 蒋惠娣, 王玲飞, 周新妹, 等. 杭白菊乙酸乙酯提取物的舒血管作用及相关机制[J]. 中国病理生理杂志, 2005, 21(2): 334-337. |
| [42] | 徐万红, 曹春梅, 夏强, 等. 杭白菊提取液对抗缺血再灌注引起的离体大鼠心肌收缩功能下降[J]. 中国病理生理杂志, 2004, 20(5): 822-826. |
| [43] | 蒋惠娣, 夏强, 徐万红, 等. 杭白菊的心血管药理作用及其机制研究进展[J]. 世界科学技术: 中药现代化, 2002, 4(2): 31-33. |
| [44] | 方雪玲, 王锡田, 黄淑如, 等. 杭白菊对小牛血管平滑肌细胞凋亡及其抗氧化性研究[J]. 浙江大学学报: 医学版, 2002, 24(9): 526-528. |
| [45] | 华波, 吕圭源. 杭白菊黄酮类化合物的心血管药理实验研究进展[J]. 青岛医药卫生, 2006, 38(4): 282-283. |
| [46] | 陈少华, 孙玉萍, 陈秀杉, 等. 降糖康对II型糖尿病患者血糖, 血液粘度, 胰岛素敏感性等指标的影响[J]. 中国中西医结合杂志, 1997, 17(11): 666-668. |
| [47] | Lii C K, Lei Y P, Yao H T, et al. Chrysanthemum morifolium Ramat. reduces the oxidized LDL-induced expression of intercellular adhesion molecule-1 and E-selectin in human umbilical vein endothelial cells[J]. J Ethnopharmacol, 2010, 128(1): 213-220. |
| [48] | 秦卫东. 杭白菊提取物抗氧化性能的研究[J]. 中国食品添加剂, 2000, 1(4): 21-23. |
| [49] | Singh R P, Agrawa P, Yim D, et a1. Aeacetin inhibits cell growth and cell cycle progression, and induces apoptosis in human prostate cancer cells: structure-activity relationship with linarin and linarin acetate[J]. Carcinogenesis, 2005, 26(4): 845-854. |
| [50] | Kim I S, Koppula S, Park P J, et a1. Chrysanthemum morifolium Ramat (CM) extract protects human neuroblastoma SH-SY5Y cells against MPP+-induced cytotoxicity[J]. J Ethnopharmacol, 2009, 126(3): 447-454. |
| [51] | 林琳. 杭白菊总黄酮对大鼠缺血/再灌损伤大脑的保护作用[D]. 杭州: 浙江大学, 2006: 1-57. |
| [52] | 康文艺, 黄嬛, 廉婷婷, 等. 杭白菊保肝作用研究[J]. 天然产物研究与开发, 2012, 24(11): 1634-1636. |
| [53] | Wang P, Pan X, Chen G, et a1. Increased exposure of vitamin A by Chrysanthemum morifolium Ramat extract in rat was not via induction of CYP1A1, CYP1A2, and CYP2B1[J]. J Food Sci, 2012, 77(6): 121-127. |
| [54] | 李英霞, 王小梅, 彭广芳. 不同产地菊花挥发油的抑菌作用[J]. 陕西中医学院学报, 1997, 20(3): 44. |
| [55] | Hu C Q, Chen K, Shi Q, et a1. Anti-AIDS agents, 10. Acacetin-7-O-β-D-galactopyranoside, an anti-HIV principle from Chrysanthemum morifolium and a structure-activity correlation with some related flavonoids[J]. J Nat Prod, 1994, 57(1): 42-51. |
| [56] | 张璐, 季巧遇, 周冬生, 等. 杭白菊的现代研究进展[J]. 江西中医药, 2011, 42(10): 60-62. |
| [57] | 孙桂菊, 康学军, 张菲菲, 等. 杭白菊挥发油解热作用及部分机理研究[C]. 第四届第二次中国毒理学会食品毒理学专业委员会与营养食品所毒理室联合召开学术会议论文集, 哈尔滨: 中国毒理学会, 2008: 216-219. |
| [58] | 杨俊, 蒋惠娣, 徐娟华. 杭白菊总黄酮的提取工艺及其含量的动态变化研究[J]. 中草药, 2002, 33(11): 988-990. |
 2014, Vol. 29
2014, Vol. 29


