头孢唑林钠自1971年上市以来在临床上得到了泛应用。第一代头孢菌素类抗菌药物头孢唑林钠抗菌谱广,除肠球菌属、耐甲氧西林葡萄球菌属外,对其他革兰阳性球菌具有良好的抗菌活性:对肺炎链球菌和溶血性链球菌高度敏感;对白喉杆菌、炭疽杆菌、李斯特菌和梭状芽抱杆菌敏感;对部分大肠埃希菌、奇异变形杆菌和肺炎克雷伯菌也具有良好的抗菌活性。该药临床广泛用于各种手术围术期预防性用药和治疗敏感细菌所致的呼吸道感染、皮肤软组织感染、骨和关节感染、败血症、肝胆系统感染等。五水头孢唑林钠是由中国食品药品检定研究院与深圳九新药业有限公司联合研制的国家四类新药,2005年在我国上市[1]。2005年以前,国内市场上流通的头孢唑林钠均为无定型产品,化学性质不稳定,澄清度、颜色和含量等指标在正常贮存条件下均有明显下降。头孢唑林钠有多种晶型,包括α型、β型、γ型和无定型[2]。五水头孢唑啉钠在预防性用药方面的疗效与头孢唑啉钠相似,但在治疗性用药方面的疗效优于头孢唑啉钠,且前者安全性优于后者[3]。
五水头孢唑林钠与普通头孢唑林钠的溶解性研究结果显示五水头孢唑林钠在灭菌注射用水和0.9%氯化钠注射液中溶解性均好于普通头孢唑林钠,有可能是五水头孢唑林钠晶型性质稳定;普通头孢唑林钠降解产生杂质使溶解性下降,具体原因有待进一步研究[4]。现已有一些比较五水头孢唑林钠与头孢唑林钠固体粉末在长期稳定性方面的研究[1]。马卫成研究了头孢唑林钠在果糖氯化钠注射液中的稳定性[5],谢玉芝等[6]采用紫外分光光度法测定了头孢唑林钠与5%葡萄糖溶液、生理盐水和5%加糖盐水中的配伍后72 h的稳定性。赖可[7]采用高效液相色谱法测定主药稳定性,考察了注射用头孢唑林钠溶液及其与氯化钠注射液、10%葡萄糖注射液、乳酸林格氏注射液、林格氏注射液和5%碳酸氢钠注射液的配伍后不同放置情况及不同时间的pH值变化,并将稳定性考察时间延长到10 d。
但比较两者在不同医用溶媒(乳酸钠林格注射液、果糖注射液、木糖醇注射液、转化糖电解质)中的稳定性研究工作没有相关报道,笔者选用了常用溶媒0.9%氯化钠注射液、5%葡萄糖注射液、5%木糖醇注射液、转化糖电解质注射液、果糖注射液和乳酸钠林格注射液为实验对象,考察头孢唑林钠两种不同晶型在溶媒中放置的稳定性,为临床选用合适的溶媒提供参考。
1 材料BP210S型电子天平(Sartorius公司);Dionex Ultimate 3000型高效液相色谱仪,配自动进样器。
注射用五水头孢唑林钠(1.0 g,深圳华润九新药业有限公司,批号1301413);注射用头孢唑林钠(1.0 g,汕头金石粉针剂有限公司,批号1207232)。
头孢唑林对照品,由中国药品生物制品检定所提供,批号0421-9603,质量分数99.3%。0.9%氯化钠注射液(250 mL∶2.25 g,广州百特医疗用品有限公司,批号GS1301021)、乳酸钠林格注射液(500 mL,浙江济民制药股份有限公司,批号130123D54)、转化糖电解质注射液(250 mL,四川美大康佳乐药业有限公司,批号12110862)、木糖醇注射液(250 mL∶木糖醇12.5 g,南京正大天晴制药有限公司,批号1302181)、果糖注射液(250 mL∶25 g,四川科伦药业股份有限公司,批号W212110501)、葡萄糖注射液(500 mL∶25 g,武汉滨湖双鹤药业有限责任公司,批号121226911)。
乙腈(色谱纯)为Tendia公司生产,其他试剂为分析纯,实验用水为纯化水。磷酸氢二钠(分析纯,上海试一化学试剂有限公司,批号080123);枸橼酸(分析纯,江苏无锡民丰化工厂,批号081120)。
2 方法与结果 2.1 外观检测分别称取注射用头孢唑林钠和注射用五水头孢唑林钠0.4 g,各10份,置25 mL具塞纳氏比色管中,分别用医用溶媒、5%葡萄糖注射液、0.9% NaCl 10 mL溶解后,室温(约25 ℃)自然放置和高温(40 ℃电热恒温干燥箱中)下恒温放置,于0、0.5、1、2、3、4、6 h采用《中国药典》2010年版附录ⅪA第一检查法[8, 9]分别观察不同时间下的溶液的颜色和澄明度的变化,结果各溶液均没有显著变化。
2.2 pH值测定取注射用头孢唑啉钠和注射用五水头孢唑林钠0.4 g,10份,置100 mL磨口锥形瓶中,使用6种溶媒分别配制4 mg/mL溶液。分别置于室温(约25 ℃)和高温(40 ℃电热恒温干燥箱中)中,于0、0.5、1、2、3、4、6 h采用《中国药典》2010年版附录Ⅺ H[8, 9]测定pH值,结果见表 1。结果显示温度和结晶形态对pH值没有显著影响。
| 表 1 头孢唑林钠在不同溶媒中不同时间的pH值 Table 1 pH values of Cefazolin Sodium samples in various solvents duringdifferent time |
分别称取注射用头孢唑林钠和五水头孢唑林钠0.4 g,各10份,置25 mL具塞纳氏比色管中,分别用医用溶媒、5%葡萄糖注射液、0.9% NaCl 10 mL溶解后,室温(约25 ℃)自然放置和高温(40 ℃电热恒温干燥箱中)下恒温放置,于0、0.5、1、2、3、4、6 h取样,即得。
2.3.2 色谱条件Dionex C18色谱柱(250 mm×4.6mm,5 μm);流动相:缓冲盐溶液(取无水磷酸氢二钠1.33 g、枸橼酸1.12 g,加水溶解并稀释成1 000 mL)-乙腈(88∶12),体积流量:1.0 mL/min;检测波长:254 nm;柱温:25 ℃。理论板数按头孢唑林钠峰计算应不小于2 500。
2.3.3 线性回归另取已测定水分的头孢唑林钠对照品适量,以流动相溶解,制成4.36 mg/mL对照品溶液。分别进样3、5、8、10、15、20、30、40 μL,测定峰面积。以峰面积对质量浓度绘制标准曲线,得方程Y=291.68 X-210.11(r=0.995 9),线性范围为13.08~174.40 μg。
2.3.4 测定结果精密量取各测试条件下的溶液0.5 mL,注入进样瓶,进样10 μL,记录色谱图,见图 1。外标法以峰面积计算头孢唑林钠的质量分数,结果见表 2。
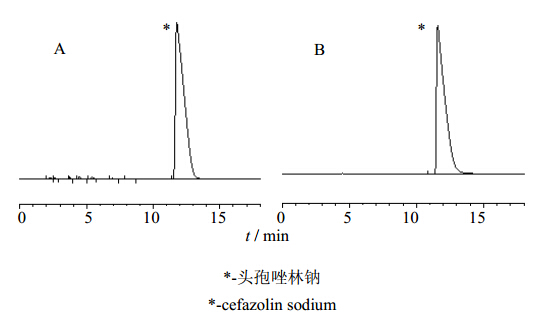 | 图 1 头孢唑啉钠对照品(A)和注射用头孢唑林钠(0.9% NaCl注射液)(B)的HPLC图谱Fig. 1 HPLC chromatograms of cefazolin sodium reference substance (A) and Cefazolin Sodium for injection (in 0.9% NaCl injection) (B) |
| 表 2 头孢唑林钠在不同溶媒中不同时间的测定结果 Table 2 Determination of cefazolin sodium in Cefazolin Sodium samples in various solvents duringdifferent time |
加入6种溶媒后在25、40 ℃下6 h内头孢唑林钠溶液均澄明,颜色无变化,无气泡、混浊及沉淀。室温和40 ℃时各溶液pH值呈明显上升趋势,0~6 h溶液的pH值相差不到0.3单位,基本稳定。以0 h时的质量分数为100%计算头孢唑林钠酯的质量分数。12 h内注射用头孢唑林钠和注射用五水头孢唑林钠在6种溶媒中的质量分数均大于95%。见表 3。
| 表 3 头孢唑林钠样品在不同溶媒中和不同温度下的稳定性 Table 3 Stabilities of CefazolinSodium samples in various solvents during different time |
结果显示,临床常用的抗菌药物溶媒0.9%氯化钠注射液、5%葡萄糖注射液、木糖醇注射液、5%乳酸钠林格注射液、果糖注射液以及转化糖电解质注射液都对注射用头孢唑林钠的稳定性无影响,临床上可以任意选用。
3 讨论近年来随着国内静脉配置中心工作的广泛开展,大多数药品,尤其是抗菌药物,经过静脉配置中心统一配置后再分发到临床使用。所以药物配制后的稳定性直接关系到其有效性和安全性。本实验结果显示,具有不同pH值的常用抗菌药物溶媒对头孢唑林钠的稳定性几乎无影响。
五水头孢唑林和头孢唑林钠的溶媒稳定性没有显著差异,在放置6 h内主要药物质量分数、pH值、溶液溶解性和澄明度均良好,两种晶型药物溶媒配置后药物质量分数均符合有效性要求。
研究显示[5],头孢唑啉钠与果糖氯化钠注射液混合后,在4 、25、35 ℃条件下,24 h内外观未见明显变化。4 ℃下,pH值随时间的变化并不是很大,温度越高,配伍液的pH值变化越明显。3种温度下,头孢唑啉的质量分数均保持在97%以上。另外,24 h内色谱图上无其他色谱峰出现,峰形保持稳定,说明配伍液是稳定的,受温度变化的影响不大。
研究表明[6]头孢唑林在5%葡萄糖注射液、0.9% NaCl、5%葡萄糖氯化钠注射液中比较稳定,在不避光条件下24h内质量分数下降小于3%。若冰箱放置可保存72 h甚至于更长时间。
研究结果显示[7],注射用头孢唑林钠与乳酸林格氏注射液配伍,在25、5 ℃条件下放置时,质量分数和pH值稳定良好。与10%葡萄糖注射液和5%碳酸氢钠注射液配伍后,pH值上升明显,均已超过《美国药典》规定,建议不与10%葡萄糖注射液和5%碳酸氢钠注射液配伍使用。
果糖是一种左旋六碳糖,为葡萄糖的同分异构体,具有直接供给热量、补充体液及营养全身的功效,并能在无胰岛素情况下代谢成糖原。在临床应用方面,国内有研究证实静脉输注10%果糖500 mL,3 h输完,前后血糖变化与0.9%氯化钠溶液对比差异无显著性[11, 12]。因此,果糖对糖尿病、肝病患者供给能量,补充体液比葡萄糖更适宜。此外,它能加速乙醇代谢,用于急性中毒的辅助治疗[13]。以上药用溶媒考虑作为注射用头孢唑林钠的稀释剂应用于临床,其配伍后尤其适用于烧创伤、术后及感染等胰岛素抵抗状态下或不适宜使用葡萄糖时需补充水分、钠盐、能源并且合并敏感菌感染的患者,这为特殊疾病患者的临床用药带来方便[14]。
| [1] | 陈宁, 申劲锋, 刘光荣. 一种新型螯合结构五水头唑林钠的长期稳定性考察[J]. 中国抗生素杂志, 2009, 34(1): 45. |
| [2] | 胡昌勤, 陈重, 尹利辉, 等. 一种具有螯合结晶水合物的头孢菌素及其制备方法[P]. 中国, CN1247596C. 2006-03-29. |
| [3] | 刘记, 李自华, 高慧玲, 等. 五水头孢唑啉钠对比头孢唑啉钠在预防性和治疗性用药中的有效性和安全性的系统评价[J]. 中国药房, 2013, 24(40):3797-3799. |
| [4] | 姜衍, 初阳, 姜明燕. 五水头孢唑林钠的溶解性影响研究[J]. 中国临床药理学杂志, 2013, 29(8): 605-608. |
| [5] | 马卫成, 徐爱仁, 应景艳. 头孢唑啉钠在果糖氯化钠注射液中的稳定性[J]. 分析现代实用医学, 2010, 22(5) :509-511. |
| [6] | 谢玉芝. 头孢唑林钠和常用输液配伍的稳定性考察[J]. 中国药学杂志, 1995, 30(5): 279-281. |
| [7] | 赖可, 陶静, 邓盛齐, 等. 注射用头孢唑林钠溶液稳定性及配伍稳定性研究[J]. 中国抗生素杂志, 2011, 36(1): 33-36. |
| [8] | 中国药典[S]. 二部. 2010: 206. |
| [9] | 国家食品药品监督管理局. 国家药品标准新药转正标准[M]. 北京: 人民卫生出版社, 2003. |
| [10] | 中国药典[S]. 二部. 2010: 151. |
| [11] | 王昕, 杨文英, 卜石, 等. 果糖注射液对糖尿病患者血糖及胰岛素的影响[J]. 中华糖尿病杂志, 2005, 13(5): 378-380. |
| [12] | 朱明炜, 郭莹, 叶国栋, 等. 果糖注射液对健康受试者血糖和胰岛功能的影响[J]. 中国临床营养杂志, 2005, 13(1): 4-7. |
| [13] | 陈新谦, 金有豫, 汤光. 新编药物学[M].15版. 北京: 人民卫生出版社, 2003 :645. |
| [14] | 杨燕贻, 田英, 王艳娇, 等. 不同输液种类对糖尿病患者血糖的影响[J]. 中国现代医学杂志, 2010, 20(17): 2679. |
 2014, Vol. 29
2014, Vol. 29


