2. 天津药物研究院 化学制药部, 天津 300193;
3. 天津中医药大学, 天津 300193
2. Centre for Chemical Pharmaceutical Research, Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China;
3. Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
丁酸氯维地平为超短效吡啶类钙通道阻滞剂,由英国阿斯利康公司研制并于2008年8月经美国FDA批准上市,主要用于急性高血压的治疗,以及心脏手术、经皮冠状动脉介入治疗等手术后的血压抑制[1]。根据丁酸氯维地平的结构、性质以及在原料药及脂肪乳制备过程中易发生水解脱羧,推测其可能产生降解杂质4-(2',3'-二氯苯基)-1,4-二氢-2,6-二甲基-3-吡啶甲酸甲酯。因此,设计了该化合物的合成,并利用MS和1H-NMR确证结构,通过HPLC进一步证实该化合物为丁酸氯维地平中的主要杂质之一,这对建立和完善丁酸氯维地平分析方法,制定已知杂质限度,提高质量标准,具有重要意义。根据目标化合物的结构,课题组以2,3-二氯苯甲醛为起始原料经缩合、环合、水解反应合成了目标化合物4-(2',3'-二氯苯基)-1,4-二氢-2,6-二甲基-3-吡啶甲酸甲酯,合成路线见图 1。
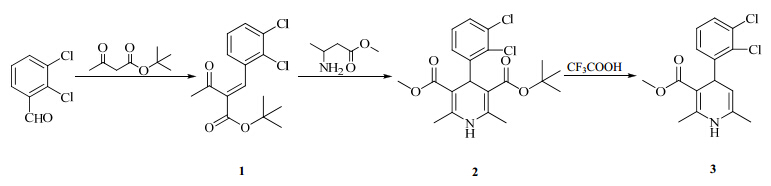 | 图 1 目标化合物的合成路线Fig. 1 Synthetic route of target compound |
HP 1200高效液相色谱仪(美国安捷伦公司);6520型Accurate-Mass-Q-TOF/MS质谱仪(美国安捷伦科技公司);Bruker 400 MHz核磁共振仪(德国Bruker公司);2,3-二氯苯甲醛(浙江洪波化工有限公司,质量分数>95%);其他所用试剂均为国产分析纯。
2 方法与结果 2.1 2-(2',3'-二氯亚苄基)乙酰乙酸叔丁酯(1)的合成[2]在250 mL四口瓶中,加入2,3-二氯苯甲醛(8.76 g,0.05 mol)、乙醇80 mL、甲酸324 mg、哌啶450 mg,乙酰乙酸叔丁酯(9.48 g,0.06 mol),20 ℃控温下搅拌3 h。旋蒸至干,加入醋酸乙酯100 mL萃取,水洗(80 mL×1),氯化钠饱和溶液洗(80 mL×1),取有机层,无水硫酸钠干燥。次日,滤过,滤液蒸干,得化合物2(14.8 g),mp 97~99 ℃,收率92%。
2.2 4-(2',3'-二氯苯基)-1,4-二氢-2,6-二甲基-3,5-吡啶二甲酸(叔丁基)(甲基)酯(2)的合成[3, 4, 5]在250 mL四口瓶中,加入化合物1(14.8 g,0.046 mol)、3-氨基丁烯酸甲酯(6.9 g,0.06 mol)、乙醇60 mL,搅拌,45 ℃下反应4 h。反应液蒸干,粗品经快速制备液相色谱分离,石油醚-醋酸乙酯(2∶1)洗脱,得化合物2(5 g),mp 154~157 ℃,收率26%。
2.3 4-(2',3'-二氯苯基)-1,4-二氢-2,6-二甲基-3-吡啶甲酸甲酯(3)的合成[6]在100 mL四口瓶中,加入化合物2(5 g,0.012 mol)、甲酸20 mL和氯仿30 mL的混合液,45 ℃下反应12 h。将反应液转移至烧杯中,加入氯仿150 mL,用饱和碳酸钠溶液调pH值为7。分液,取有机层用氯化钠饱和溶液洗(120 mL×2),有机层无水硫酸钠干燥。次日,滤过,滤液蒸干。粗品用快速制备液相色谱分离,石油醚-二氯甲烷(3∶1)洗脱,得化合物3(0.5 g),收率为13%。HPLC归一化法测得质量分数为98.3%。分子式为C15H15Cl2NO2,ESI-MS m/z:312.054 9 [M+H]+。1H-NMR(400 Hz,CDCl3)δ:1.692(3H,s,CH3),2.377(3H,s,CH3),3.466(3H,s,CH3),4.728(1H,d,CH,J=4.8 Hz),5.024(1H,d,CH,J=4.8 Hz),5.137(1H,s,NH),7.101~7.240(3H,m,Ar-H)。
色谱条件:Venusil MPC18色谱柱(4.6×25 mm,5 μL);进样量为20 μL;体积流量为1 mL/min;柱温为30 ℃;流动相为甲醇-水(70∶30)。
在上述色谱条件下,化合物3的保留时间为11.058 min,丁酸氯维地平产品中杂质的保留时间为11.063 min,将化合物3加入到丁酸氯维地平中进行HPLC分析,结果显示其对应的杂质峰明显增加,即可确定化合物3即为丁酸氯维地平中主要杂质之一。见图 2。
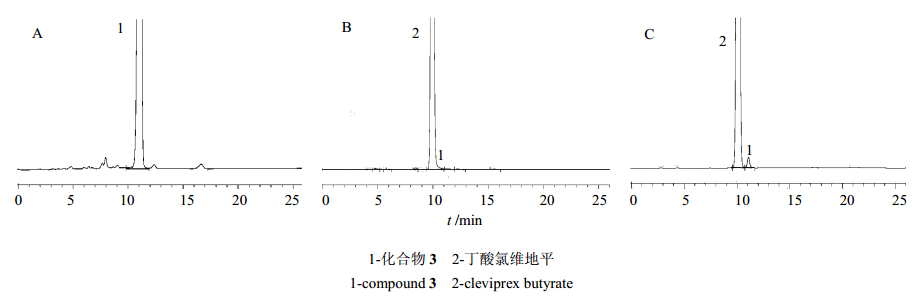 | 图 2 化合物3(A)、丁酸氯维地平(B)和化合物3+丁酸氯维地平混合物(C)的HPLC图谱Fig. 2 HPLC of compound 3 (A), cleviprex butyrate (B), and compound 3 + cleviprex butyrate (C) |
本课题组对丁酸氯维地平进行了合成研究,并且得到了适合工业化生产的工艺路线[7]。在丁酸氯维地平粗品的杂质研究中,发现LC-MS中氯维地平主峰后有一分子离子峰为312的杂质峰,根据氯维地平结构筛选,推测此杂质最有可能为4-(2',3'-二氯苯基)-1,4-二氢-2,6-二甲基-3-吡啶甲酸甲酯,遂设计以上合成路线,通过合成化合物3,确定了氯维地平中对应杂质的结构,进而证明此杂质为丁酸氯维地平水解脱羧降解产物。反应或储存过程中的高温、高湿和光照会加速其降解,因此在生产过程中控制反应温度,在运输和储存丁酸氯维地平成品时,避免高温和光照,可避免该杂质的过度产生。这对在有效期内保证产品质量,避免杂质含量超标至关重要。
| [1] | 邓超, 闫少杰, 黄汉忠, 等. 丁酸氯维地平成品中杂质的合成与结构鉴定[J]. 现代药物与临床, 2011, 26(1): 43-45. |
| [2] | Che Daqing, Guntoori B R, Murthy K S. Process to prepare 1,4-dihydropyridine intermediates and derivatives thereof[P]. US: 2004/0204604 A1, 2004-10-14. |
| [3] | 阿斯特拉公司. 新的制备方法[P]. 中国: 1207726, 1999-02-10. |
| [4] | Desai R, Aguilar D A, Aslam M, et al. Process to prepare dihydropyridine and derivatives thereof[P]. US: 5977369, 1999-11-02. |
| [5] | Ogawa T, Hatayama K, Maeda H. Mild and facile cleavage of 2-cyanoethyl ester using sodium sulfide or tetrabutyl-ammonium fluoride. Synthesis of 1,4-dihydro-pyridine monocarboxylic acids and unsymmetrical 1,4-dihydro-pyridine[J]. Chem Pharm Bull, 1994, 42(8): 1579-1589. |
| [6] | Gorlitzer K, Baltrusch H J. The reaction mechanism for formation of a 9-hydroxy-beta-carbolin-4-carboxylic acid from the nifedipine analogue biscyanoethyl ester[J]. Pharmazie, 2000, 55(10): 747-750. |
| [7] | 李树军, 黄汉忠, 闫少杰. 丁酸氯维地平的合成工艺[J]. 现代药物与临床, 2010, 25(6): 445-447. |
 2014, Vol. 29
2014, Vol. 29


