2. 中药制药共性技术国家重点实验室, 山东 临沂 276006;
3. 山东省中药制药新技术重点实验室, 山东 临沂 276006
2. State Key Laboratory of Generic Manufacture Technology of Chinese Traditional Medicine, Linyi 276006, China;
3. Shandong Provincial Key Laboratory of New Manufacture Technology of TCM, Linyi 276006, China
栀子为茜草科植物栀子Gardenia jasminoides Ellis的干燥成熟果实,具有泻火除烦、清热利尿、凉血解毒之功效[1]。栀子中主要有效成分为环烯醚萜苷类化合物[2],具有利胆、解热、抗炎、抗病毒、保护心脑血管等药理活性[3],但在体内消除快,滞留时间短,肠道内具广泛的吸收窗[4, 5],因此制备成缓释制剂可减少服用次数,提高患者顺应性,减少血药浓度的波动性,避免峰谷现象,降低药物的不良反应。本实验制备了持续释放12 h的栀子总苷缓释片,对其多组分释放度的评价方法进行了探讨。
1 仪器与试剂Agilent 1100高效液相色谱仪(安捷伦科技有限公司),ZRS—8G智能溶出试验仪(天津大学无线电厂),CARY300紫外分光光度计(瓦里安公司),AG285分析天平(梅特勒托利多公司)。
栀子苷(批号110749-200309,中国食品药品检定研究院);羟异栀子苷(自制,质量分数大于98%);京尼平龙胆二糖苷(自制,质量分数大于98%);乙腈为色谱纯,水为重蒸水,其他试剂均为分析纯。栀子总苷(UV法以栀子苷计质量分数为91.2%,自制);HPMC(K15M,批号ZB06012N01,美国陶氏公司);MCC(PH102,批号212824109,美国FMC公司);硬脂酸镁(批号131011,上海药用辅料厂)。
2 方法与结果 2.1 栀子总苷缓释片的制备取栀子总苷192 g、HPMC 144 g、MCC 144 g,过100目筛,混匀,用95%乙醇适量润湿,制成软材,过20目筛制粒,50 ℃干燥,过18目筛整粒,加适量硬脂酸镁混匀,用12 mm浅凹冲模压制成片,即得栀子总苷缓释片。每片质量480 mg,含栀子总苷192 mg,制备3批,批号分别为1311-1、1311-2和1311-3。
2.2 羟异栀子苷、京尼平龙胆二糖苷、栀子苷的测定 2.2.1 色谱条件Kromasil C18色谱柱(200 mm×4.6 mm,5 μm),流动相:乙腈(A)-0.05%三氟乙酸水溶液(B),梯度洗脱,0~15 min,95%~94%B;15~23 min,94%~90%B;23~35 min,90%~80%B;体积流量:1.0 mL/min;柱温:40 ℃;检测波长:327 nm;进样量:10 μL。
2.2.2 对照品溶液的制备精密称取羟异栀子苷、京尼平龙胆二糖苷、栀子苷对照品适量,用水溶解,定容,制得含羟异栀子苷0.121 0 mg/mL、京尼平龙胆二糖苷0.215 6 mg/mL、栀子苷1.113 0 mg/mL混合对照品溶液。
2.2.3 供试品溶液的制备取栀子总苷缓释片10片,研细,精密称取53.3 mg,置于100 mL量瓶中,加水超声10 min使溶解,加水至刻度,摇匀,过0.45 μm微孔滤膜滤过,即得(相当于1片栀子总苷缓释片溶解于900 mL溶出介质中)。
2.2.4 阴性样品溶液的制备按处方比例精密称取空白辅料21.3 mg,置于100 mL量瓶中,加水超声10 min使溶解,加水至刻度,摇匀,过0.45 μm微孔滤膜滤过,即得。
2.2.5 线性关系考察取混合对照品溶液0.1、0.2、0.4、0.6、0.8、1.0、1.2 mL置于10 mL量瓶中,加水定容,得到系列对照品溶液。按色谱条件进样测定,以峰面积为纵坐标,质量浓度为横坐标进行回归,得线性方程。羟异栀子苷:Y=1 608 X-1.966,r=0.999 9,线性范围0.121 0~1.452 0 μg;京尼平龙胆二糖苷:Y=1 002 X-6.455,r=0.999 9,线性范围0.215 6~2.587 2 μg;栀子苷:Y=1 359 X-2.130,r=1.000 0,线性范围1.113 0~13.356 0 μg。
2.2.6 专属性试验取对照品溶液、供试品溶液和阴性样品溶液各10 μL注入色谱仪,结果样品和对照品分离度均较好,辅料没有干扰,见图 1。
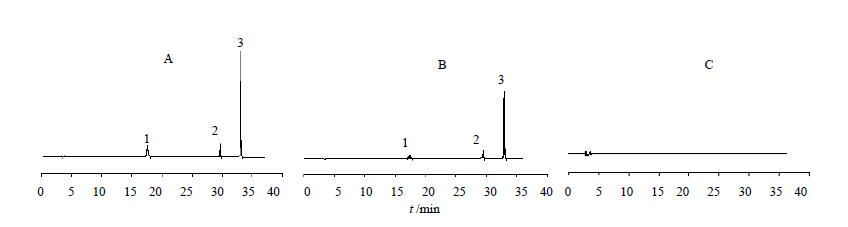 | 1-gardenoside 2-genipingeniobioside 3-geniposide 1-羟异栀子苷 2-京尼平龙胆二糖苷 3-栀子苷图 1 混合对照品(A)、栀子总苷缓释片(B)和阴性样品(C)的HPLC图谱Fig. 1 HPLC chromatograms of mixed reference substances (A),GardeniaTotal Glycosides Sustained-release Tablets (B),and negative sample (C) |
取混合对照品溶液0.1、0.6、1.2 mL置于10 mL量瓶中,加水至刻度。按上述色谱条件,重复进样6次,其相对保留时间稳定,记录峰面积,计算得羟异栀子苷、京尼平龙胆二糖苷、栀子苷峰面积的RSD值分别为1.00%、0.67%、0.77%;0.98%、0.79%、0.63%;1.12%、0.59%、0.75%。
2.2.8 稳定性试验取批号1311-1样品制备供试品溶液,分别于0、2、4、8、12、24 h测定,羟异栀子苷、京尼平龙胆二糖苷和栀子苷峰面积的RSD值分别为2.13%、2.03%、1.09%,说明供试品溶液在24 h内稳定。
2.2.9 重复性试验取批号1311-1样品10片研细,平行制备供试品溶液6份,分别测定,记录峰面积,计算得羟异栀子苷、京尼平龙胆二糖苷和栀子苷质量分数的RSD值分别为1.03%、1.38%、0.95%。
2.2.10 回收率试验精密称取干燥至恒定质量的栀子总苷原料5.7、11.5、19.2 mg,按处方比例加入相应空白辅料,使栀子总苷含量相当于栀子总苷缓释片总量的30%、60%、100%,分别制备3份,置于100 mL量瓶中,制备供试品溶液,分别测定,计算得羟异栀子苷、京尼平龙胆二糖苷、栀子苷的平均回收率分别为为99.53%、99.97%、100.53%,RSD值分别为0.56%、0.47%、0.22%。
2.2.11 样品测定取供试品溶液10 μL注入液相色谱仪,按色谱条件测定,计算各供试品溶液中羟异栀子苷、京尼平龙胆二糖苷和栀子苷的质量浓度。
2.3 栀子总苷的UV法测定 2.3.1 测定波长的选择分别取栀子苷对照品溶液、供试品溶液溶液和阴性对照溶液,以试剂作为空白,在200~400 nm波长扫描,结果对照品在237.4 nm处有最大吸收,供试品溶液在236.6 nm处有最大吸收,两者均在波长237 nm左右处有最大吸收,与栀子苷的最大吸收波长接近,阴性对照溶液在237 nm处几乎无吸收,故选择237 nm作为检测波长。
2.3.2 线性关系的考察精密称取栀子苷对照品,加水配成32.14 μg/mL的溶液,作为对照品溶液。精密量取栀子苷对照品溶液2.0、4.0、6.0、8.0、10.0 mL,分别置10 mL量瓶中,定容,同时以水做空白。照紫外-可见分光光度法(《中国药典》2010版一部附录VA)在237 nm波长处测定吸光度值。以吸光度值为纵坐标,栀子苷质量浓度为横坐标,计算得回归方程C=38.96 A-0.020 4,r=0.999 9。结果表明栀子苷在6.428~32.140 μg/mL呈良好的线性关系。
2.3.3 精密度试验配制质量浓度分别为6.428、16.07、32.14 μg/mL栀子苷对照品溶液,每个质量浓度均配制3份溶液,平行测定吸光度,计算得RSD值分别为1.26%、1.12%、0.69%。
2.3.4 稳定性试验取批号1311-1样品制备供试品溶液,置于37 ℃水浴中,分别于0、2、4、6、8、10、12、24 h测定吸光度值,结果其RSD值为2.02%,表明供试品溶液在24 h内基本稳定。
2.3.5 重复性试验取批号1311-1样品10片研细,依照“线性关系的考察”项下方法制备供试品溶液6份,分别测定,记录吸光度值,计算得其RSD值为1.83%。
2.3.6 回收率试验精密称取干燥至恒定质量的栀子总苷原料5.7、11.5、19.2 mg,按处方比例加入相应空白辅料,使栀子总苷含量相当于栀子总苷缓释片总量的30%、60%、100%,分别制备3份,依照“线性关系的考察”项下方法制备供试品溶液,分别测定,计算得栀子总苷回收率为102.4%,RSD值为0.12%。
2.3.7 测定方法取供试品溶液适当稀释,以水为空白,在237 nm波长处测定吸光度值,以栀子苷计计算栀子总苷的质量分数。
2.4 累积释放度的测定取3批栀子总苷缓释片样品,依照《中国药典》2010年版二部释放度测定法(附录XD第一法)转蓝法,转速100 r/min,溶出介质为脱气的水900 mL,溶出温度(37.0±0.5)℃。取栀子总苷缓释片6片,分别投入6个转篮内,从药片浸入溶出介质开始计时,在1、2、3、5、7、9、12 h分别取溶液5 mL,同时补充相同温度体积的水,所取溶液用0.45 μm微孔滤膜滤过,测定羟异栀子苷、京尼平龙胆二糖苷、栀子苷、栀子总苷的质量浓度(3批样品平均值),根据标准曲线的回归方程及累积释放度计算公式,计算各时间点的累积释放率,绘制累积释放曲线,见图 2。
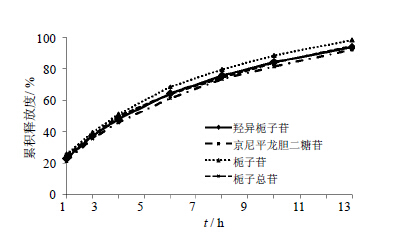 | 图 2 栀子总苷缓释片释放曲线Fig. 2 Cumulative release curves of GardeniaTotal Glycosides Sustained-release Tablets |
结果表明,栀子苷、京尼平龙胆二糖苷、羟异栀子苷和栀子总苷可持续释放12 h,12 h累积释放率达到90%以上,达到了缓释制剂要求,4条释放曲线比较接近,表明各组分释放同步较好。
2.5 各测定成分释放度相似性比较采用相似因子法,以栀子苷的累积释放率为参比,计算羟异栀子苷、京尼平龙胆二糖苷和栀子总苷累积释放率与其相比的相似因子(f2),f2分别为81%、72%、91%,说明释放的同步性较好,实现均衡释放。
2.6 释放机制考察分别将栀子苷、京尼平龙胆二糖苷、羟异栀子苷、栀子总苷的累积释放度(Mt/M∞)或待释放度(1-Mt/M∞)与时间(t)分别按零级方程、一级方程和Higuchi方程进行拟合,结果见表 1。结果表明栀子苷、京尼平龙胆二糖苷、羟异栀子苷、栀子总苷均以按Higuchi方程拟合的相关系数最大,R2>0.99,说明释放机制相同。
| 表 1 栀子总苷缓释片累积释放度拟合方程 Table 1 Cumulative release rate-time model fitting of GardeniaTotal Glycosides Sustained-release Tablets |
中药缓控释制剂的研究已取得了较大的进展[6, 7],但中药不同于化学药物,中药是通过多组分、多系统、多靶点发挥治疗作用的,各组分之间通过对吸收、代谢和作用的相互影响,产生综合治疗作用。中药各组分由于理化性质不同,释放速度会有所不同,在缓控释制剂能否同步释放应作为释放度评价的重点。本研究对栀子总苷缓释片中栀子苷、京尼平龙胆二糖苷、羟异栀子苷3个指标成分和栀子总苷的释放特度进行了测定,可持续释放12 h,各组分释放率相似因子大于70%,基本达到了同步释放,符合缓释制剂的要求。
本实验考察了盐酸溶液(pH 1.2)、磷酸盐缓冲液(pH 6.8)和水3种溶剂,结果栀子苷、京尼平龙胆二糖苷和羟异栀子苷3个指标成分的溶出差异不明显,均符合漏槽条件,这与栀子总苷水溶性较好有关,确定用水作为溶出介质。
| [1] | 中国药典 [S]. 一部. 2010. |
| [2] | 杨全军, 范明松, 孙兆林, 等. 栀子化学成分、药理作用及体内过程研究进展 [J]. 中国现代中药, 2010, 12(9): 7-12. |
| [3] | 陈 雁, 张现涛, 张雷红, 等. 栀子化学成分及药理研究进展 [J]. 海峡药学, 2010, 22(12): 1-5. |
| [4] | 杜先华, 牛 欣, 冯前进, 等. 栀子苷大鼠在体肠吸收动力学的研究 [J]. 华西药学杂志, 2008, 23(5): 558-560. |
| [5] | 王又红, 郭琳琳, 刘卫红, 等. 栀子苷在大鼠体内的药代动力学研究 [J]. 中医研究, 2011, 24(6): 29-31. |
| [6] | 魏元锋, 林 晓, 张 宁, 等. 中药口服缓控释给药系统质量评价体系的构建 [J]. 药学学报, 2010, 45(4): 430-435. |
| [7] | 张立兵, 葛卫红, 张继稳. 我国中药缓控释制剂的研究状态分析 [J]. 世界科学技术: 中医药现代化, 2007, 9(5): 83-90. |
 2014, Vol.
2014, Vol. 


